Clear Sky Science · nl
Structurele modellering en dockinganalyse van canonische en nieuwe resistentie-geassocieerde missense-mutaties in Sudanese Escherichia coli
Waarom dit van belang is voor alledaagse gezondheid
Infecties die resistent zijn tegen antibiotica zijn geen zeldzame medische curiositeiten meer; ze vormen een groeiende bedreiging voor routinematige behandelingen van urineweginfecties, chirurgische ingrepen en intensive care. Deze studie bekijkt Escherichia coli-bacteriën uit Soedan en stelt een zeer gerichte vraag: hoe veranderen kleine genetische afwijkingen in bacteriële eiwitten de werking van veelgebruikte antibiotica? Door structurele modellering op de computer te gebruiken in plaats van dure laboratoriumexperimenten, ontdekken de auteurs verborgen resistentiepatronen die standaardtests en wereldwijde databanken kunnen missen—vooral in omgevingen met weinig middelen waar resistentie het snelst toeneemt. 
Een kijkje in de gereedschapskist van de bacterie
De onderzoekers concentreerden zich op "missense"-mutaties—éénletter-DNA-veranderingen die één bouwsteen van een eiwit voor een andere laten inspringen. Ze analyseerden volledige genoomsequenties van 55 E. coli-isolaten afkomstig uit Soedan en zoomen in op bacteriële eiwitten die directe doelwitten zijn van belangrijke antibioticaklassen, waaronder fluoroquinolonen, macroliden en rifampicine. Deze doelwitten omvatten DNA-wringende enzymen (gyrase en topoisomerase IV), het eiwitten makende ribosoom en het enzym RNA-polymerase. Van de 71 in deze eiwitten gevonden mutaties werden er 19 door meerdere predictietools aangemerkt als waarschijnlijk schadelijk voor de eiwitfunctie, en opvallend genoeg bleken de meeste hiervan nieuwe variaties die nog niet in wereldwijde resistentiedatabanken zijn gekatalogiseerd.
Nieuwe probleemgebieden in bekende doelwitten
Een aantal van de belangrijkste veranderingen bleek zich te clusteren in een ribosomaal eiwit genaamd L22, dat helpt het kanaal te vormen waarlangs pas gemaakte eiwitten het ribosoom verlaten. Dit gebied fungeert ook als dockingsite voor macrolide-antibiotica zoals erytromycine. De studie identificeerde een geconcentreerde set eerder niet gerapporteerde L22-mutaties, veelal in één stam, die precies langs dit kanaal en op contactpunten met ribosomaal RNA liggen. Computationele analyses suggereerden dat verschillende van deze veranderingen de lokale structuur destabiliseren of flexibeler maken, waardoor het kanaal mogelijk zodanig wordt hervormd dat macrolide-moleculen minder goed passen. Tegelijkertijd verschenen meer bekende "canonische" resistentiemutaties in DNA-verwerkende eiwitten ParC en ParE en in RNA-polymerase, wat bevestigt dat Sudanese stammen enkele wereldwijde resistentiekenmerken delen maar ook hun eigen lokale varianten hebben.
Hoe verandering in vorm de grip van antibiotica verzwakt
Het team ging verder dan enkel sequentielijsten en onderzocht hoe deze mutaties de driedimensionale passing tussen antibiotica en hun doelwitten zouden kunnen veranderen. Met behulp van moleculaire docking-simulaties vergeleken ze hoe verschillende geneesmiddelen binden aan normale en gemuteerde eiwitten. Voor het topoisomerase IV-eiwit ParC verzwakten sleutelmutaties nabij de drug-contactplaats de voorspelde binding van de fluoroquinolon trovafloxacine aanzienlijk, wat duidt op een lossere grip bij het enzym–DNA–drug-kruispunt. In het gerelateerde ParE-eiwit verminderden mutaties de binding van novobiocine enigszins. Daarentegen leek een nieuwe mutatie in het gyrase-eiwit GyrA de structuur van het enzym te destabiliseren zonder de bindingssterkte van de fluoroquinolon moxifloxacine merkbaar te veranderen, wat suggereert dat resistentie soms kan ontstaan door subtiele verstoring van enzymfunctie in plaats van door eenvoudigweg het geneesmiddel weg te stoten. 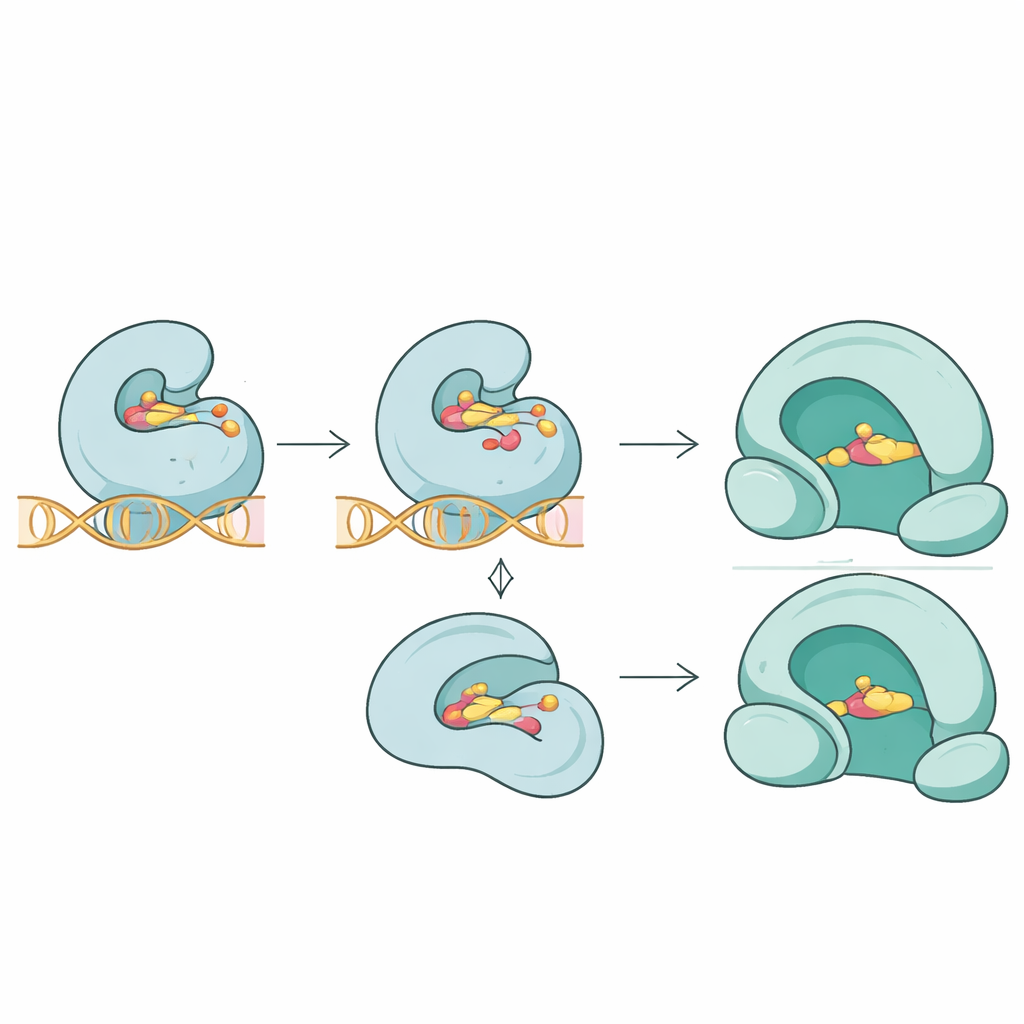
Gemengde effecten op verschillende geneesmiddelen
Niet alle mutaties hadden hetzelfde effect. Klassieke rifampicine-resistentieveranderingen in het RNA-polymerase-eiwit RpoB verstoorden de binding van een nieuwere, structureel afwijkende remmer die een nabijgelegen site target, maar weinig, wat suggereert dat toekomstige geneesmiddelen zo ontworpen kunnen worden dat ze bestaande resistentiepatronen omzeilen. Voor het ribosomale eiwit L22 lieten dockingstudies met erytromycine een bont palet aan uitkomsten zien: sommige mutaties verzwakten de binding, sommige hadden weinig effect, en één verbeterde zelfs licht de voorspelde passing. Deze resultaten benadrukken dat resistentie zelden alles-of-niets is; elke mutatie duwt eiwitstabiliteit, flexibiliteit en geneesmiddelbinding in verschillende richtingen, en het uiteindelijke effect op de behandeling hangt af van hoe deze veranderingen zich combineren in een levende bacteriële cel.
Wat dit betekent voor patiënten en surveillance
Voor een lekenpubliek is de kernboodschap dat bacteriën op plaatsen als Soedan resistentie ontwikkelen via zowel bekende als minder bekende routes. De bekende routes omvatten klassieke mutaties die al door internationale programma's worden gevolgd, maar deze studie toont aan dat veel extra, lokaal verrijkte mutaties antibiotica op subtielere manieren kunnen verzwakken. Door deze veranderingen op gedetailleerde eiwitstructuren in kaart te brengen, leveren de auteurs een korte lijst met mutaties die in het laboratorium getest en in regionale diagnostische panelen opgenomen zouden moeten worden. Praktisch gezien pleit hun werk ervoor dat slimme computermodellering landen met beperkte laboratoriumcapaciteit kan helpen om opkomende resistentie beter in de gaten te houden, wat uiteindelijk betrouwbaardere behandelkeuzes ondersteunt en het ontwerp van geneesmiddelen stimuleert die de bacteriële evolutie een stap voor blijven.
Bronvermelding: Sage, E.E., Ibrahim, S.A.E., Firdaus-Raih, M. et al. Structural modeling and docking analysis of canonical and novel resistance-associated missense mutations in Sudanese Escherichia coli. Sci Rep 16, 8995 (2026). https://doi.org/10.1038/s41598-026-39491-7
Trefwoorden: antimicrobiële resistentie, Escherichia coli, missense-mutaties, structurele bioinformatica, Soedan