Clear Sky Science · nl
Rol van atoomkrachtmicroscopie bij de karakterisering van heterotiepe kankersferoïden en hun interactie met microplasticdeeltjes
Waarom het gevoel van kankweefsel ertoe doet
Kanker wordt vaak beschreven in termen van genen en afwijkende cellen, maar het fysieke gevoel—hoe zacht of stijf het weefsel is—vormt ook hoe een tumor groeit en op zijn omgeving reageert. Deze studie onderzoekt kleine driedimensionale klusters van longkankercellen, sferoïden genoemd, en stelt twee praktische vragen: kunnen we een hoge-resolutie ‘aanraak’-microscoop gebruiken om betrouwbaar te meten hoe stijf deze mini‑tumoren zijn, en beïnvloedt die stijfheid hoe ze interageren met in lucht aanwezige microplasticdeeltjes die de longen kunnen bereiken?
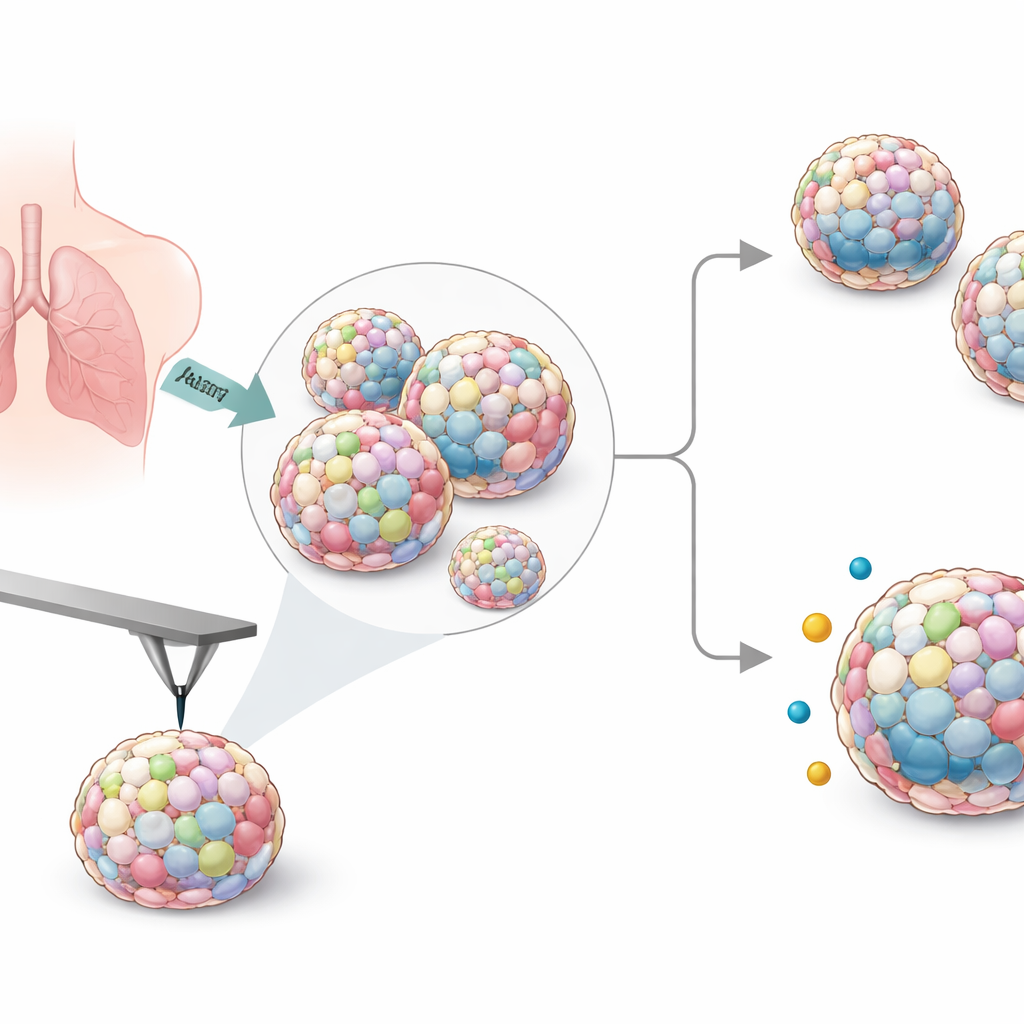
Mini‑longtumoren in het lab opbouwen
Om de complexe samenstelling van echte tumoren na te bootsen, kweekten de onderzoekers gemengde sferoïden uit zes menselijke longkankercellijnen samen met ondersteunende cellen, fibroblasten, en soms immuunachtige macrofagen. Ze probeerden verschillende methoden om deze klusters te vormen en kozen uiteindelijk speciale laag‑hechtende platen die betrouwbaar ronde, stabiele sferoïden opleverden die groot genoeg waren om te hanteren. Door het aantal en de verhoudingen van cellen aan te passen, creëerden ze zowel kleine als grotere sferoïden en kozen daarna een standaardrecept dat consistent werkte over alle kankerceltypen heen.
Inzicht in de binnenkant en controle van celgezondheid
Zodra de sferoïden gevormd waren, onderzocht het team hun interne structuur en celgedrag met verschillende kleuringen en snijtechnieken. Dunne snedes toonden dat sommige kankercelcombinaties zeer compacte bolletjes vormden, terwijl andere losser waren met meer open ruimtes. Fibroblasten neigden zich naar het centrum te schikken, vooral in de meeste celcombinaties, terwijl de kankercellen zich naar de buitenkant concentreerden. Live‑dead kleuring toonde een bekend patroon dat ook in echte tumoren voorkomt: goed gevoede levende cellen aan de rand en meer beschadigde of stervende cellen in de laag‑zuurstof kern. Een DNA‑labeltest voor celdeling liet zien dat bij de meeste sferoïden cellen door de hele structuur heen nog konden prolifereren, hoewel één kankercellijn (Calu‑3) voornamelijk aan de buitenrand deelde.
Stijfheid meten met een nanoschaalsonde
Om textuur in cijfers om te zetten, gebruikten de wetenschappers atoomkrachtmicroscopie, waarbij een piepklein, scherp probe zacht op het sferoïde-oppervlak drukt en registreert hoeveel het indeukt. Hieruit berekenden ze de Youngs modulus, een standaardmaat voor stijfheid. Hoewel de sferoïden vergelijkbaar in grootte waren, varieerde hun stijfheid sterk afhankelijk van welke longkankerlijn ze bevatten. Sferoïden met A549‑cellen behoorden tot de zachtste, terwijl die met H23 of HCC827 duidelijk stugger waren. Het toevoegen van macrofagen verhoogde over het algemeen de stijfheid voor meerdere kankertypes. Toen het team deze waarden vergeleek met hoe snel de oorspronkelijke kankercellen in platte kweek groeiden, vonden ze dat langzamer delende cellen de neiging hadden stuggere sferoïden te vormen, wat groeigedrag koppelt aan mechanische eigenschappen.
Contact met microplastics testen
Aangezien microscopische plasticfragmenten in longtumoren zijn aangetroffen, brachten de onderzoekers hun sferoïden vervolgens bloot aan fluorescerende polystyreenbolletjes van ongeveer één micrometer, in concentraties vergelijkbaar met die gemeten in menselijk bloed. Onder stilstaande omstandigheden klonterden de deeltjes samen en kleefden ongelijkmatig aan één zijde van de sferoïden, dus schakelde de groep over op zacht wiegen van de monsters om beter stromende lichaamsvloeistoffen na te bootsen. Onder deze dynamische condities hechtten of drongen slechts enkele individuele deeltjes binnen in de buitenste cellagen door, te weinig voor nauwkeurige telling. In plaats daarvan keerde het team terug naar stijfheidsmetingen. Na blootstelling werden veel sferoïde‑typen iets stijver, wat overeenkomt met het vasthaken of vastklemmen van stijve plastic bolletjes aan het oppervlak, maar deze verandering toonde geen duidelijke, eenvoudige afhankelijkheid van de oorspronkelijke stijfheid van het sferoïde.
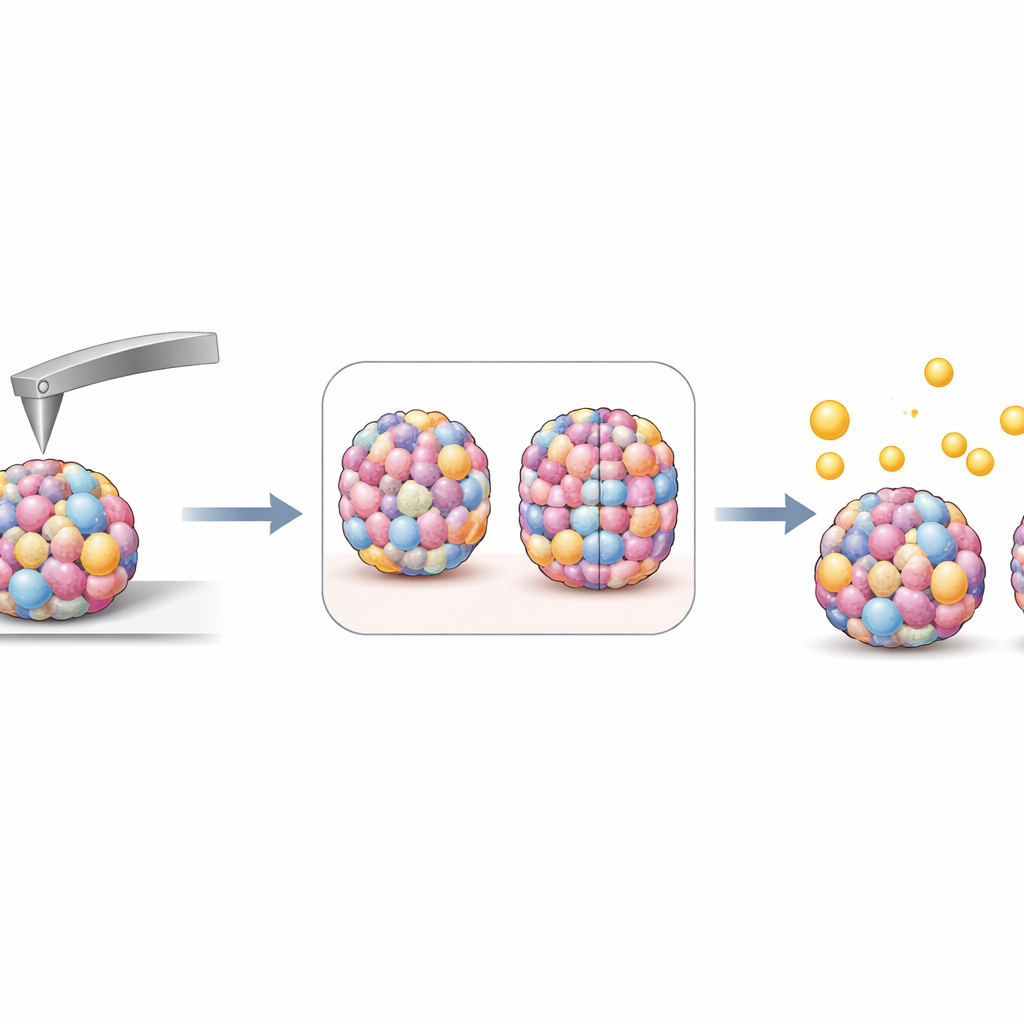
Wat dit betekent voor toekomstige kanker‑ en vervuilingsstudies
Het werk laat zien dat stijfheid een informatieve extra parameter is voor het beschrijven van driedimensionale kankermodellen die er anders vergelijkbaar uitzien in grootte en vorm. De manier waarop cellen zich binnen het sferoïde schikken en hoe snel ze zich delen verklaart deze mechanische verschillen slechts gedeeltelijk, wat suggereert dat stijfheid verborgen aspecten van tumorgedrag vangt. Hoewel deze studie geen eenvoudige regel vond die sferoïde‑stijfheid koppelt aan microplasticopname bij realistische deeltjesniveaus, benadrukt ze dat onder zachte, bewegende omstandigheden slechts een klein aantal zulke deeltjes waarschijnlijk aan tumorachtige weefsels hecht. Op langere termijn kan het combineren van gedetailleerde stijfheidsmetingen met gevoeliger deeltjesvolgonderzoek onderzoekers helpen beter te voorspellen hoe tumoren reageren op zowel anticancerous geneesmiddelen als op milieuverontreinigende stoffen die de longen bereiken.
Bronvermelding: Kolesnik, T., Öhlinger, K., Absenger-Novak, M. et al. Role of atomic force microscopy in characterization of heterotypic cancer spheroids and their interaction with microplastic particles. Sci Rep 16, 8303 (2026). https://doi.org/10.1038/s41598-026-39445-z
Trefwoorden: longkankersferoïden, atoomkrachtmicroscopie, celstijfheid, microplastics, tumormicro-omgeving