Clear Sky Science · nl
Ontdekking van potentiële antivirale verbindingen en versnelling van therapeutische ontdekking tegen het apenpokkenvirus
Waarom dit onderzoek nu belangrijk is
Apenpokken, tegenwoordig vaak mpox genoemd, is geëvolueerd van een zeldzame tropische infectie naar een wereldwijde zorg, met uitbraken op meerdere continenten in de afgelopen jaren. In tegenstelling tot COVID-19 is er nog geen geneesmiddel dat specifiek is ontwikkeld om dit virus te stoppen. Deze studie gebruikt geavanceerde computertools om te zoeken naar nieuwe kleine moleculen die het virus op zijn meest kwetsbare punt kunnen verlammen: zijn vermogen zich te verbergen voor ons immuunsysteem. Als dit in het laboratorium wordt bevestigd, zouden deze kandidaatverbindingen het startpunt kunnen vormen voor een nieuwe klasse antivirale middelen.
Hoe het virus zich verbergt voor onze verdediging
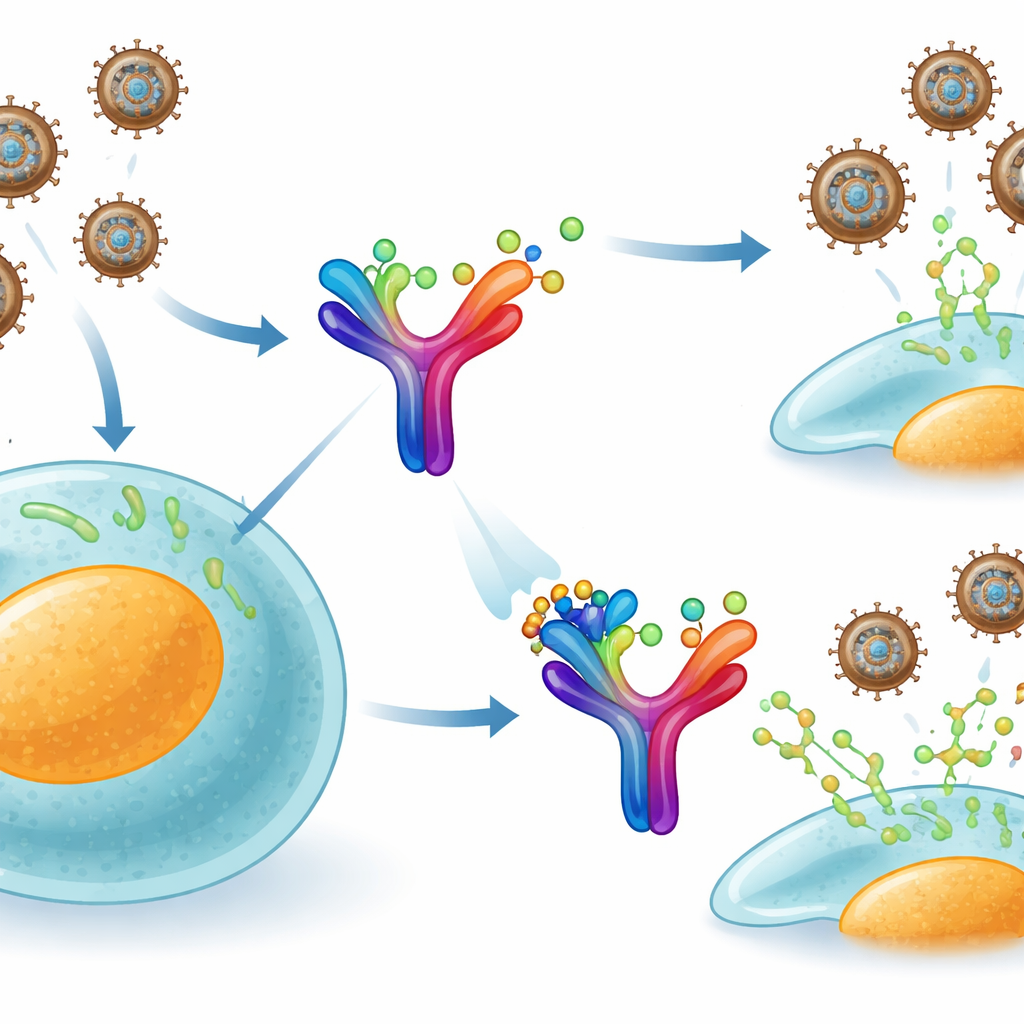
Apenpokken behoort tot dezelfde brede familie als pokken en gebruikt een slimme truc om het immuunsysteem te ontwijken. Onze cellen geven een signaalmolecuul af dat interferon-gamma heet, dat normaal gesproken naburige cellen waarschuwt en antivirale verdedigingen activeert. Het virus maakt echter zijn eigen uitgescheiden eiwit, B8R genoemd, dat buiten geïnfecteerde cellen ronddrijft. B8R bootst sterk ons eigen interferon-gamma-receptor na en grijpt deze immuunsignalen voordat ze hun werkelijke doel kunnen bereiken. In feite werkt het als een spons: het zuigt de alarmberichten van het lichaam op en verhindert zo een volledige antivirale reactie.
Computers gebruiken om slimmere behandelingen te ontwerpen
Traditionele geneesmiddelenontdekking kan vele jaren en enorme middelen vergen. Hier wendden de onderzoekers zich tot computerondersteund geneesmiddeldesign om het proces te versnellen. Omdat er geen experimentele 3D-structuur van het B8R-eiwit bestaat, gebruikten ze eerst AlphaFold-gebaseerde tools om de atomaire vorm te voorspellen en controleerden ze zorgvuldig de kwaliteit van dat model. Met een betrouwbare 3D-structuur in handen hebben ze virtueel 5000 kleine moleculen uit een chemische bibliotheek gescreend. Regels die beschrijven wat gewoonlijk een pilachtig geneesmiddel maakt (zoals grootte, vorm en oplosbaarheid) werden gebruikt om slechte kandidaten eruit te filteren, waardoor 2890 veelbelovende verbindingen overbleven voor gedetailleerde tests tegen het B8R-eiwitmodel.
Het vinden van een veelbelovende chemische "sleutel"
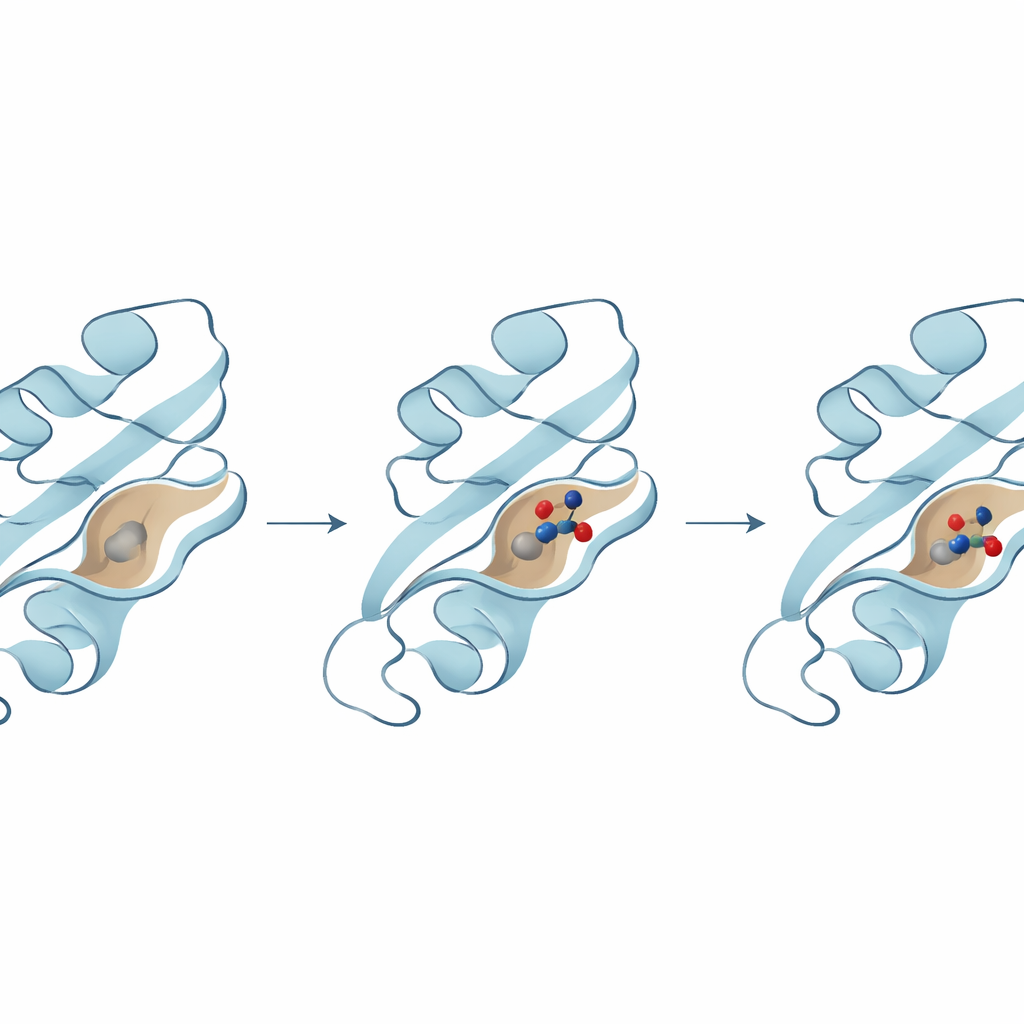
De volgende stap was nagaan welke moleculen precies in een belangrijk pocket op het B8R-oppervlak konden passen, waar het normaal met interferon-gamma zou interageren. Het team gebruikte moleculair docken, een techniek die miljarden mogelijke posities van een molecuul in de eiwitpocket uitprobeert en beoordeelt hoe stevig het zou binden. Drie topkandidaten kwamen naar voren, elk voorspeld sterke interacties te vormen met sleutelaminozuren in de pocket. Eén verbinding toonde in het bijzonder de sterkste bindingsenergie en maakte meerdere stabiliserende contacten met kritieke residuen die helpen het op zijn plaats te verankeren, wat suggereert dat het bijzonder effectief zou kunnen zijn in het blokkeren van de activiteit van B8R.
Moleculen in beweging over tijd bekijken
Eiwitten en geneesmiddelmoleculen zijn niet stijf; ze bewegen, buigen en 'ademen' in hun waterige omgeving. Om dit vast te leggen, voerden de onderzoekers lange moleculaire dynamicasimulaties uit—virtuele films van honderden nanoseconden—om te zien hoe elk eiwit–verbinding-paar zich in de loop van de tijd gedroeg. Deze simulaties toonden aan dat de best presterende verbinding diep in de B8R-pocket bleef zitten, waarbij het eiwit zich lichtjes aanpaste maar structureel stabiel bleef. Daarentegen zwierven de andere twee verbindingen meer, verschoven naar alternatieve pockets of vertoonden grotere fluctuaties, wat wijst op zwakkere of minder betrouwbare binding. Aanvullende analyses van flexibiliteit, energie en grootschalige bewegingen wezen allemaal naar dezelfde winnaar: één verbinding die consequent het meest stabiele en energetisch gunstige complex opleverde.
Wat dit kan betekenen voor toekomstige behandelingen
De studie beweert niet een afgewerkt geneesmiddel te hebben ontdekt en er zijn nog geen experimenten in cellen of dieren uitgevoerd. In plaats daarvan levert het een sterke, datagedreven uitgangspositie: een specifiek klein molecuul dat er ideaal gevormd uitziet om zich vast te klemmen in het B8R-eiwit van apenpokken en mogelijk het interferon-alarm van het lichaam te herstellen. Door de immuunontwijkingsstrategie van het virus te richten in plaats van het replicatiemechanisme, biedt deze benadering een nieuw invalshoek voor antivirale therapie. De auteurs betogen dat hun leidende verbinding nu in het laboratorium getest zou moeten worden, waar de capaciteit om B8R te blokkeren en mpox-infectie te beperken direct gemeten kan worden. Als die tests slagen, zou dat de weg kunnen effenen naar een gerichte behandeling die het immuunsysteem helpt het virus beter te zien en te stoppen.
Bronvermelding: Ahmad, F., Navid, A., Irfan, M. et al. Discovery of potential antiviral compounds and accelerating the therapeutic discovery against monkeypox virus. Sci Rep 16, 8306 (2026). https://doi.org/10.1038/s41598-026-39427-1
Trefwoorden: apenpokken antiviraal, immuunontwijking, geneesmiddelenontdekking, computationale modellering, interferon signalering