Clear Sky Science · nl
Het verlies van mechanische belasting veroorzaakt synovitis, fibrose en degeneratie van het gewrichtskraakbeen via verschillende synoviale celsubsets
Waarom rust voor gewrichten risicovol kan zijn
Veel mensen weten dat overbelasting van gewrichten slijtage kan veroorzaken, maar deze studie toont aan dat te weinig gebruik hen ook kan schaden. Onderzoekers gebruikten een muismodel om te onderzoeken wat er in kniegewrichten gebeurt wanneer beweging en draaglast gedurende weken sterk worden verminderd, vergelijkbaar met langdurig gips, verlamming of langdurig bedlegerig zijn. Door microscopische weefselveranderingen en genactiviteit per cel te volgen, ontdekten ze hoe het wegvallen van mechanische stress een kettingreactie in het synovium (de gewrichtsvoering) op gang brengt die uiteindelijk het gladde kraakbeen aantast dat nodig is voor pijnloze beweging.
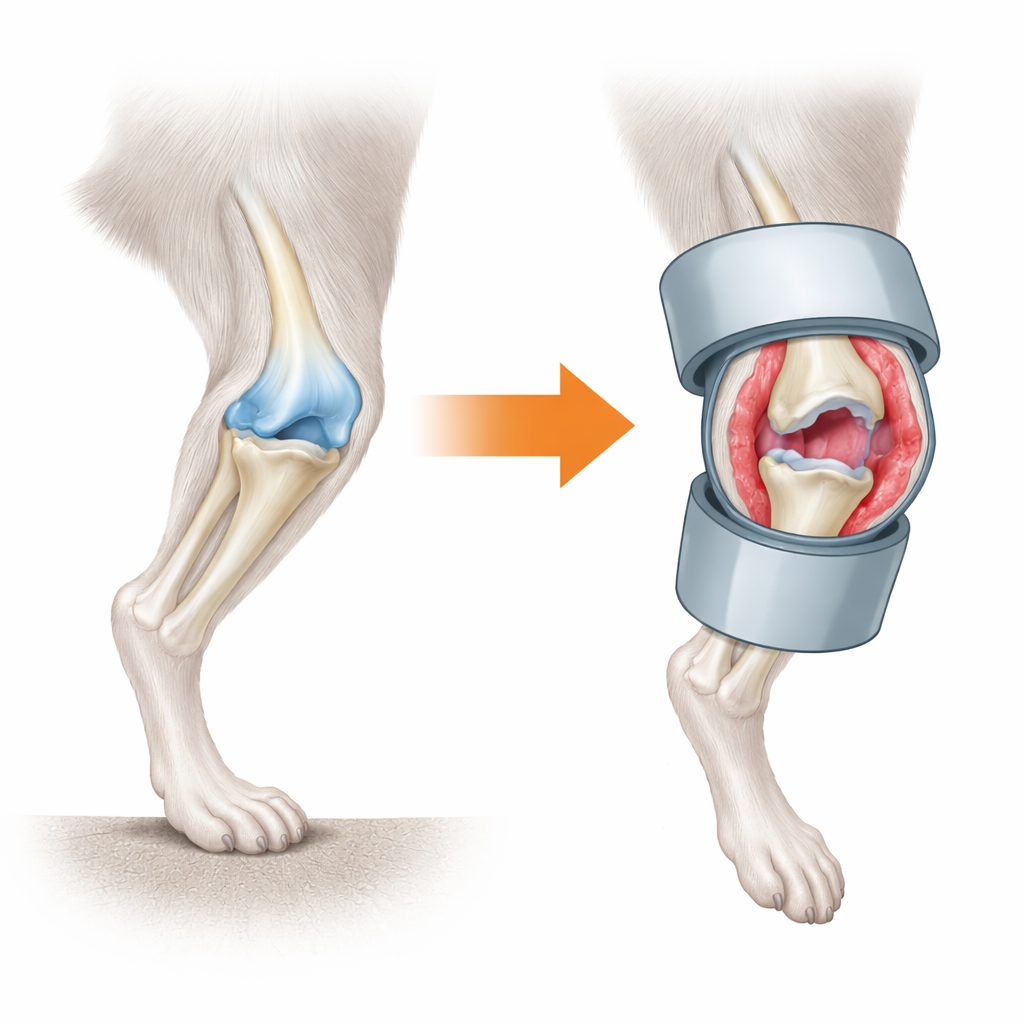
Wat er gebeurt als een knie stopt met bewegen
Het team maakte een model van "geminimaliseerde mechanische stress" door muenknees te immobiliseren met kleine plastic cilindertjes en de staarten van de dieren op te hangen zodat de achterpoten geen gewicht droegen. Al binnen drie dagen raakte het synovium ontstoken: de cellagen werden dikker, er verschenen nieuwe bloedvaten en immuuncellen stapelden zich op. In de twee weken daarna ontwikkelde dat synovium vezelig, littekenachtig weefsel en verstijfde het gewricht. Kraakbeen — het gladde weefsel dat de uiteinden van botten bekleedt — brak niet meteen af. In plaats daarvan toonde het pas ruwheid en verlies van oppervlaktemateriaal nadat de synoviale veranderingen goed op gang waren, en deze schade verslechterde over zes weken.
Beweging en druk als medicijn voor gewrichten
De onderzoekers vroegen zich vervolgens af of deze veranderingen omkeerbaar waren. Na twee weken immobilisatie en ontlasting herstelden sommige muizen alleen de gewrichtsbeweging terwijl ze onbelast bleven, en andere kregen zowel beweging als draaglast terug. In beide groepen nam de synoviale ontsteking af en werd de voering weer dunner richting normaal, wat aantoont dat eenvoudige beweging sterk van invloed is op de gezondheid van het synovium. Kraakbeen herstelde echter het best wanneer zowel beweging als belasting werden hersteld. Op moleculair niveau waren genen die betrokken zijn bij de opbouw van gezond kraakbeen sterk gereduceerd tijdens het niet-gebruik, maar herstelden grotendeels toen de gewrichten weer mochten bewegen en gewicht dragen. Dit suggereert dat kraakbeen afhankelijk is van een combinatie van glijdende beweging en milde druk om zijn structuur te behouden.
Hoe cellen in de gewrichtsvoering kraakbeenschade aansturen
Dieper gravend onderzochten de wetenschappers welke genen in het synovium werden geactiveerd naarmate de schade vorderde. Ze vonden verhoogde activiteit van genen verbonden aan fibrose, weefselremodellering en enzymen die kraakbeen kunnen afbreken. Veel van deze signalen kwamen van immuungerelateerde boodschappers, zoals inflammatoire cytokinen en groeifactoren, die nabijgelegen kraakbeencellen kunnen beïnvloeden. Single-cell RNA-sequencing toonde dat ontlasting de cellulaire samenstelling binnen het synovium hervormde. Twee ongebruikelijke celgroepen namen toe in geïmmobiliseerde gewrichten: myofibroblast-achtige cellen gespecialiseerd in het produceren van vezelige matrix, en een subset van macrofagen die hoge niveaus van inflammatoire moleculen en kraakbeenafbrekende enzymen tot expressie brachten. Gezamenlijk vormden deze cellen een distinctief, schadebevorderend micro-omgevingsgebied rond het gewricht.
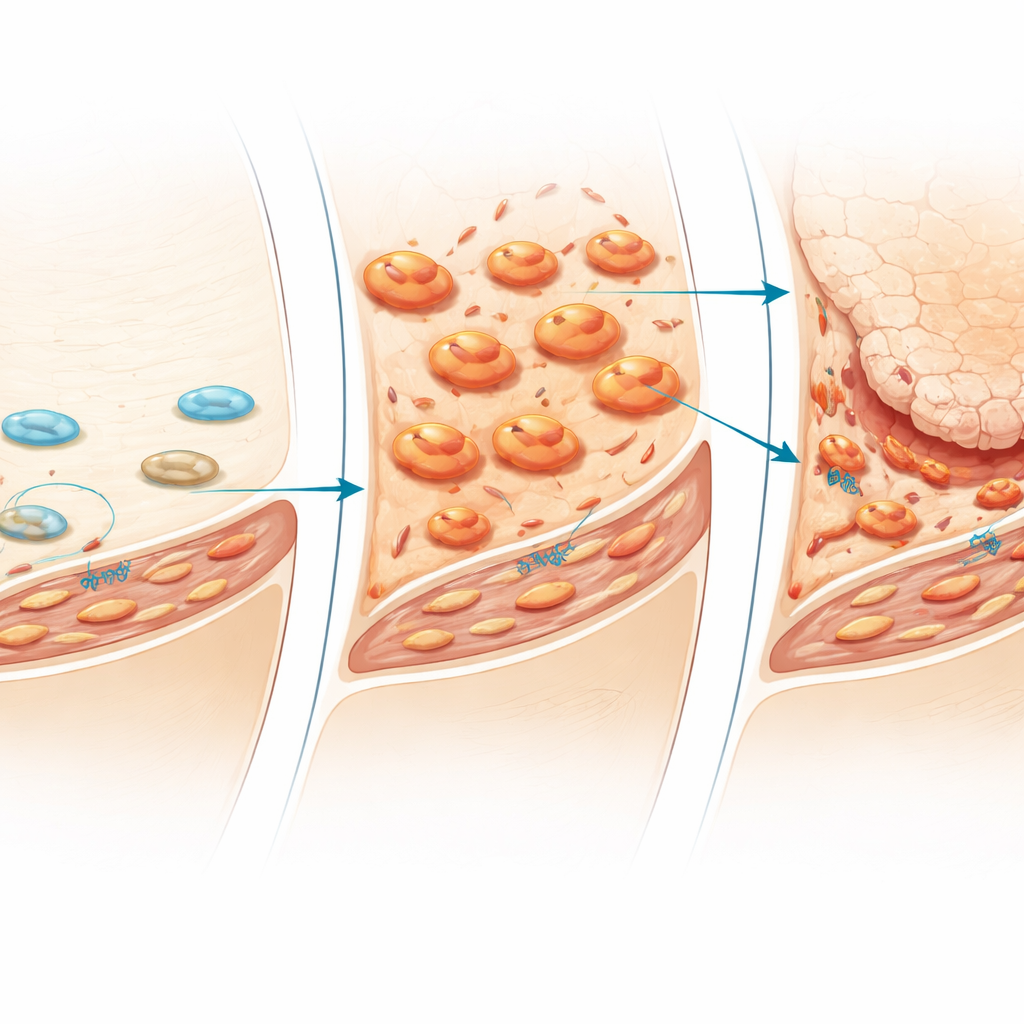
De vroege rol van immuuncellen
Timing bleek cruciaal. In weefselsecties genomen op verschillende stadia, steeg het aantal macrofagen eerst in de dunne synoviale voering al enkele dagen nadat mechanische stress was weggenomen, en verspreidden ze zich daarna dieper in het weefsel. Pas daarna begonnen fibroblasten te prolifereren en ontstond dik vezelig weefsel. Wanneer het team selectief synoviale macrofagen uitputte door liposomen te injecteren die deze cellen elimineren, veranderde de cascade sterk: ontsteking en fibrose in de gewrichtsvoering werden fors verminderd en de degeneratie van kraakbeen was duidelijk minder ernstig. Merkers van de myofibroblast-subset daalden ook. Deze bevindingen wijzen op macrofagen als vroege organisatoren van de schadelijke reactie op ontlasting, die fibroblasten activeren en het toetreden van latere kraakbeenschade voorbereiden.
Wat dit betekent voor het beschermen van gewrichten
Samengevat laat de studie zien dat gewrichten afhankelijk zijn van regelmatige beweging en geschikte mechanische belasting om synovium en kraakbeen in balans te houden. Wanneer die mechanische input verdwijnt, verschuiven gespecialiseerde immuun- en fibroblastcellen in het synovium naar een inflammatoir, fibrotisch stadium dat geleidelijk kraakbeen afbreekt. Belangrijk is dat het herstellen van beweging en draaglast dit proces kan terugdraaien, vooral als dat gebeurt voordat de schade vergevorderd is. Voor mensen die lange periodes van immobiliteit tegemoet zien — door gips, verlamming of langdurig bedlegerig zijn — benadrukken deze resultaten het belang van vroegtijdige, begeleide gewrichtsbeweging en veilige belasting, evenals de mogelijkheid van toekomstige geneesmiddelen die de macrofaag–fibroblast-as richten om blijvend gewrichtsletsel te voorkomen.
Bronvermelding: Ishikura, H., Okada, H., Kin, Y. et al. Loss of mechanical stress induces synovitis, fibrosis and articular cartilage degeneration via distinct synovial cell subsets. Sci Rep 16, 8007 (2026). https://doi.org/10.1038/s41598-026-39416-4
Trefwoorden: immobiliteit van het gewricht, synovitis, degeneratie van kraakbeen, mechanische belasting, macrofagen