Clear Sky Science · nl
Optimalisatie van THP-1-CAR-monocyten met gebruik van CD32a-signaleringsfagocytose voor antigeenspecifieke T-celactivering
Het immuunsysteem nieuwe vaardigheden leren
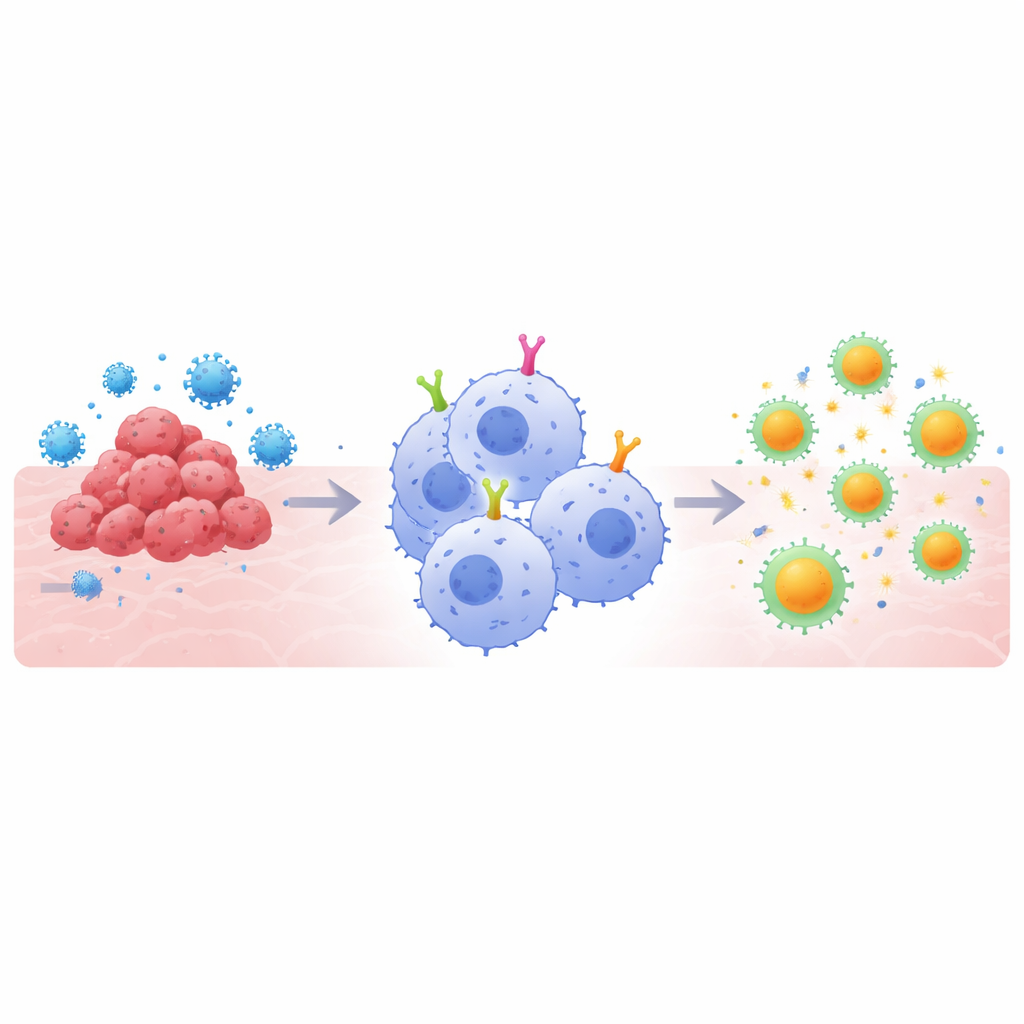
Moderne celtherapieën herprogrammeren immuuncellen om kanker op te sporen, maar de meeste vertrouwen op T-cellen, die het moeilijk kunnen hebben in de vijandige omgeving van solide tumoren. Deze studie richt zich in plaats daarvan op een andere krachtige verdediger—macrofagen, de professionele "eters" van het lichaam—en onderzoekt hoe je ze zodanig kunt herbedraden dat ze niet alleen schadelijke cellen of virussen efficiënter inslikken, maar ook T-cellen oproepen voor een duurzamere, gerichte aanval. Het werk onthult ontwerprichtlijnen voor het bouwen van betere chimere antigeenreceptor (CAR)-macrofagen die toepasbaar zouden kunnen zijn op zowel infecties zoals COVID-19 als moeilijk behandelbare solide tumoren.
Waarom super-eters ertoe doen
CAR-gebaseerde therapieën werken door immuuncellen uit te rusten met op maat gemaakte oppervlaktereceptoren die een gekozen doel herkennen, zoals een tumoreiwit of een virusspike. Versies met T-cellen hebben de behandeling van bepaalde bloedkankers getransformeerd, maar stuiten op obstakels bij solide tumoren en bij sommige infecties. Macrofagen bieden een andere invalshoek: zij nemen bedreigingen van nature op en hakken ze in stukjes die aan T-cellen kunnen worden gepresenteerd, waarmee de "aangeboren" en "verworven" afweer met elkaar worden verbonden. De meeste CAR-ontwerpen waren echter oorspronkelijk ontwikkeld voor T-cellen, niet voor macrofagen. De auteurs redeneerden dat, om de sterke punten van macrofagen ten volle te benutten, de interne signaalonderdelen van CARs—de segmenten die de cel vertellen wat te doen zodra een doel is gebonden—specifiek op deze etende cellen afgestemd moeten worden.
Het beste interne bedrading vinden
Het team vergeleek systematisch verschillende interne signaaldomeinen binnen CARs geïntroduceerd in een humane monocytencelijn (THP‑1) die tot macrofagen kan worden gedifferentieerd. Ze concentreerden zich op domeinen afkomstig van receptoren die normaal fagocytose en ontsteking aansturen: CD3ζ (de klassieke T-celmodule), CD32a (een receptor die aan antilichaam-gecoate doelwitten bindt), CR3-componenten CD11b en CD18 (belangrijke complementreceptoren), en TLR4 (een sensor voor microbiële dreiging). Met behulp van bolletjes en pseudovirussen bedekt met het SARS‑CoV‑2-spike-eiwit maten ze hoe goed elk CAR-ontwerp cellen in staat stelde doelen op te nemen, ontstekingsmoleculen te produceren en vervolgens menselijke CD8-T-cellen te activeren die eerder het virus hadden gezien. Ze zetten de meest veelbelovende ontwerpen daarna om in CARs gericht tegen mesothelin, een eiwit dat in veel solide tumoren overgeproduceerd wordt, om te zien of dezelfde regels ook in een kankersetting golden.
Betere eters en signaalversterkers bouwen
Er ontstond een duidelijk patroon: CARs gebaseerd op CD32a stimuleerden consequent sterkere en snellere fagocytose dan die met het conventionele CD3ζ-domein, ondanks dat CD3ζ meer van de gebruikelijke activatiemotieven bevatte. Met andere woorden, de "passing" tussen het signaal en de macrofaagmachinerie bleek belangrijker dan loutere signaalsterkte. Het toevoegen van CR3-afgeleide delen (CD11b of CD18) bovenop CD32a verhoogde in de meeste omstandigheden niet verder de eetcapaciteit, maar het verhoogde wel de niveaus van sleutelontstekingscytokinen zoals TNF‑α en IL‑1β. Combinaties met TLR4 gingen nog verder in het versterken van ontstekingssignalen en de oppervlaktemarker CD86, die geassocieerd is met T-celstimulerend vermogen, hoewel dit met afwegingen kwam: lagere CAR-niveaus op het celoppervlak en enigszins verminderde fagocytose.
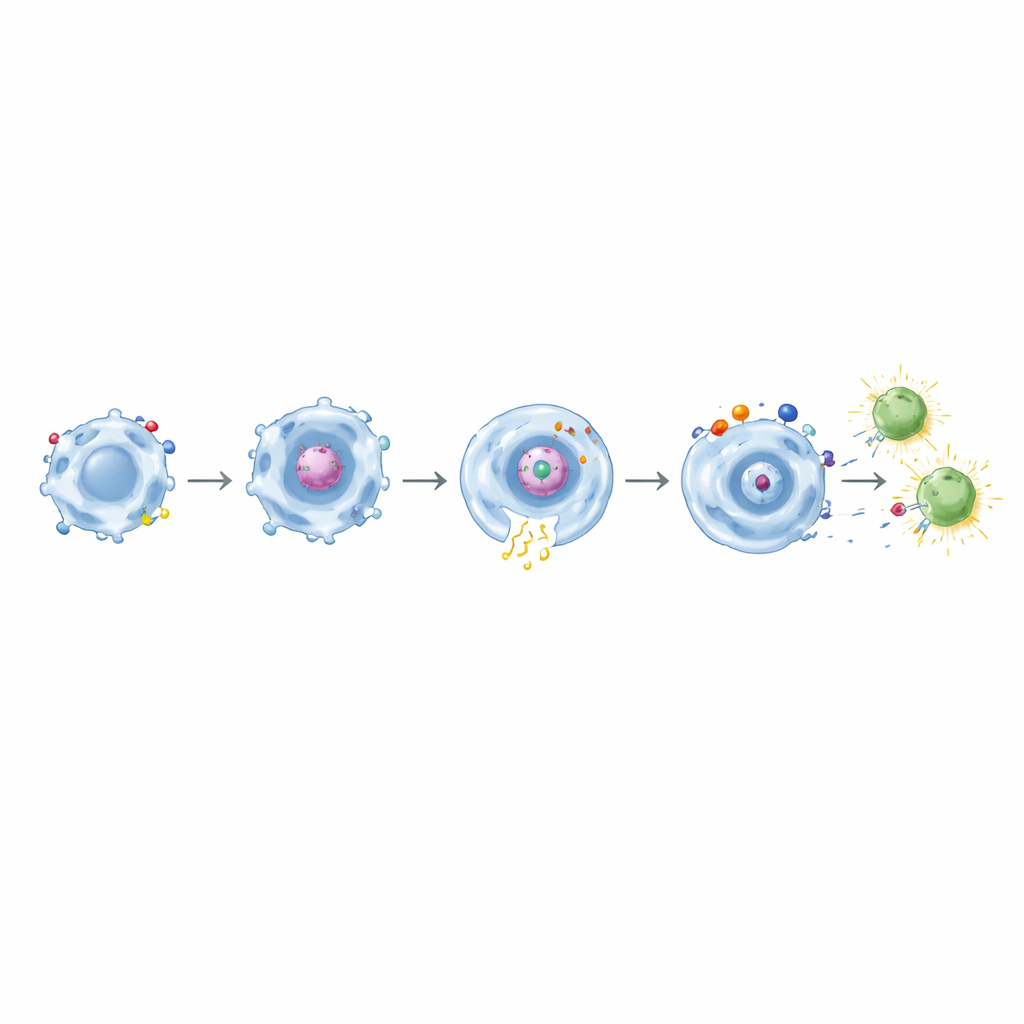
Van eten naar T-cellen onderwijzen
Cruciaal was dat, nadat macrofagen met CD32a-gebaseerde CARs het spike-eiwit hadden opgenomen, ze in staat waren geheugen CD8-T-cellen van eerder tegen COVID‑19 gevaccineerde personen te activeren. Deze T-cellen zetten vroege activeringsmarkers aan en produceerden effectormoleculen zoals interferon‑γ en TNF‑α. Het effect werd nog sterker met duale domein-CARs die CD32a combineerden met CD11b, CD18 of TLR4. Toen soortgelijke ontwerpen gericht tegen mesothelin werden getest tegen gemodificeerde tumorcellen, toonden ze opnieuw precieze, doelafhankelijke fagocytose gecombineerd met verhoogde ontstekingssignaleringsniveaus. Hiervan sprong de CD32a+TLR4-combinatie eruit als een krachtige "weefselalarm", die het meest effectief cytokinesecretie en CD86 versterkte terwijl hij toch specifieke tumoropname behield.
Wat dit kan betekenen voor toekomstige behandelingen
Voor een niet‑specialist laat deze studie zien dat het ingrijpen in macrofagen geen one‑size‑fits‑all‑probleem is. Door interne signaalmodules te verwisselen en te combineren, kunnen wetenschappers cellen vormgeven die ofwel focussen op efficiënte opruiming van zieke cellen, ofwel fungeren als immuunversterkers die de onderdrukkende tumoromgeving herstructureren en T-cellen rekruteren. CD32a-gebaseerde CARs kwamen naar voren als een sterke basis voor dergelijke ontwerpen, beter presterend dan traditionele T-celmodules in macrofagen en werkend zowel tegen virus- als tumorantigenen. Hoewel deze resultaten afkomstig zijn uit laboratoriummodellen en bevestigd moeten worden in primaire menselijke cellen en diermodellen, bieden ze een blauwdruk voor next‑generation CAR-macrofagetherapieën die beter solide tumoren en hardnekkige infecties zouden kunnen bestrijden door snelle opname te verenigen met precieze T‑celactivering.
Bronvermelding: Hong, J., Lee, S., Kim, Y. et al. Optimization of THP-1-CAR monocytes utilizing CD32a signaling phagocytosis for antigen-specific T cell activation. Sci Rep 16, 8175 (2026). https://doi.org/10.1038/s41598-026-39406-6
Trefwoorden: CAR-macrofagen, CD32a-signalisatie, fagocytose, immunotherapie voor solide tumoren, T-celactivering