Clear Sky Science · nl
Integratie van multi-omicsanalyse identificeert DNA-schade-gerelateerd gen CLSPN als biomarker bij maagkanker
Waarom dit onderzoek ertoe doet
Maagkanker blijft een van de dodelijkste vormen van kanker wereldwijd, grotendeels omdat de ziekte vaak laat wordt ontdekt en het ontbreekt aan betrouwbare vroege waarschuwingssignalen. Deze studie duikt diep in de genetische "krassen" die ontstaan door DNA-schade en identificeert een gen genaamd CLSPN als een veelbelovende marker die artsen mogelijk kan helpen maagkanker eerder te detecteren, de agressiviteit beter te begrijpen en behandelingen gerichter af te stemmen.
Op zoek naar gevaarsignalen in maagtumoren
De onderzoekers startten vanuit een eenvoudige gedachte: als DNA-schade bijdraagt aan maagkanker, dan kunnen genen die betrokken zijn bij het omgaan met die schade belangrijke aanwijzingen bevatten over wie ziek wordt en hoe de ziekte verloopt. Om dit te testen verzamelden zij meerdere grote datasets. Deze omvatten bulk-RNA-sequencing, die de gemiddelde genactiviteit in hele tumormonsters meet; single-cell RNA-sequencing, die duizenden individuele cellen één voor één onderzoekt; en ruimtelijke transcriptomica, die genactiviteit terugplaatst op het weefseldak. Ze stelden ook een uitgebreide lijst samen van genen die al eerder met DNA-schade in verband zijn gebracht. Met deze bronnen vroegen ze welke DNA-schade-gerelateerde genen het sterkst geassocieerd zijn met maagkanker en met het overleven van patiënten.
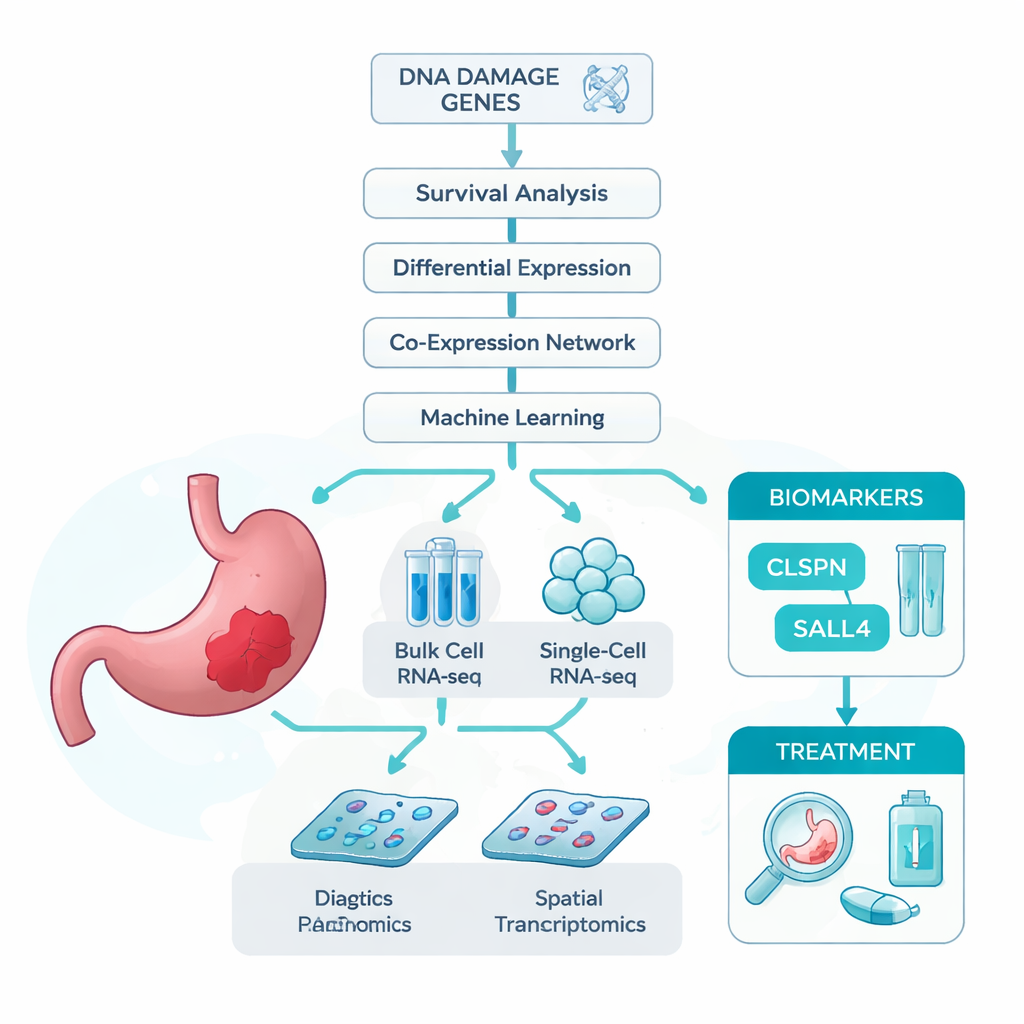
Met slimme algoritmes op zoek naar sleutelgenen
Aangezien duizenden genen veranderen bij kanker, gebruikte het team een reeks statistische en machine learning-tools om het veld te verkleinen. Eerst filtreerden ze genen die zowel ontregeld waren in tumoren als duidelijk gerelateerd aan de overleving van patiënten. Vervolgens groepeerden ze genen op basis van gezamenlijke expressie en kruisten dit met de DNA-schadelijst. Deze meerstapsfilter leverde 13 veelbelovende kandidaatgenen op. Om te bepalen welke van deze het meest onderscheidend waren tussen tumor en normaal weefsel, trainden ze zeven verschillende machine learning-modellen, elk met een rangschikking van genen naar classificatiewaarde. In alle modellen stegen twee genen—CLSPN en SALL4—consistente naar de top, met nauwkeurigheidsscores rond of boven 97% en ROC-gebieden boven 0,96, wat suggereert dat deze genen uitstekend diagnostisch potentieel hebben.
Inzoomen op CLSPN binnen de tumor
Van de twee leidende genen stak CLSPN er als meest informatief uit, waarna de auteurs het gedetailleerder onderzochten. In single-cell-gegevens van meer dan 30.000 cellen bleek CLSPN veel actiever in tumorcellen dan in nabijgelegen normale of ondersteunende cellen, wat wijst op een tumorspecifieke rol. Ruimtelijke mapping van patiëntweefsels toonde een vergelijkbaar patroon: CLSPN-expressie clustere in regio’s die pathologen als kankerlijk identificeerden. Toen het team tumorcellen splitste in groepen met "hoog CLSPN" en "laag CLSPN", vertoonde de hoge groep sterkere activiteit in routes gerelateerd aan DNA-replicatie, celdeling en herstel—processen die, wanneer te actief of foutief gereguleerd, onbeheerst groei kunnen aanwakkeren. Pseudotime-analyse, die reconstrueren probeert hoe cellen veranderen over een hypothetische tijdlijn, suggereerde dat CLSPN-niveaus doorgaans stijgen naarmate tumorcellen vorderen, wat erop wijst dat CLSPN-opregulatie mogelijk deel uitmaakt van de verschuiving naar een meer kwaadaardige toestand.
Verbindingen met het immuunsysteem en behandelingsrespons
De studie onderzocht ook hoe CLSPN zich verhoudt tot de tumoromgeving en tot mogelijke therapieën. Tumoren met hogere CLSPN-expressie vertoonden verschillende samenstellingen van immuuncellen, met name macrofagen en bepaalde T- en NK-cellen, wat suggereert dat CLSPN kan bijdragen aan het vormen van een immuunsuppressieve omgeving. Modellering van gevoeligheid voor geneesmiddelen gaf aan dat kankers met meer CLSPN mogelijk kwetsbaarder zijn voor verscheidene chemotherapieën en gerichte middelen, aangezien hogere CLSPN-niveaus geassocieerd waren met lagere voorspelde doses die nodig zijn om groei te remmen. Belangrijk is dat bij kleuring van echte weefselmonsters van 70 patiënten de CLSPN-eiwitniveaus duidelijk hoger waren in kanker dan in normaal maagweefsel en geassocieerd waren met grotere tumoren, diepere invasie, uitzaaiing naar lymfeklieren en kortere totale overleving.
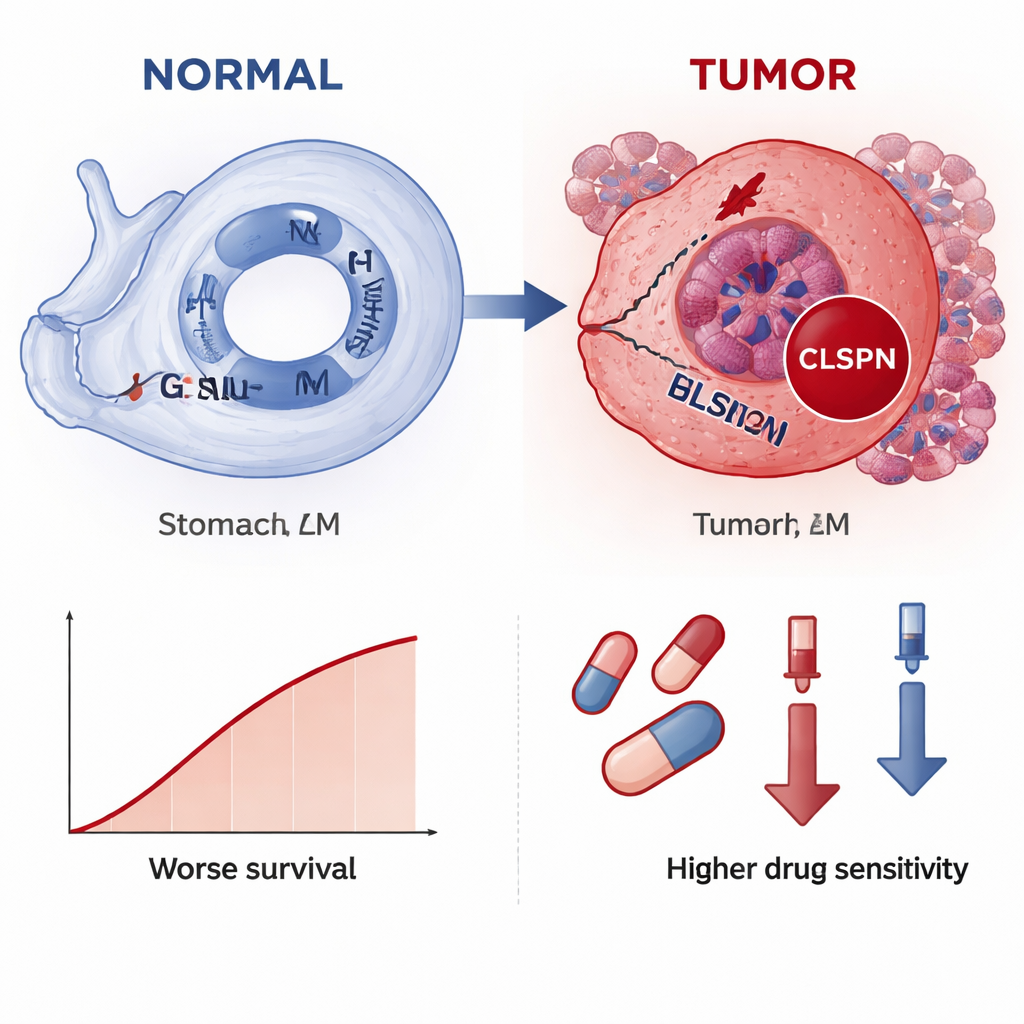
Wat dit voor patiënten kan betekenen
In gewone bewoordingen suggereert de studie dat CLSPN zich gedraagt als een rood waarschuwingslampje voor maagkanker: het schakelt voornamelijk aan in tumorcellen, brandt feller bij gevorderde ziekte en wijst op een hoger risico op een slechtere uitkomst. Omdat het zowel op RNA-niveau als met standaard ziekenhuis-kleuringstechnieken kan worden gedetecteerd, zou CLSPN een praktisch biomarker kunnen worden om pathologen te helpen maagkanker te bevestigen, patiënten naar risicogroepen in te delen en mogelijk behandelingskeuzes te sturen. Hoewel meer klinische testen nodig zijn voordat het routinematig kan worden toegepast, benadrukt dit werk hoe het lezen van de sporen van DNA-schade over meerdere datalagen nieuwe instrumenten kan onthullen voor vroegere diagnose en meer gepersonaliseerde behandeling van maagkanker.
Bronvermelding: Ma, Q., Yang, X., Sun, N. et al. Integrating multi-omics analysis identifies DNA damage-related gene CLSPN as a biomarker in gastric cancer. Sci Rep 16, 7789 (2026). https://doi.org/10.1038/s41598-026-39387-6
Trefwoorden: maagkanker, DNA-schade, CLSPN, biomarker, single-cell-analyse