Clear Sky Science · nl
Een nieuwe humane acute myeloïde leukemie-cellijn SDEY-AML1 met KMT2A:MLLT3- en IKZF1:EVX1-fusies vertoont hoge tumorigeniteit in NSG-muizen
Waarom dit onderzoek ertoe doet
Acute myeloïde leukemie (AML) bij kinderen en volwassenen kan nog steeds dodelijk zijn, vooral wanneer kankercellen bepaalde hoogrisico-genetische afwijkingen dragen en resistent zijn tegen standaardmedicatie. Deze studie introduceert een nieuwe laboratorium-leukemieceldijn, SDEY-AML1, gekweekt uit het beenmerg van een tienerjongen met bijzonder agressieve AML. Omdat deze cellen de belangrijkste kenmerken van zijn ziekte behouden, bieden ze wetenschappers een krachtig nieuw model om te begrijpen waarom sommige leukemieën zo moeilijk te behandelen zijn en om nieuwere, meer gerichte therapieën te testen.
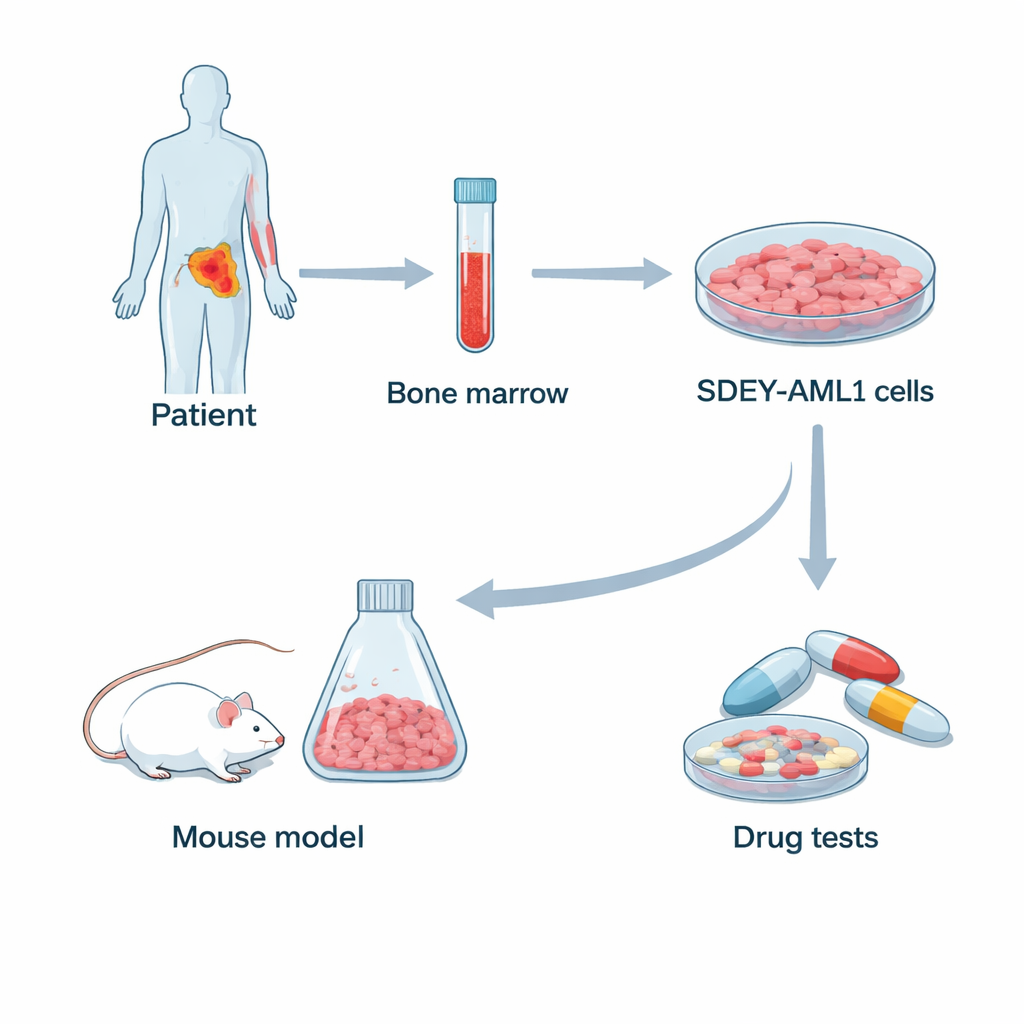
Van patiënt naar labmodel
De onderzoekers behandelden een 14-jarige jongen van wie de leukemie gepaard ging met extreem hoge witte bloedcelaantallen, gezwollen lymfeklieren en milt, en herhaalde koortsaanvallen. Ondanks meerdere rondes intensieve chemotherapie en nieuwere medicijncombinaties bereikte zijn ziekte nooit volledige remissie en hij overleed aan complicaties van de kanker. Tijdens zijn behandeling verzamelden artsen beenmerg en isoleerden ze leukemiecellen. In het laboratorium verzorgden ze deze cellen in voedingsrijke vloeistof en bouwden ze geleidelijk de toegevoegde groeifactoren af. Na ongeveer drie maanden begonnen de cellen zelfstandig gestaag te groeien en konden ze meer dan een jaar in stand worden gehouden, wat aantoonde dat er een stabiele, zelfvernieuwende cellijn was ontstaan.
Hoe de nieuwe cellen zich gedragen
Onder de microscoop vertonen SDEY-AML1-cellen de kenmerken van monocytische leukemie: onregelmatige maar herkenbare celvormen, gevouwen kernen met zichtbare nucleoli (de „kernen binnen de kern” van de cel) en een grijsblauwe buitenlaag bezaaid met kleine korreltjes. Chemische kleuringen bevestigden dat de cellen bij dit leukemiesubtype horen en geen signalen vertoonden die typisch zijn voor andere bloedceltypen. Met flowcytometrie — een techniek die celoppervlaktekenmerken labelt met fluorescerende antilichamen — ontdekte het team dat SDEY-AML1-cellen dezelfde myeloïde markers dragen als de oorspronkelijke leukemiecellen van de jongen, wat aangeeft dat de laboratoriumlijn trouw de ziekte in zijn lichaam weerspiegelt.
Verborgen genetische boosdoeners
Moderne sequencing-methoden onthulden waarom deze leukemie zo agressief was. De SDEY-AML1-cellen bevatten twee grote genfusies, waarbij delen van verschillende genen abnormaal aan elkaar zijn gekoppeld: KMT2A::MLLT3 en een nieuw beschreven fusie IKZF1::EVX1. Beide betreffen genen die bekendstaan om hun rol in de ontwikkeling van bloedcellen en worden vaak geassocieerd met slecht-scorende bloedkankers. Daarbovenop dragen de cellen twee schadelijke mutaties in TP53 — de bekende „bewaker van het genoom” tumor suppressor — en een truncerende mutatie in ETV6, een ander gen dat belangrijk is voor bloedvorming. Gezamenlijk hebben deze complexe veranderingen waarschijnlijk de snelle ziekteprogressie en therapieresistentie aangedreven, en maken zij SDEY-AML1 nu tot een zeldzaam instrument om te bestuderen hoe zulke combinaties van defecten op elkaar inwerken.
Testen van groei, verspreiding en geneesmiddelrespons
Het team toonde aan dat SDEY-AML1-cellen talrijke kolonies kunnen vormen in zacht agar, een klassieke test voor kwaadaardige groei. Om te zien hoe ze zich in een levend organisme gedragen, programmeerden de wetenschappers de cellen om luciferase te produceren, een lichtuitstralend eiwit, en injecteerden ze deze in sterk immuundeficiënte NSG-muizen. Binnen 40–50 dagen ontwikkelden de meeste muizen gezwollen buiken vol bloedgetinte vloeistof en duidelijke tekenen van tumorinvasie, en werden leukemiecellen in hun beenmerg gedetecteerd. Dit bevestigde dat SDEY-AML1 in vivo sterk tumorneigend is, waardoor het geschikt is voor preklinische testen. De onderzoekers hebben de cellen ook blootgesteld aan een reeks chemotherapie- en gerichte middelen en vonden dat verschillende geneesmiddelen, waaronder histon-modificerende middelen en kinase-remmers, de levensvatbaarheid van de cellen verminderden, wat vroege aanwijzingen biedt over combinaties die patiënten met vergelijkbare genetische profielen mogelijk zouden kunnen helpen.
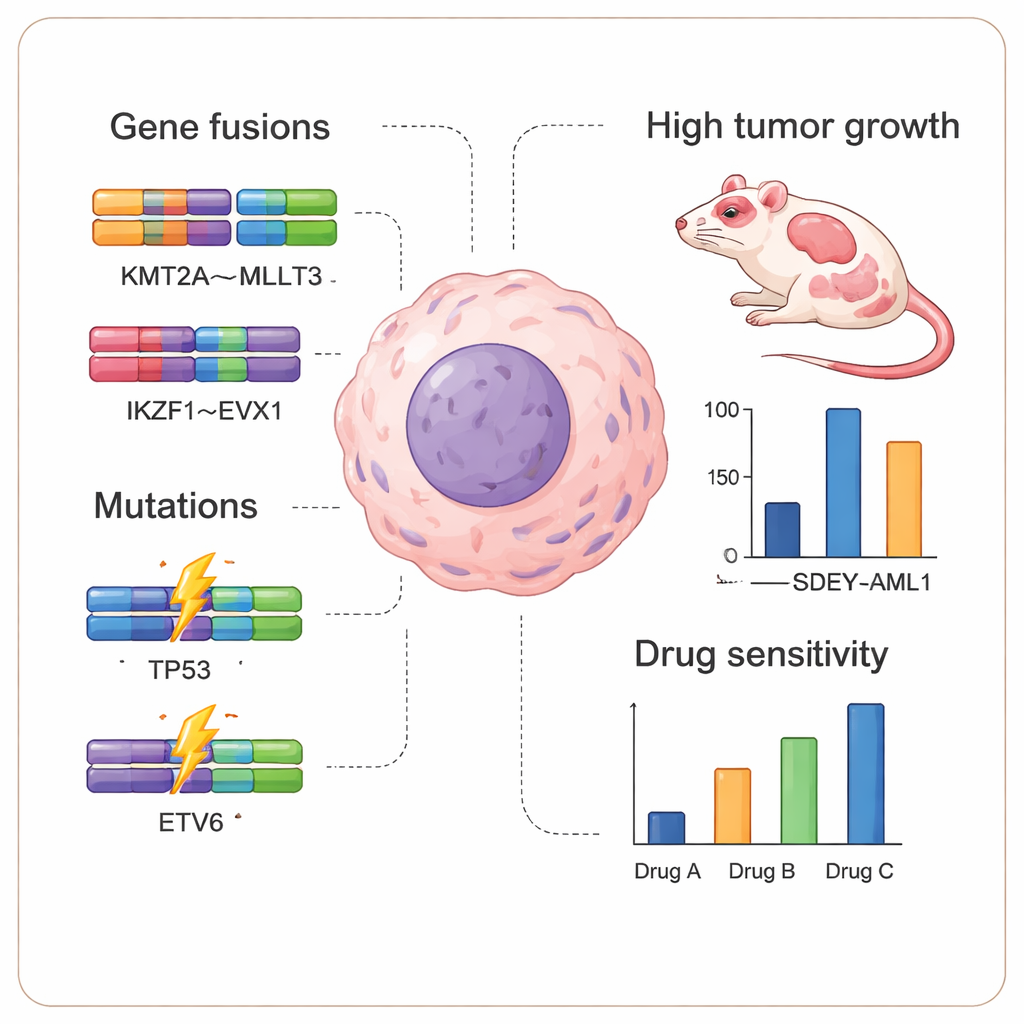
Wat dit betekent voor toekomstige behandelingen
Voor een niet‑specialist kan SDEY-AML1 worden gezien als een gedetailleerde „plaatsvervanger” voor een bijzonder gevaarlijk type leukemie — een die wordt aangedreven door meerdere gebroken instructies in het DNA van de cel. Omdat de lijn goed in schaaltjes groeit en snel ziekte veroorzaakt in muizen, biedt ze een reproduceerbare manier om te onderzoeken waarom deze mutaties standaardbehandelingen doen falen en om snel nieuwe geneesmiddelen of combinaties te screenen voordat die patiënten bereiken. Op lange termijn zouden inzichten die met deze cellijn zijn verkregen, kunnen leiden tot meer gepersonaliseerde behandelstrategieën voor mensen van wie de leukemie vergelijkbare genetische handtekeningen draagt, en zo mogelijk de momenteel moeilijkst te behandelen gevallen beter hanteerbaar maken.
Bronvermelding: Yang, C., Zhang, W., Wu, Y. et al. A novel human acute myeloid leukemia cell line SDEY-AML1 with KMT2A: MLLT3, IKZF1: EVX1 fusions exhibits high tumorigenicity in NSG mice. Sci Rep 16, 7792 (2026). https://doi.org/10.1038/s41598-026-39353-2
Trefwoorden: acute myeloïde leukemie, leukemie cellijn, genfusie, middelenresistentie, precisie-oncologie