Clear Sky Science · nl
FAM120A - een eiwit ingebed in het ALS-ziektenetwerk
Waarom dit belangrijk is voor mensen en gezinnen
Amyotrofische laterale sclerose (ALS) is een verwoestende ziekte die mensen langzaam verlamt door het doden van de zenuwcellen die beweging aansturen. Vandaag de dag begrijpen we nog steeds niet volledig waarom deze motorische neuronen afsterven, en effectieve behandelingen blijven schaars. Deze studie werpt licht op een weinig bekend eiwit, FAM120A genoemd, en suggereert dat het zenuwcellen kan helpen omgaan met stress en het voorkomen van de ophoping van schadelijke eiwitklonten — een kenmerk van ALS. Door bloot te leggen hoe dit eiwit zich tijdens de ziekte gedraagt, opent het werk een nieuw pad naar begrip en mogelijk uiteindelijk naar behandeling van ALS.
Een verborgen speler vinden in een druk genennetwerk
De onderzoekers begonnen niet aan de laboratoriumbank maar achter de computer. Ze gebruikten een “convergerende analyse” om vele bestaande datasets over met ALS geassocieerde genen en hun interacties te combineren. Dit netwerkperspectief maakte het mogelijk clusters van eiwitten te zien die samenwerken in sleutelprocessen in de cel, vooral die betrokken bij RNA-verwerking en eiwitkwaliteitscontrole — beide bekende knelpunten bij ALS. Binnen een van die clusters kwam FAM120A naar voren als een eerder over het hoofd gezien maar sterk verbonden eiwit dat interacteert met meerdere gevestigde ALS-gerelateerde eiwitten. De bekende rollen in het helpen van cellen te overleven bij oxidatieve stress en in het beheer van RNA maakten het tot een sterke kandidaat voor nadere studie.
Een kwetsbaar eiwit volgen tijdens ziekteprogressie
Om te testen of FAM120A daadwerkelijk van belang is bij ALS, schakelde het team over op een veelgebruikt muismodel met een gemuteerde versie van het SOD1-gen, een van de eerste geïdentificeerde genetische oorzaken van ALS. Ze maten zowel de RNA-boodschappers als de eiwitniveaus van de muisversie, Fam120A, in het ruggenmerg in de loop van de tijd, van voor het optreden van symptomen tot ver in de ziekte. Vroeg daalden de RNA-niveaus van Fam120A in het ruggenmerg voordat de dieren duidelijke ziekteverschijnselen vertoonden. Later, toen verlamming zich ontwikkelde, daalde het Fam120A-eiwit zelf sterk. Deze mismatch — eerst verandering in RNA, later pas in eiwit — suggereert dat meerdere lagen van regulatie uit elkaar vallen naarmate de ziekte vordert.
Waar in het ruggenmerg dit eiwit voorkomt
Vervolgens vroegen de wetenschappers waar precies Fam120A in het ruggenmerg te vinden is. Met fluorescerende microscopie op weefselsneden zagen ze dat Fam120A voornamelijk aanwezig is in neuronen in de ventrale hoorn — het gebied rijk aan motorneuronen dat bij ALS aantast wordt. In laatstadium zieke dieren vonden ze enige signalen in ondersteunende cellen genaamd astrocyten, maar het dominante patroon bleef neuronale expressie. Deze waarnemingen verbinden Fam120A direct met de cellen die falen bij ALS en ondersteunen het idee dat verlies ervan hun vermogen om cellulair stress aan te kunnen kan verzwakken, mogelijk bijdragen aan verlies van motorische functie.
Extra FAM120A inzetten in zenuwachtige cellen
Het team ging daarna naar gekweekte zenuwachtige cellen om te onderzoeken wat FAM120A daadwerkelijk doet. Ze manipuleerden deze cellen zodat ze ofwel normale ofwel gemuteerde SOD1 produceerden, die de neiging heeft toxische aggregaten te vormen, en dwongen de cellen vervolgens om extra menselijk FAM120A te maken. Wanneer de gemuteerde SOD1 aanwezig was, verminderde het verhogen van FAM120A zowel de hoeveelheid onoplosbare SOD1 die biochemisch werd gedetecteerd als het aantal zichtbare aggregaten onder de microscoop aanzienlijk. Belangrijk is dat FAM120A weinig effect had op de normale vorm van SOD1, wat erop wijst dat het specifiek cellen kan helpen met verkeerd gevouwen of aggregatiegevoelige eiwitten om te gaan — een centraal probleem in ALS en andere neurodegeneratieve ziekten.
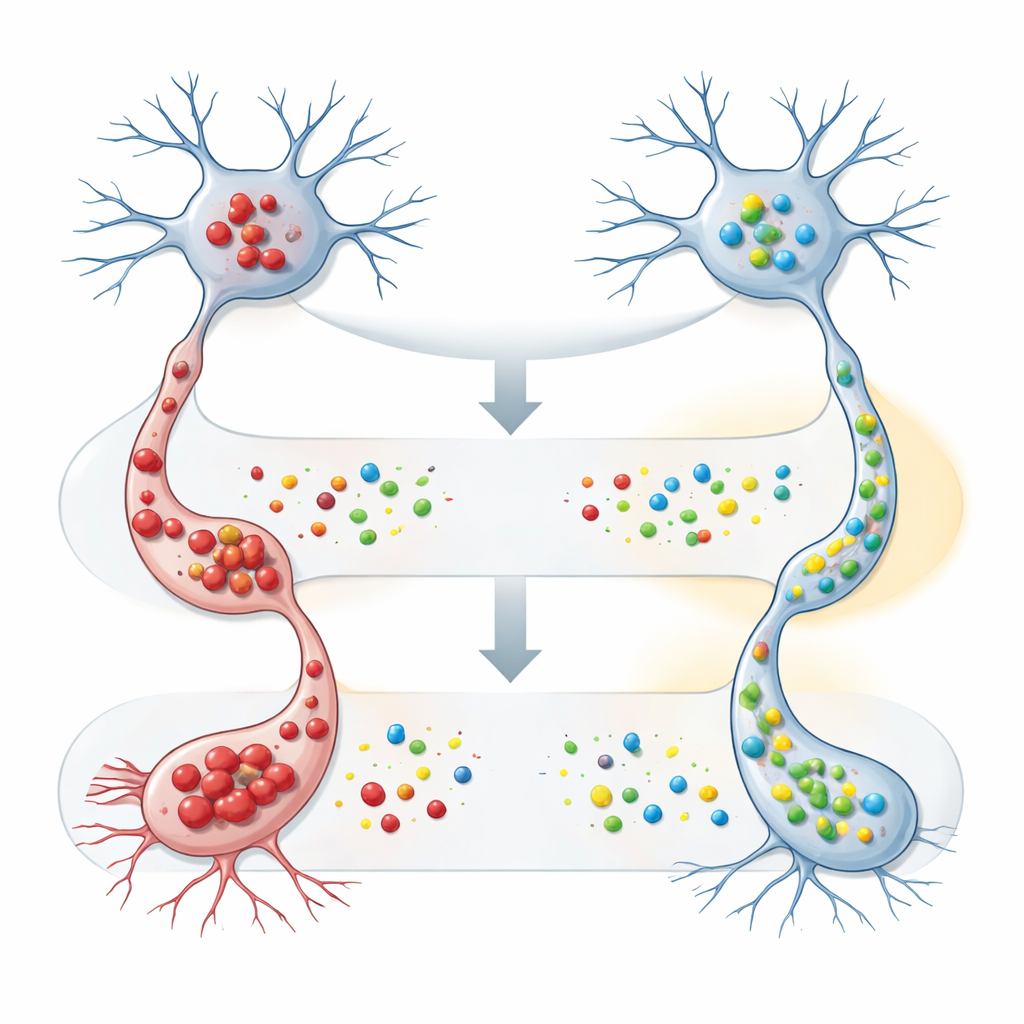
Een bredere kaart bouwen van moleculaire bondgenoten en vijanden
Buiten deze experimenten onderzochten de onderzoekers het bredere interactienetwerk van FAM120A. Ze bevestigden dat het fysiek geassocieerd is met PURA, een RNA-bindend eiwit dat al in verband wordt gebracht met hersenontwikkeling en neurodegeneratie, en vonden dat PURA-niveaus ook dalen in het ALS-muugrgen, zij het later in de ziekte. Ze belichten aanvullende banden tussen FAM120A, het antisense partnergen FAM120Aos, en een ander RNA-bindend eiwit, ELAVL1, dat ontstekings- en stressresponsgenen in de hersenen reguleert. Dit groeiende web van verbindingen plaatst FAM120A op het kruispunt van RNA-regulatie, stressresponsen en eiwitkwaliteitscontrole — precies de systemen die tekortschieten bij ALS.
Wat dit kan betekenen voor toekomstige ALS-behandelingen
Samengevat suggereren de bevindingen dat FAM120A niet slechts een toeschouwer is maar een betekenisvol onderdeel van het ALS-ziektenetwerk. Het vroege verlies in kwetsbare motorneuronen, de fysieke verbindingen met andere RNA-regulerende eiwitten en het vermogen om toxische SOD1-klonten in cellen te verminderen wijzen allemaal op een beschermende rol bij het behouden van eiwitbalans. Hoewel er nog veel werk te doen is — met name om te onderzoeken of vergelijkbare veranderingen optreden bij mensen met ALS en in andere ziektmodellen — valt FAM120A nu op als een veelbelovend doelwit voor vervolgonderzoek en mogelijk voor therapieën gericht op het behoud van de gezondheid van motorneuronen.
Bronvermelding: Vicencio, E., Gomez, L., Beltran, S. et al. FAM120A - a protein inserted in the ALS disease network. Sci Rep 16, 8200 (2026). https://doi.org/10.1038/s41598-026-39329-2
Trefwoorden: amyotrofische laterale sclerose, motorische neuronen, eiwitaggregatie, RNA-bindende eiwitten, neurodegeneratie