Clear Sky Science · nl
Microbiologische en reologische dynamiek van gemengde biofilms gevormd door bacteriën en eukaryote virussen
Verborgen gemeenschappen op medische apparaten
Veel ziekenhuisinfecties beginnen niet met één enkele kiem, maar met plakkerige, onzichtbare gemeenschappen die biofilms worden genoemd en die katheters en andere medische apparaten bedekken. Deze studie behandelt een vaak over het hoofd geziene vraag met grote implicaties voor de patiëntveiligheid: wat gebeurt er wanneer niet alleen bacteriën, maar ook virussen die mensen kunnen infecteren, samen in deze biofilms terechtkomen? Door te volgen hoe een veelvoorkomend zoogdiervirus zich gedraagt binnen bacteriële biofilms, laten de onderzoekers zien hoe deze kleverige microbiële steden virusdeeltjes stilletjes kunnen herbergen en hun gedrag kunnen veranderen.
Klevende steden van microben
Biofilms zijn als microscopische steden die microben bouwen op vochtige oppervlakken—leidingen, stenen, tanden of kunststof buisjes die bij patiënten worden geplaatst. Bacteriën vestigen zich, vermenigvuldigen zich en scheiden een lijmachtig matrix uit die hen beschermt tegen uitdroging, chemicaliën en het immuunsysteem. In ziekenhuizen vormen zulke biofilms zich vaak op urine- en intraveneuze katheters, waar ze bloedbaaninfecties en urineweginfecties kunnen veroorzaken die moeilijk te behandelen zijn. Deze biofilms bevatten meestal veel verschillende soorten en zelfs verschillende rijken van het leven, maar het merendeel van het onderzoek heeft zich op bacteriën alleen geconcentreerd, waardoor de rol van virussen grotendeels onontgonnen is gebleven.
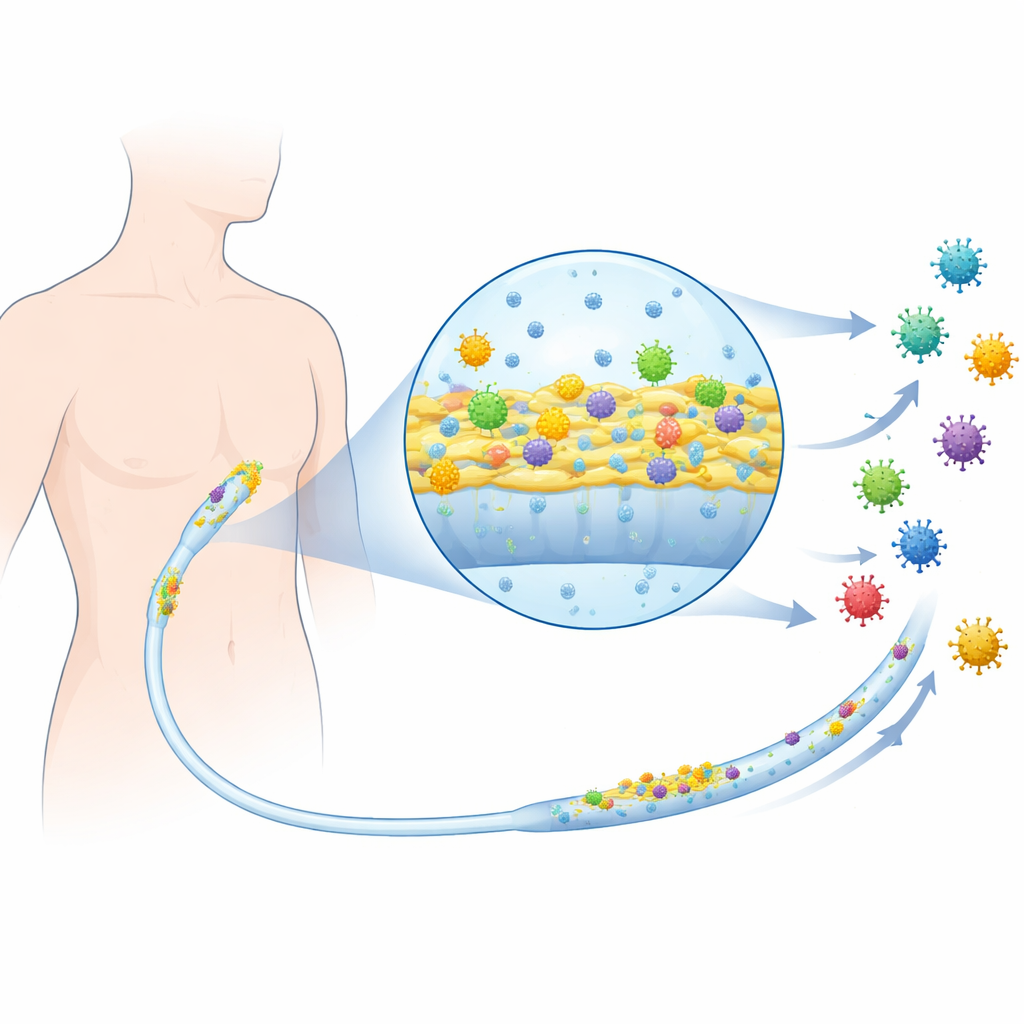
Een zoogdiervirus in de mix brengen
Het team werkte met klinische bacteriestammen die bekendstaan om kolonisatie van katheters, waaronder uropathogene Escherichia coli uit urineweginfecties en andere bacteriën die vaak worden aangetroffen bij centrale lijninfecties. Vervolgens introduceerden ze zoogdierreovirus, een goed bestudeerd, niet-ingekapseld virus dat dierlijke cellen infecteert, als proxy voor menselijk-pathogene virussen in het algemeen. Eerst controleerden ze of het toevoegen van virusbevattend materiaal de normale, vrij zwevende bacteriegroei beïnvloedde. Over veel stammen heen groeiden en overleefden de bacteriën even goed met of zonder het virus, wat aantoont dat het virus de bacteriën niet direct doodde of als een antibioticum fungeerde.
Biofilms veranderen de textuur, niet de omvang
Wanneer bacteriën zich in biofilms vestigen, werd het verhaal genuanceerder. Voor de meeste stammen veranderde de totale hoeveelheid biofilm—gemeten met een standaardkleuring die kwantificeert hoeveel materiaal een oppervlak bedekt—nauwelijks in aanwezigheid van het virus. Een paar stammen produceerden echter iets meer of minder biofilm afhankelijk van of er viruspreparaten aanwezig waren, wat wijst op stam-specifieke effecten. Om verder te gaan dan eenvoudige hoeveelheid leenden de onderzoekers instrumenten uit de materiaalkunde en maten ze hoe “zacht” of “stevig” elk biofilm was, vergelijkbaar met het onderzoeken van de textuur van een gel. Ze vonden dat elke bacteriestam zijn eigen mechanische signatuur vormde. Belangrijk is dat het toevoegen van virus deze biofilms óf kon verharden óf verzachten, afhankelijk van de stam: bij één E. coli-stam maakte het virus de matrix star, terwijl bij een Staphylococcus epidermidis-stam het virus leidde tot een zwakkere, meer toegeeflijke structuur.
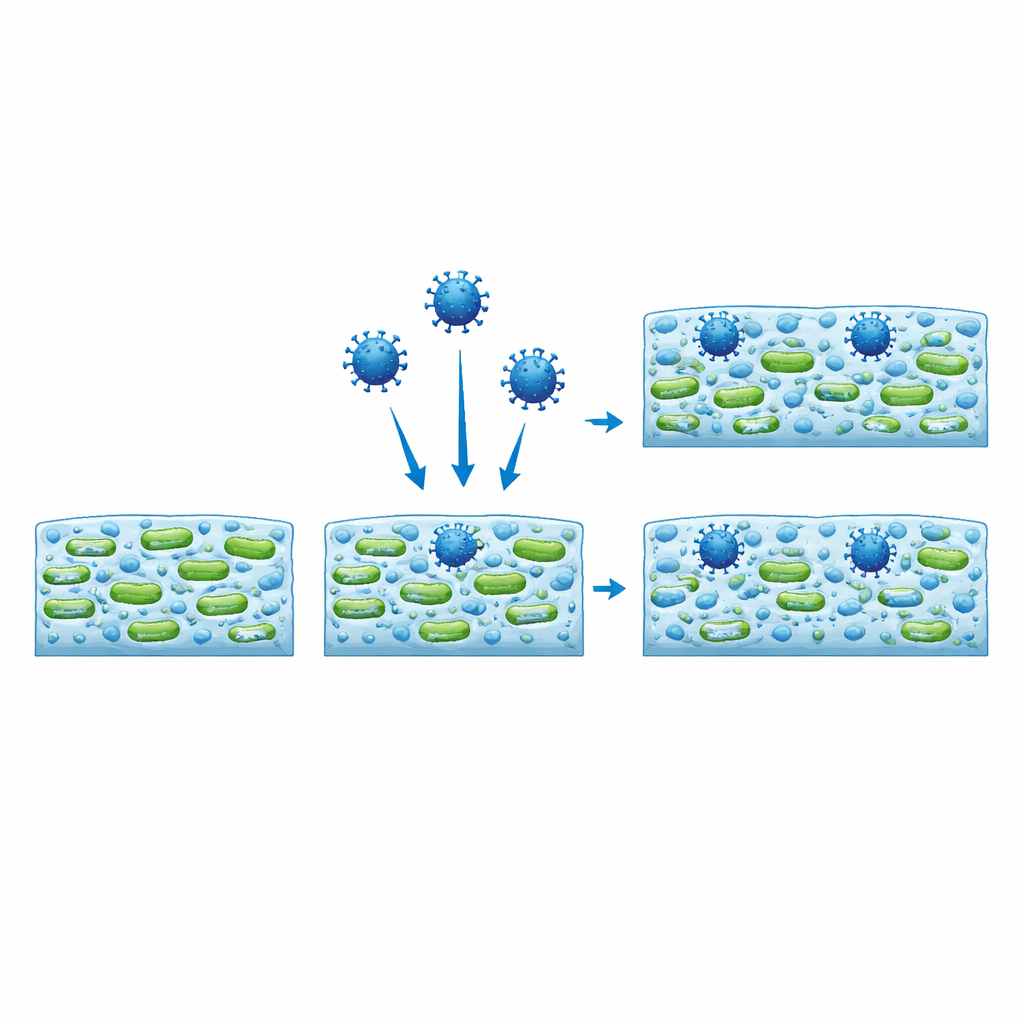
Virussen vinden schuilplaats en blijven infectieus
Met fluorescentiemicroscopie labelden de wetenschappers virale deeltjes zodat ze gingen gloeien en volgden waar ze terechtkwamen binnen het biofilm. In tegenstelling tot inert, even groot plastic grit, dat grotendeels in sparsere gebieden bleef en werd weggespoeld, drongen de virussen diep in de matrix door en clusteren ze doorgaans waar bacteriële cellen het dichtst zaten. In sommige gevallen veranderde de aanwezigheid van virus zelfs de algehele vorm van het biofilm, waarbij compacte klonten in meer webachtige netwerken veranderden of omgekeerd, opnieuw afhankelijk van de bacteriële stam. Om te testen of deze ingesloten virussen nog steeds gevaarlijk waren, isoleerden de auteurs ze uit de biofilms en brachten ze in contact met zoogdiercellen. De teruggewonnen virussen bleven infectieus, ondanks dat ze gedurende twee dagen in de bacteriële slijmlaag ingebed waren geweest.
Waarom dit belangrijk is voor patiënten en daarbuiten
Voor een leek is de kernboodschap dat biofilms op medische apparaten niet alleen bacteriën tegen behandeling kunnen beschermen—ze kunnen ook virussen verbergen en behouden die menselijke of dierlijke cellen infecteren. De studie toont aan dat virussen zich in de bacteriële matrix kunnen nestelen, de structuur van het biofilm subtiel kunnen veranderen en toch volledig in staat blijven nieuwe cellen te infecteren zodra ze vrijkomen. Dit suggereert dat katheters en andere met biofilm bedekte oppervlakken als stille reservoirs kunnen dienen waar virussen persistent blijven, afgeschermd tegen uitdrogen, ontsmettingsmiddelen en immuunaanvallen. Het begrijpen van deze gemengde microbiële gemeenschappen kan cruciaal zijn voor het ontwerpen van betere materialen, reinigingsstrategieën en therapieën die zowel bacteriële als virale partners aanpakken om hardnekkige, apparaatgeassocieerde infecties te verminderen.
Bronvermelding: Gao, J., Abriat, C., Laekas-Hameder, M. et al. Microbiological and rheological dynamics of mixed biofilms formed by bacteria and eukaryotic virus. Sci Rep 16, 8315 (2026). https://doi.org/10.1038/s41598-026-39314-9
Trefwoorden: biofilms, katheterinfecties, virus–bacterie-interacties, reovirus, microbiële gemeenschappen