Clear Sky Science · nl
Een polymeerfysisch model van de interfasecelkern voor radiobiologische simulaties
Waarom de vorm van ons DNA-thuis ertoe doet
Radiatie is een tweesnijdend zwaard in de geneeskunde: het kan kankercellen doden, maar ook gezond weefsel beschadigen. In het hart van zowel risico’s als voordelen ligt ons DNA, dicht opeengepakt in de celkern. Dit artikel toont hoe een gedetailleerd, door de natuurkunde geïnspireerd 3D-model van die nucleaire “DNA-stad” wetenschappers kan helpen voorspellen hoe straling chromosomen breekt en foutief herstelt, wat mogelijk de behandeling van kanker en schattingen van ruimteradiatierisico’s kan verbeteren.
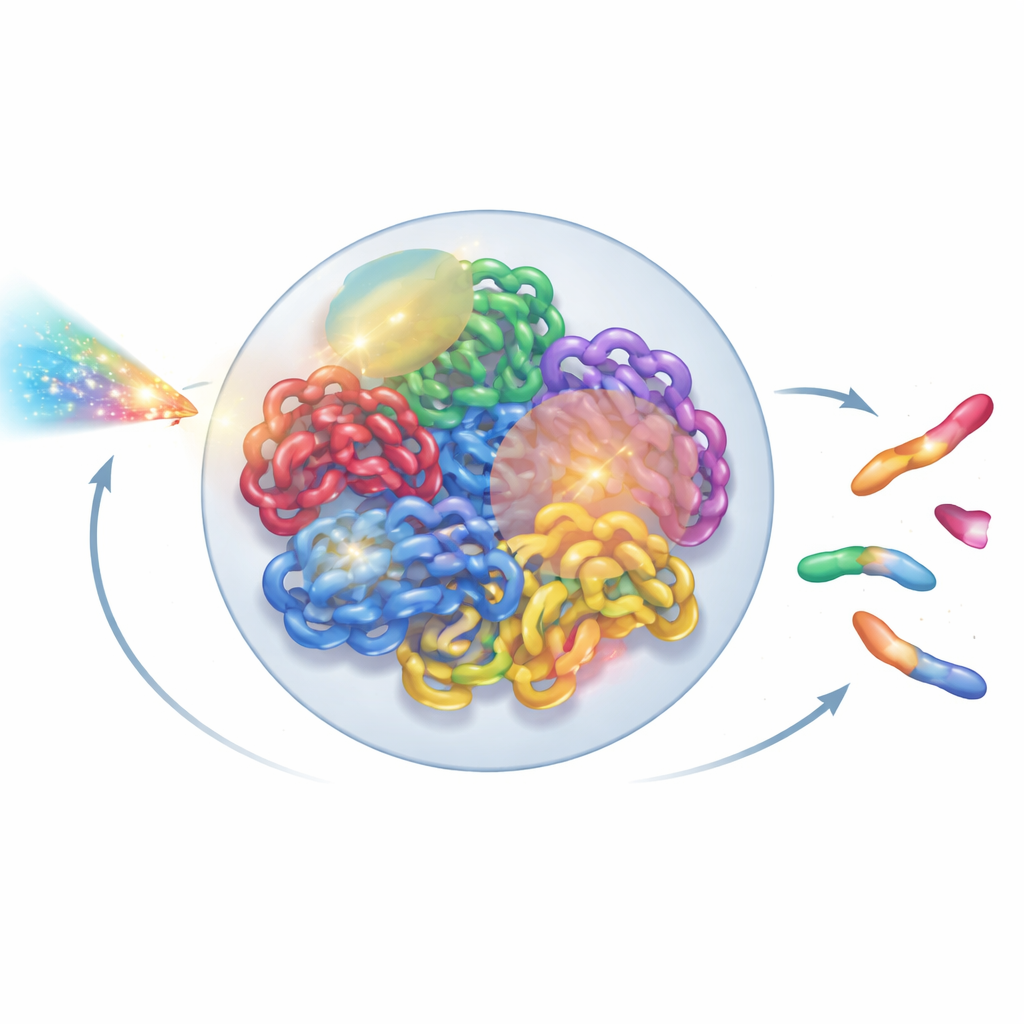
Het genoom zien als een levende structuur
In elke menselijke cel zijn twee meter DNA opgevouwen in een piepkleine kern van slechts enkele micrometers. Die vouwing is niet willekeurig: elk chromosoom neigt zijn eigen territorium te bezetten, dat verder is verdeeld in buurten en lusvormige domeinen. Nieuwe experimentele instrumenten, zoals superresolutiemicroscopie en Hi-C-contactkaarten, hebben deze ingewikkelde 3D-indeling in opmerkelijk detail blootgelegd. Toch behandelen de meeste stralingsmodellen DNA nog steeds als een vereenvoudigde warboel van lijnen of geïdealiseerde lussen, waarbij deze hogere-orde organisatie wordt genegeerd. De auteurs stelden zich ten doel een heel-kernmodel te bouwen dat respecteert wat biologen hebben geleerd over echte chromatinearchitectuur, terwijl het toch snel genoeg blijft om op gewone labcomputers te draaien.
Een virtuele kern bouwen met polymeerfysica
Het team modelleerde chromosomen als flexibele ketens en ontleende ideeën aan de polymeerfysica, hetzelfde vakgebied dat wordt gebruikt om kunststoffen en zachte materialen te begrijpen. Ze verdeelden het probleem in drie relaxatiestadia om de enorme rekenkosten te beteugelen. Eerst plaatsten ze grote bouwstenen genaamd chromatinedomeinen door de hele kern, lieten ze elkaar afstoten, zich langs hun lengten uitrekken en clusteren tot bredere subcompartimenten. Vervolgens zoomden ze binnen elk domein in om de fijnere chromatinedraden uit te leggen, inclusief geluste regio’s die door bindende eiwitten bij elkaar worden gehouden. Ten slotte lieten ze alle vezels weer vrij met elkaar interageren binnen de kernbegrenzing om een realistische eindconfiguratie te benaderen. Door het proces op deze manier te splitsen en hiërarchische zoek- en parallelle rekentrucs toe te voegen, verkortten ze de uitvoeringstijd van onpraktische vier maanden tot ongeveer drie uur per virtuele kern op een 64-core werkstation.
Van stralingssporen naar DNA-breuken en reparaties
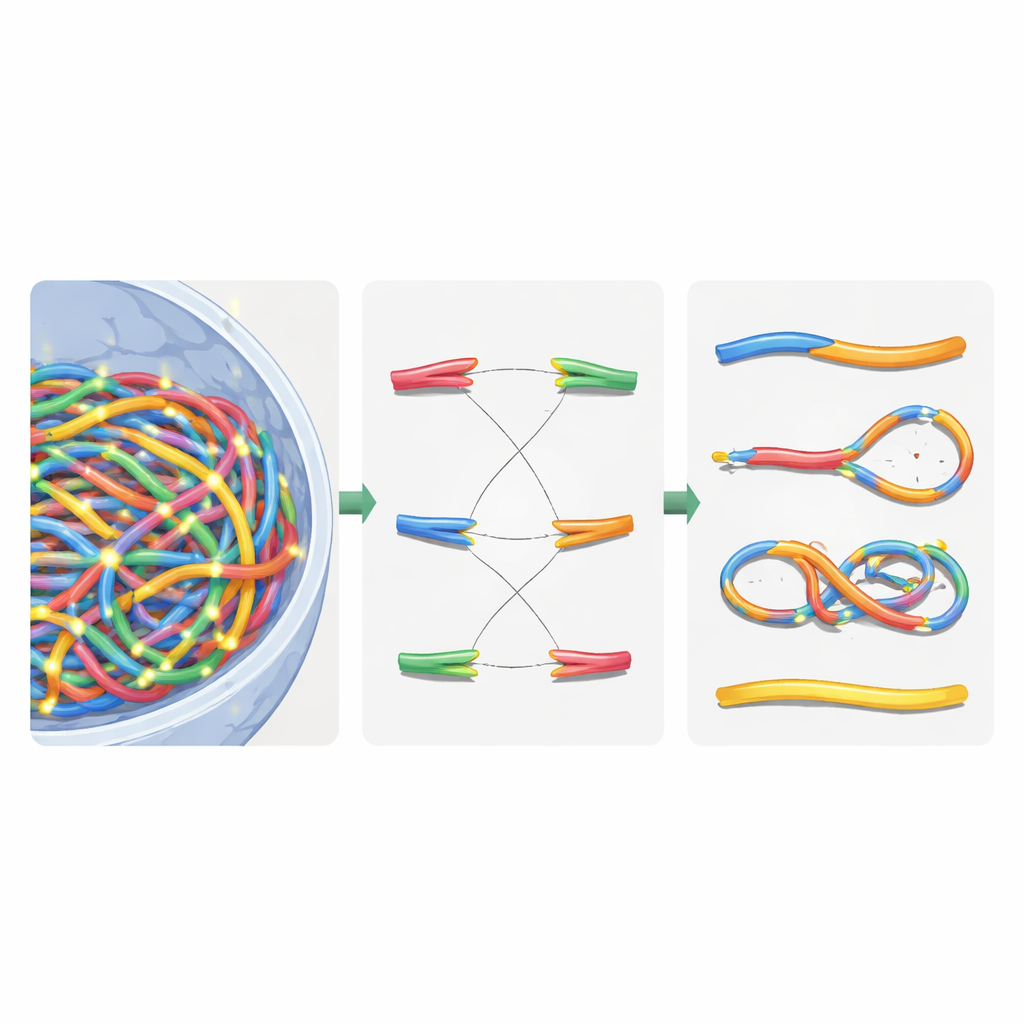
Zodra de virtuele kern was opgebouwd, legden de auteurs gedetailleerde stralingssporen over die waren gegenereerd met Geant4-DNA-simulaties. Ze gebruikten een hiërarchische zoekmethode om voor elk ionisatiegebeuren te vinden welk chromatinedomein, welk vezelsegment en uiteindelijk welke nucleotide het dichtstbij lag, zonder ooit alle tien miljard nucleotideposities in het geheugen op te slaan. In plaats daarvan behielden ze een herbruikbare chromatinesjabloon en pasten ze handige coördinatentransformaties toe op het moment zelf. Ionisaties in de DNA-ruggengraat werden behandeld als strengbreuken, en nabije breuken op tegenoverliggende strengen werden dubbele strengbreuken. Om het repareermechanisme van de cel na te bootsen, introduceerden de auteurs een op afstand gebaseerde herbindingsregel: vrije DNA-einden die dicht bij elkaar liggen, hebben een grotere kans om weer samen te komen. Herbindingsbeslissingen werden stap voor stap genomen totdat alle uiteinden ofwel gepaard waren of onverholpen bleven, waarbij zowel correcte reparaties als foutief samengestelde fragmenten werden nagebootst.
Gebroken chromosomen sorteren met netwerktopologie
Na deze virtuele reparatie bevatte de kern een mix van opnieuw samengestelde chromosomen en achtergebleven stukken. Om te classificeren wat er was gebeurd, zetten de auteurs het herstelde genoom om in een niet-gerichte graaf: chromosoomsegmenten werden randen, en hun uiteinden en breekpunten werden knopen. Met een standaard algoritme voor verbonden componenten konden ze automatisch elk nieuw chromosoomachtig object terugvinden en belangrijke kenmerken tellen zoals het aantal centromeren (aangedhechtingspunten voor celdeling) en telomeren (natuurlijke uiteinden). Hieruit identificeerden ze dicentrische chromosomen (chromosomen met twee centromeren), ringen en deleties. Vervolgens vergeleken ze hun simulaties met klassieke experimenten in menselijke huidcellen blootgesteld aan gamma- en alfadeeltjes, en vonden dat het totaal aantal chromosoomafwijkingen binnen ongeveer 20% van de gemeten waarden werd gereproduceerd, een substantiële verbetering ten opzichte van eerdere modellen.
Wat dit betekent voor patiënten en astronauten
In eenvoudige bewoordingen laat dit werk zien dat waar DNA zich in de kern bevindt en hoe het is gevouwen sterk beïnvloedt hoe stralingsschade optelt tot gevaarlijke chromosoomveranderingen. Door realistische 3D-genoomarchitectuur, efficiënte natuurkundig gebaseerde simulatie en graafgebaseerde interpretatie van gebroken chromosomen te combineren, bieden de auteurs een krachtige brug tussen structurele biologie en radiobiologie. Ze stellen dat toekomstige verfijningen — zoals het toevoegen van gedetailleerde timing van reparatie en het gebruik van volledige-genoomvolgordata — deze aanpak nog beter kunnen maken in het voorspellen van de biologische impact van hoogenergetische deeltjes die worden gebruikt in kankertherapie of die worden aangetroffen in diepe ruimte. Uiteindelijk kunnen betere modellen van het DNA-thuis in onze cellen helpen om veiligere, effectievere bestralingstherapieën op maat te maken en ons begrip van langetermijnrisico’s van straling te verscherpen.
Bronvermelding: Zhao, M., Huang, G., Xu, Z. et al. A polymer physics model of the interphase cell nucleus for radiobiological simulations. Sci Rep 16, 7913 (2026). https://doi.org/10.1038/s41598-026-39234-8
Trefwoorden: radiatie-geïnduceerde DNA-schade, chromatine 3D-architectuur, chromosoomafwijkingen, polymeerfysische modellering, deeltjestherapie