Clear Sky Science · nl
Voortgang van mitochondriale functie in perifere bloedmononucleaire cellen tijdens de vroege fase van sepsis bij patiënten op de intensivecare
Waarom de energiefabriekjes in onze cellen ertoe doen bij dodelijke infecties
Sepsis, een levensbedreigende reactie op een infectie, doet jaarlijks honderdduizenden mensen naar intensivecareafdelingen (ICU’s) gaan en veroorzaakt wereldwijd miljoenen doden. Artsen weten dat veel organen falen tijdens sepsis, maar de verborgen rol van kleine “energiecentrales” in onze immuuncellen — de mitochondriën — is lastiger vast te stellen. In deze studie werden ICU-patiënten met sepsis in hun eerste week op de intensivecare gevolgd om te zien hoe de energieproductie van belangrijke bloedimmuuncellen in de loop van de tijd veranderde en of die veranderingen samenhingen met overleving.
In het bloed kijken tijdens sepsis
De onderzoekers richtten zich op perifere bloedmononucleaire cellen, een belangrijke groep witte bloedcellen die ontsteking aansturen en ziekteverwekkers bestrijden. Omdat deze cellen door het hele lichaam circuleren en gemakkelijk te bemonsteren zijn, vormen ze een nuttig venster op hoe het immuunsysteem het volhoudt. Het team vergeleek 40 volwassenen met sepsis of septische shock op een Nederlandse ICU met 30 zorgvuldig afgestemde ziekenhuiscontroles van vergelijkbare leeftijd en geslacht zonder sepsis en verder metabolisch gezond. Van sepsispatiënten werd bloed drie keer afgenomen — binnen twee dagen na opname op de ICU en opnieuw rond dag drie tot vier en dag vijf tot zes — terwijl controles één keer werden bemonsterd. Uit elk staal isoleerden de onderzoekers immuuncellen, plaatsten die in een gestandaardiseerde voedingsoplossing en maten hoe snel hun mitochondriën zuurstof verbruikten onder verschillende condities, een directe aflezing van hoe hard de energiefabriekjes van de cellen werkten. 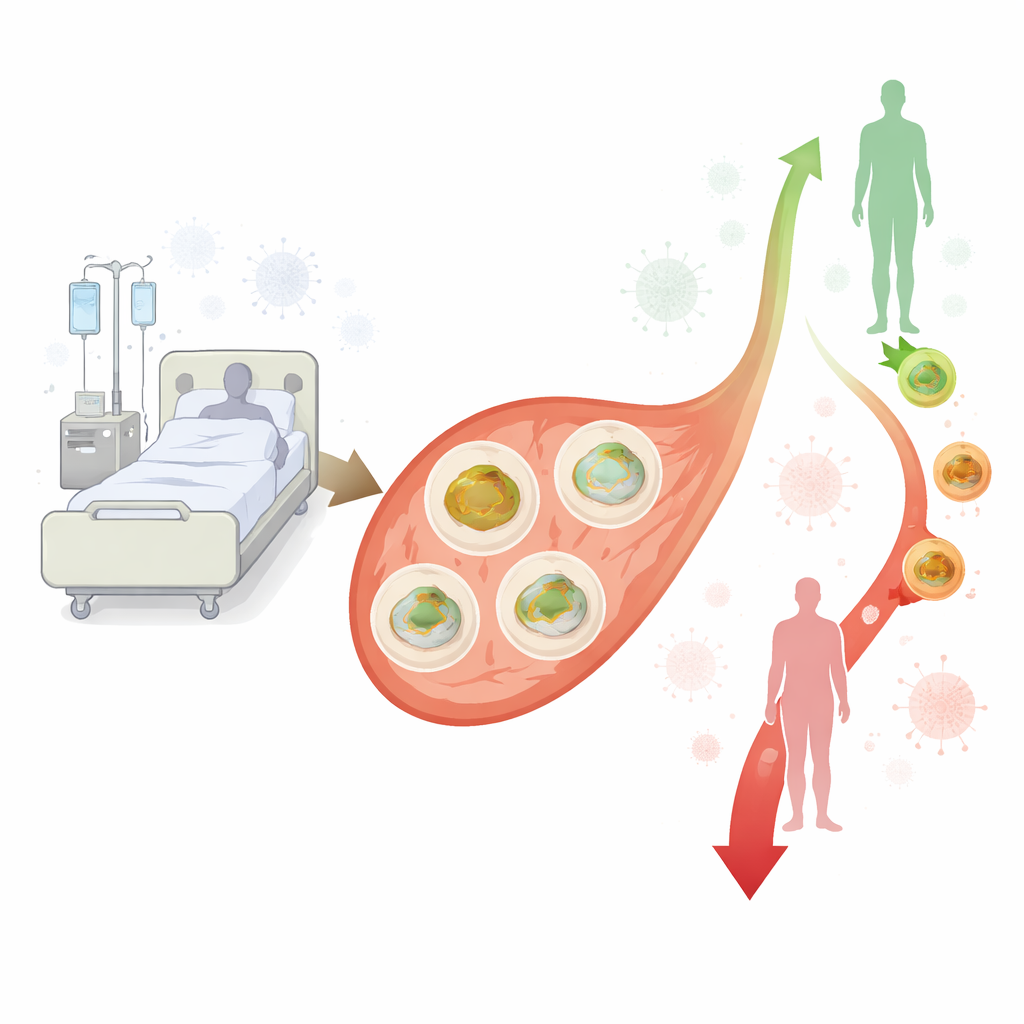
Immuuncelmotoren op volle toeren
Tegenover de veronderstelling dat sepsis simpelweg de cellulaire energieproductie “uitschakelt”, vond het team dat de mitochondriale activiteit in immuuncellen consequent hoger was bij sepsispatiënten dan bij controles. Over alle tijdstippen heen was de basale respiratie (het basale zuurstofgebruik in rust) verhoogd. Componenten die samenhangen met nuttige energieproductie — ATP-gekoppelde respiratie — evenals de maximale ademhalingscapaciteit van de mitochondriën neigden ook hoger te zijn, met name later in de eerste week. Zelfs protonlekkage, een vorm van “verloren” ademhaling waarbij brandstof wordt verbrand zonder energie te produceren, was toegenomen. Samen suggereren deze bevindingen dat, althans in circulerende immuuncellen, de energiemachines op toeren draaien in plaats van stil te vallen tijdens vroege sepsis, mogelijk als weerspiegeling van de intensieve vraag van een geactiveerde immuunrespons.
Genexpressie die past bij de hogere activiteit
Om te onderzoeken of deze hogere ademhalingssnelheid moleculair werd ondersteund, bekeken de onderzoekers de activiteit van meerdere genen die cruciale onderdelen van de mitochondriale machinere in coderen. In een subset van 10 sepsispatiënten en 10 afgestemde controles maten ze de genexpressie van onderdelen van de oxidatieve fosforyleringscomplexen — de eiwitassemblages die brandstof omzetten in ATP. Twee genen in het bijzonder, SDHB (onderdeel van complex II) en ATP5F1A (onderdeel van complex V, de ATP-synthase), waren significant actiever bij sepsispatiënten op meerdere tijdstippen, met toenames van ruwweg 40–50% ten opzichte van controles. Deze moleculaire “opschakeling” van de kernmachinerie sluit goed aan bij de functionele gegevens en versterkt het idee dat mitochondriën van immuuncellen tijdens sepsis harder worden gezet om te werken in plaats van volledig te bezwijken. 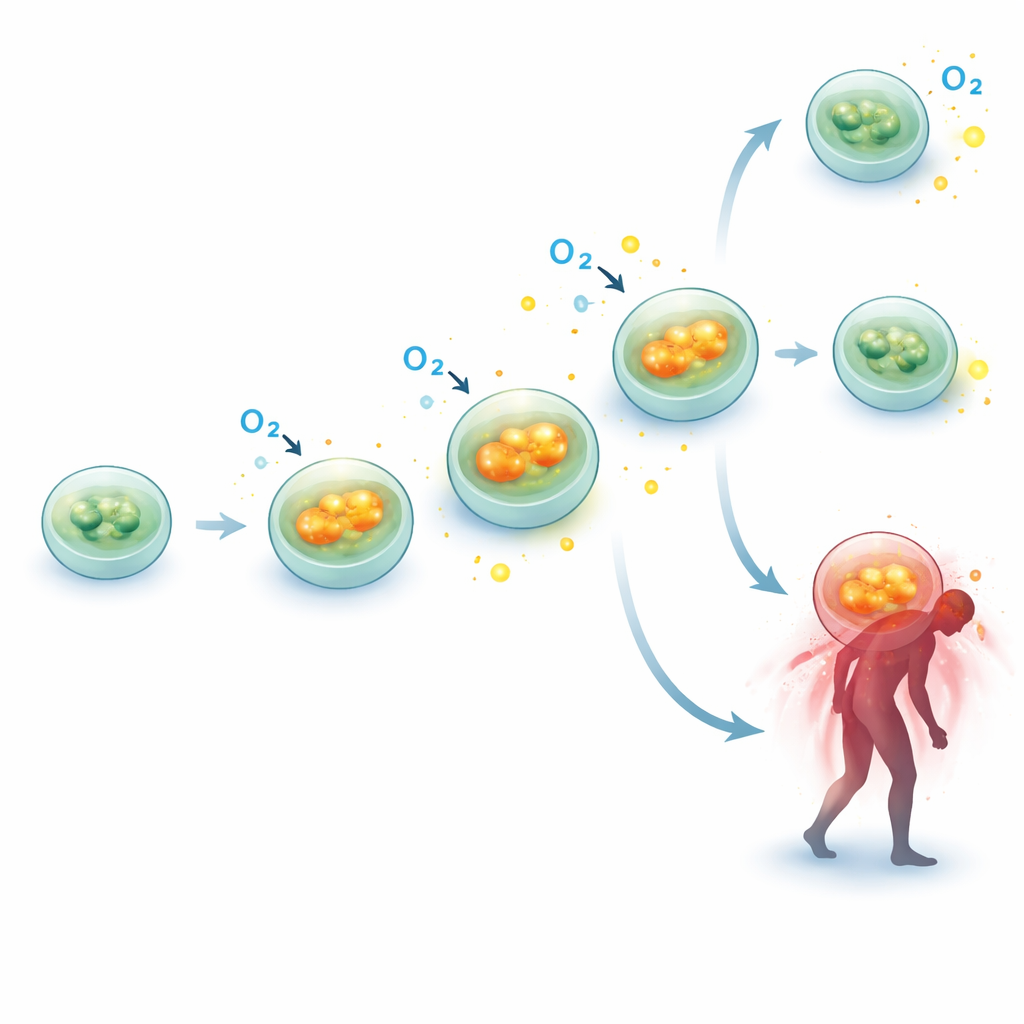
Energieveranderingen gekoppeld aan overleving
De meest aangrijpende bevinding was hoe deze mitochondriale veranderingen samenhingen met de uitkomst. Toen het team overlevenden vergeleek met niet-overlevenden over drie maanden, zagen ze geen grote verschillen in mitochondriale functie bij de allereerste meting. De richting van de verandering tijdens de eerste week vertelde echter een ander verhaal. Bij overlevenden neigde de mitochondriale respiratie in immuuncellen licht naar beneden of bleef stabiel. Bij patiënten die later overleden, stegen diezelfde maten — basale, ATP-gekoppelde en maximale respiratie en de reservecapaciteit — verder naarmate de week vorderde. Statistische analyse suggereerde dat een sterkere toename van de basale respiratie tussen de eerste en laatste meting geassocieerd was met een hoger risico binnen drie maanden te overlijden, zelfs na correctie voor ziektegerelateerde scores. Omdat het aantal sterfgevallen beperkt was, benadrukken de auteurs dat deze koppeling verkennend is en bevestiging behoeft, maar het suggereert dat een aanhoudend escalerende metabole aandrijving in immuuncellen een waarschuwingssignaal kan zijn.
Wat dit betekent voor patiënten met sepsis
Voor niet‑specialisten is de kernboodschap dat in vroege sepsis de energiefabriekjes in circulerende immuuncellen niet simpelweg uitvallen; in plaats daarvan lijken ze in overdrive te schakelen. Deze extra inspanning kan helpen de vroege strijd tegen infectie te ondersteunen, maar bij sommige patiënten blijft die activiteit stijgen in plaats van te stabiliseren, en die aanhoudende overactiviteit in bloedimmuuncellen ging samen met een slechtere overleving. De studie toont nog niet of deze mitochondriale opschudding behulpzaam, schadelijk of beide is in verschillende stadia, maar benadrukt dat sepsis net zozeer een ziekte van de energiebalans van het lichaam is als van infectie en ontsteking. In de toekomst zou het zorgvuldig volgen en mogelijk subtiel bijsturen van dit cellulaire energiegebruik deel kunnen worden van hoe artsen risico inschatten en behandelingen afstemmen voor mensen die met sepsis op de ICU vechten.
Bronvermelding: Moonen, H.P.F.X., Slingerland-Boot, R., de Jong, J.C.B.C. et al. Progression of peripheral blood mononuclear cell mitochondrial function during the early phase of sepsis in intensive care unit patients. Sci Rep 16, 8828 (2026). https://doi.org/10.1038/s41598-026-39202-2
Trefwoorden: sepsis, mitochondriën, immuuncellen, kritieke ziekte, cellulaire stofwisseling