Clear Sky Science · nl
Toegenomen atherosclerose en expressie van inflammarafts in macrofaag-schuimcellen bij AIBP-deficiënte muizen.
Waarom verstopte slagaders meer zijn dan alleen extra vet
Atherosclerose — het geleidelijke dichtslibben en verharden van onze slagaders — is een belangrijke oorzaak van hartaanvallen en beroertes. We denken er vaak simpelweg aan als vetophoping in bloedvaten, maar het verhaal is complexer: immuuncellen in de vaatwand kunnen de situatie kalmeren of de vlammen van ontsteking aanwakkeren. Deze studie onderzoekt waarom deze cellen onder bepaalde omstandigheden omslaan van vetopslagende “opruimteams” naar gevaarlijke aanstichters die plaques naar een dodelijker stadium duwen.
Immuuncellen die vet hamsteren
Binnen zich ontwikkelende arteriële plaques neemt een type witte bloedcel, de macrofaag, grote hoeveelheden cholesterol op en verandert in een zogenoemde schuimcel — een opgezwollen cel vol oliedruppels. Eerder werk in muizen suggereerde dat deze schuimcellen, ondanks hun ongezonde uiterlijk, verrassend stil zijn qua ontstekingsactiviteit, terwijl slankere macrofagen in de buurt juist meer ontstekingssignalen produceren. Het nieuwe onderzoek vraagt wat er gebeurt als het lichaam een eiwit mist dat AIBP heet, dat normaal helpt cholesterol van celoppervlakken te verwijderen en bepaalde membraan-‘brandpuntjes’ in bedwang te houden.
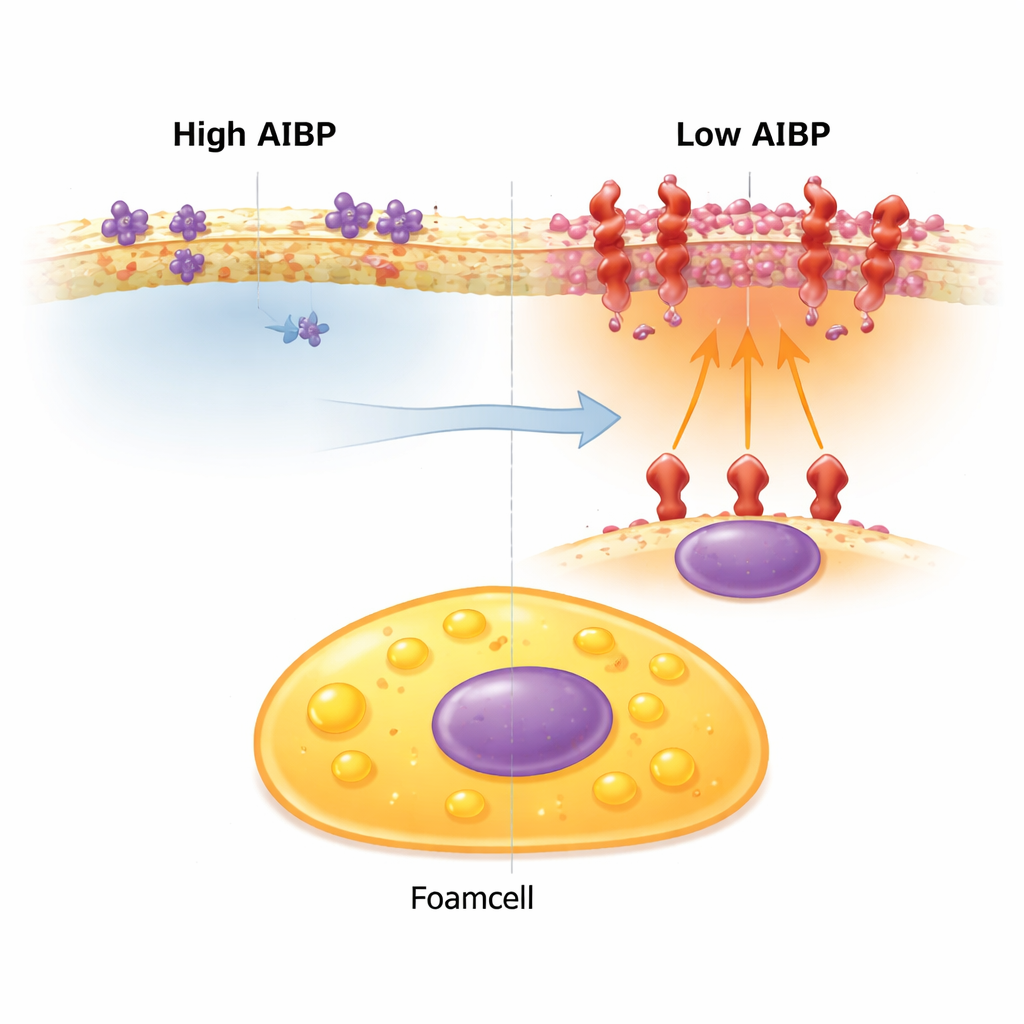
Membraan-brandpuntjes die alarmsignalen versterken
Het celoppervlak is niet uniform. Cholesterol en bepaalde vetten clusteren in kleine platforms waar receptoren die gevaar waarnemen dicht bij elkaar kunnen zitten. Wanneer deze platforms groeien en ontstekingsreceptoren samenpakken, noemen de auteurs ze “inflammarafts.” Eén van die receptoren, TLR4, helpt cellen bedreigingen te detecteren maar kan chronische ontsteking aanwakkeren bij overactivatie. Bij normale muizen die gevoelig zijn voor een hoog cholesterolgehalte dragen niet-schuimige macrofagen doorgaans meer van deze inflammarafts, terwijl schuimcellen er relatief weinig van hebben — een verklaring waarom schuimcellen eerder als minder ontstekingsbevorderend werden gezien.
Wanneer vetgeladen cellen verhit raken
Het team vergeleek muizen die zowel AIBP als een belangrijke receptor voor cholesterolverwijdering misten (waardoor ze sterk vatbaar zijn voor vaatziekte) met controlemuizen die alleen de receptor misten. Na 16 weken op een vetrijk dieet hadden de AIBP-deficiënte muizen plaques met meer schuimcellen, elk gevuld met meer neutrale vetten. Cruciaal was dat deze schuimcellen nu hoge niveaus van TLR4-paren en cholesterolrijke membraanpatches toonden — de kenmerken van inflammarafts — waardoor zij de belangrijkste ontstekingscel in de plaque werden in plaats van de rustigere, opslaggerichte cellen die eerder werden gezien. In kweektoestanden schakelden macrofagen van AIBP-deficiënte muizen die tot schuimcellen waren gemaakt met geoxideerd cholesterol genen aan die gelinkt zijn aan ontsteking, weefselafbraak en vasculair remodelleren, en vertoonden ze meer oxidatieve stress en gestreste mitochondriën.
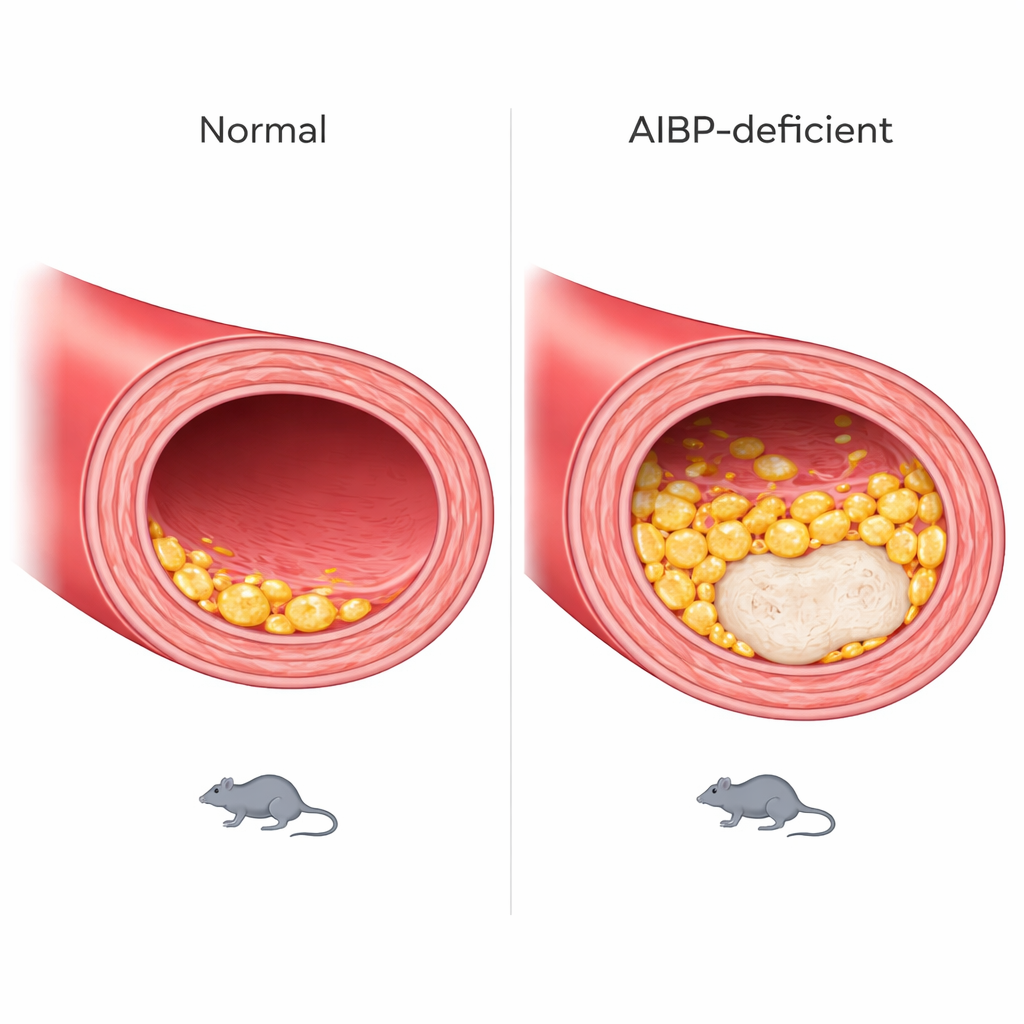
Groeiende, instabiele plaques in de vaatwand
Deze cellulaire veranderingen spiegelden zich in ernstigere vaatziekte. Dwarsdoorsneden van de hoofdslagader van het hart toonden dat AIBP-deficiënte muizen grotere plaques ontwikkelden en, belangrijker, grotere necrotische kernen — dode zones binnen de plaque die geassocieerd zijn met scheurgevoelige, “kwetsbare” laesies. Zowel mannelijke als vrouwelijke muizen werden getroffen, hoewel het patroon van waarlangs in het vat de ergste schade optrad tussen de seksen verschilde. De dieren kwamen ook sneller aan in gewicht en hadden hogere triglyceridenwaarden in het bloed, wat wijst op bredere verstoringen in vetstofwisseling.
Wat dit zou kunnen betekenen voor toekomstige behandelingen
Voor niet-specialisten is de kernboodschap dat niet alle cholesterol-beladen cellen in een plaque hetzelfde zijn. Als AIBP aanwezig is, gedragen schuimcellen zich vaker als opslagunits die stilletjes overtollig vet vasthouden. Als AIBP ontbreekt, herstructureren diezelfde cellen hun oppervlakken, bouwen inflammarafts en beginnen luide ontstekingssignalen te geven die plaques naar gevaarlijke, gevorderde stadia helpen drijven. Hoewel het werk bij muizen is gedaan, benadrukt het AIBP en de controle van deze membraan-brandpuntjes als potentiële aangrijpingspunten voor toekomstige therapieën gericht op het voorkomen dat arteriële plaques instabiel en levensbedreigend worden.
Bronvermelding: Li, S., Nazarenkov, N., Alekseeva, E. et al. Increased atherosclerosis and expression of inflammarafts in macrophage foam cells in AIBP-deficient mice.. Sci Rep 16, 7645 (2026). https://doi.org/10.1038/s41598-026-39113-2
Trefwoorden: atherosclerose, macrofaag-schuimcellen, ontsteking, cholesterolsmetabolisme, AIBP