Clear Sky Science · nl
AI-gedreven diagnose van acuut aorta-syndroom gebaseerd op multimodale informatiefusie
Waarom dit belangrijk is voor mensen met pijn op de borst
Het acuut aorta-syndroom is een medische noodsituatie waarbij de hoofdslagader van het lichaam plots kan scheuren, wat binnen enkele uren tot de dood kan leiden als het niet wordt herkend. Toch doen de symptomen vaak denken aan een hartinfarct, spierverrekking of zelfs indigestie, waardoor het berucht gemakkelijk gemist wordt. Deze studie beschrijft een nieuw kunstmatig-intelligentiesysteem dat CT-scans en bloedonderzoek combineert om artsen te helpen deze stille arteriële catastrofes eerder en nauwkeuriger te herkennen en om twijfelgevallen te markeren die een tweede beoordeling nodig hebben.
Een gevaarlijke scheur die in het volle zicht verborgen zit
Het acuut aorta-syndroom (AAS) omvat verschillende verwante problemen in de wand van de aorta, zoals klassieke dissectie, intramuraal hematoom en penetrerende ulcera. Ze delen allemaal hetzelfde gevaar: bloed forceert zich naar binnen of door de vaatwand, wat snel kan leiden tot ruptuur of verlies van bloedtoevoer naar vitale organen. Het risico is het hoogst in de eerste dag of twee nadat de symptomen beginnen, wanneer de sterfte zonder snelle behandeling naar ongeveer 70% kan stijgen. Artsen gebruiken CT-angiografie om de aorta te bekijken en bloedonderzoeken zoals D-dimeer en ontstekingsmarkers om stolling en immuunactiviteit in te schatten. Maar de klachten van patiënten zijn vaak vaag, lichamelijk onderzoek kan misleidend normaal zijn, en CT-beelden kunnen subtiel zijn of verslechterd door beweging of artefacten, waardoor ruwweg één op de drie gevallen aanvankelijk gemist wordt in de routinepraktijk.
Wat huidige AI-hulpmiddelen missen
De laatste jaren zijn krachtige systemen voor beeldherkenning ontwikkeld die CT- of röntgenbeelden kunnen scannen op tekenen van aortascheuren. De meeste van deze hulpmiddelen kijken echter alleen naar beelden en negeren bloedtesten, of ze koppelen gescheiden datastromen simpelweg aan elkaar zonder echt te leren hoe die interactie werkt. Dat staat haaks op hoe clinici denken: zij weven mentaal samen wat ze op de scan zien met laboratoriumwaarden en de voorgeschiedenis van de patiënt. Eenvoudige "stapeling" van beeldkenmerken en labwaarden kan de zaak zelfs verslechteren, omdat bloedtestgegevens ruisig, incompleet en wiskundig onderling verweven zijn. Veel AI-modellen functioneren bovendien als zwarte dozen en geven een oordeel zonder het redeneerproces bloot te leggen, wat spoedeisende artsen terughoudend maakt om erop te vertrouwen wanneer levens op het spel staan.
Een nieuwe manier om scans en bloedtesten te verbinden
De auteurs bouwden een multimodaal multi-schaal fusie (MMMF)-model dat is ontworpen om te imiteren hoe ervaren radiologen en cardiologen redeneren. Allereerst bekijkt een dubbelvertakt beeldencoder de CT-angiografiescan op twee detailniveaus: grote patches vangen de algemene vorm en koers van de aorta, terwijl kleinere patches zich richten op fijne details zoals kleine intimale scheurtjes of kleine bloedophopingen in de wand. Tegelijkertijd worden belangrijke bloedindicatoren—waaronder D-dimeer en een paneel van ontstekingsmarkers afgeleid van witte bloedcellen en bloedplaatjes—omgezet in numerieke featurepunten. Deze beeld- en laboratoriumkenmerken worden knooppunten in een grafiekachtige structuur, waar een geavanceerd graph neural network "berichten" tussen hen doorgeeft en leert hoe bepaalde bloedpatronen subtiele beeldbevindingen versterken of tegenspreken.
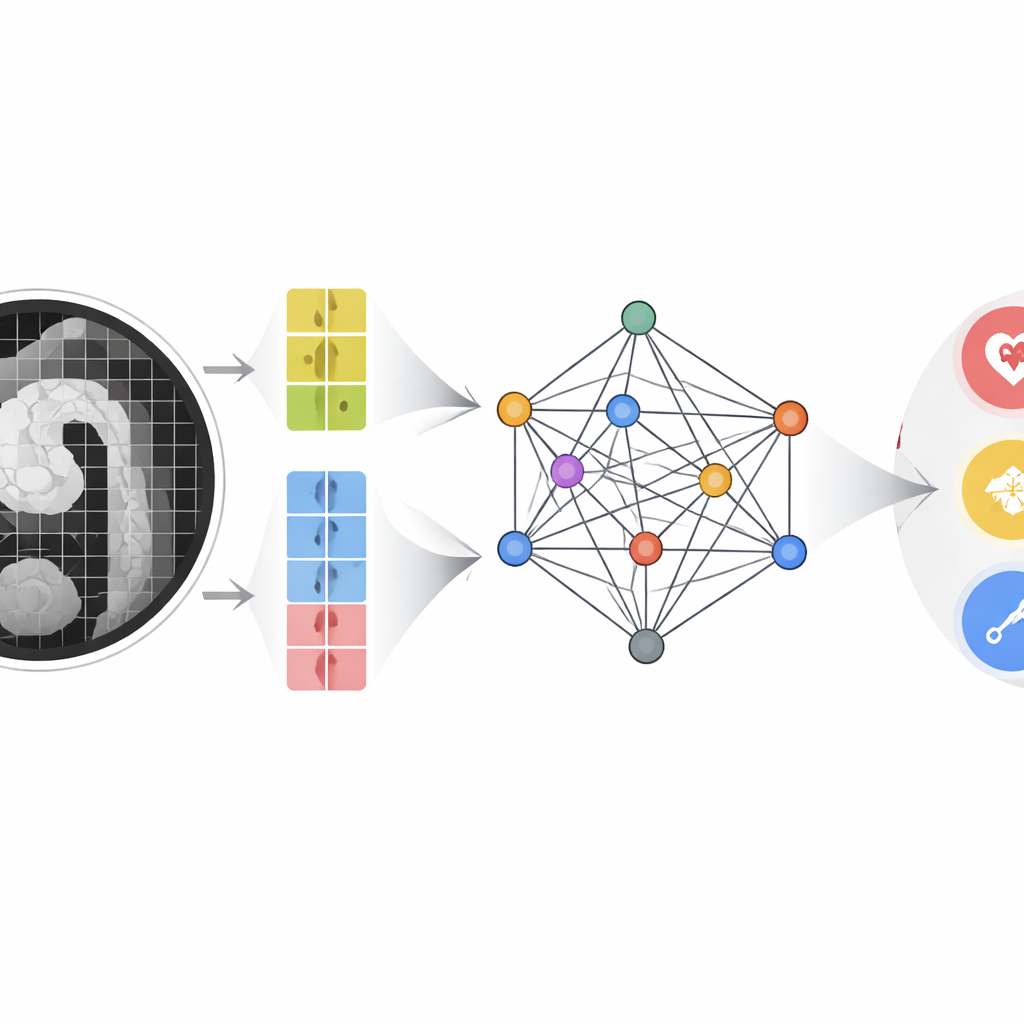
Hoe goed het systeem presteert
Het team trainde en testte het MMMF-model op CT-scans en gelijktijdige bloedtesten van 493 patiënten onderzocht tussen 2019 en 2024, met bevestigde AAS van verschillende typen en niet-AAS-controles. Ze vergeleken hun benadering met bekende beeld-only modellen, alleen-labdata modellen en verschillende state-of-the-art multimodale systemen die oorspronkelijk waren ontworpen om beelden met tekst te koppelen. Over nauwkeurigheid, precisie, recall en F1-score kwam het MMMF-model als beste uit de bus. De totale area under the receiver operating characteristic curve lag boven 0,9, wat duidt op een sterke capaciteit om te onderscheiden tussen normale aorta's, klassieke dissecties die de opgaande of dalende aorta betreffen, en atypische vormen. Beeldgegevens bleven de sterkste enkele informatiebron, maar zorgvuldig gestructureerde fusie met labgegevens leverde een meetbare verbetering op, vooral bij moeilijke of grensgevallen. Ablatie-experimenten toonden aan dat twee elementen cruciaal waren: de duale-schaal beeldweg en de transformer-gebaseerde grafiek die langafstandrelaties tussen kenmerken modelleert.
Op weg naar een partnerschap tussen artsen en machines
Naast de headline-nauwkeurigheidscijfers is een belangrijke bijdrage van dit werk de nadruk op samenwerking in plaats van vervanging. Het systeem is bijzonder bedreven in het snel afhandelen van duidelijk normale scans en duidelijk zieke atypische gevallen, en fungeert als een soort intelligente frontlinie-screening. Even belangrijk is dat het kan herkennen wanneer het eigen vertrouwen laag is—vaak in gevallen die menselijke experts ook lastig vinden, zoals vroege of mildere vormen van dissectie—zodat het die patiënten kan markeren voor urgente herbeoordeling, extra beeldvorming of consultatie met een senior. In wezen laat de studie zien dat wanneer beelddetails en bloedtestsignalen op een gestructureerde, klinisch geïnspireerde manier worden samengeweven, AI zowel de vroege diagnose van acuut aorta-syndroom kan aanscherpen als een vangnet kan bieden tegen gemiste noodsituaties, terwijl artsen stevig aan het roer blijven van de eindbeslissingen.
Bronvermelding: Yang, Z., Xu, S., Wang, B. et al. AI-driven diagnosis of acute aortic syndrome based on multi-modal information fusion. Sci Rep 16, 8332 (2026). https://doi.org/10.1038/s41598-026-39111-4
Trefwoorden: acuut aorta-syndroom, aortascheuring, medische AI, multimodale diagnose, graph neural network