Clear Sky Science · nl
Dlgap2‑tekort verstoort synaptische homeostase door ubiquitinegemedieerde afbraak van Itsn1 in een valproïnezuur‑geïnduceerd autismelijk model
Waarom een veelgebruikt medicijn en hersenbedrading ertoe doen
Valproïnezuur is een lang gebruikt middel tegen epilepsie en stemmingsstoornissen, maar gebruik tijdens de zwangerschap is in verband gebracht met een verhoogd risico op autisme bij kinderen. Deze studie stelt een dringende vraag voor gezinnen en artsen: wat doet dit middel precies met de zich ontwikkelende hersenbedrading? Door veranderingen terug te voeren tot specifieke moleculen bij synapsen — de communicatiepunten tussen zenuwcellen — onthullen de onderzoekers een nieuwe keten van gebeurtenissen die autismelijk gedrag kan verklaren en die kan wijzen op toekomstige behandelstrategieën. 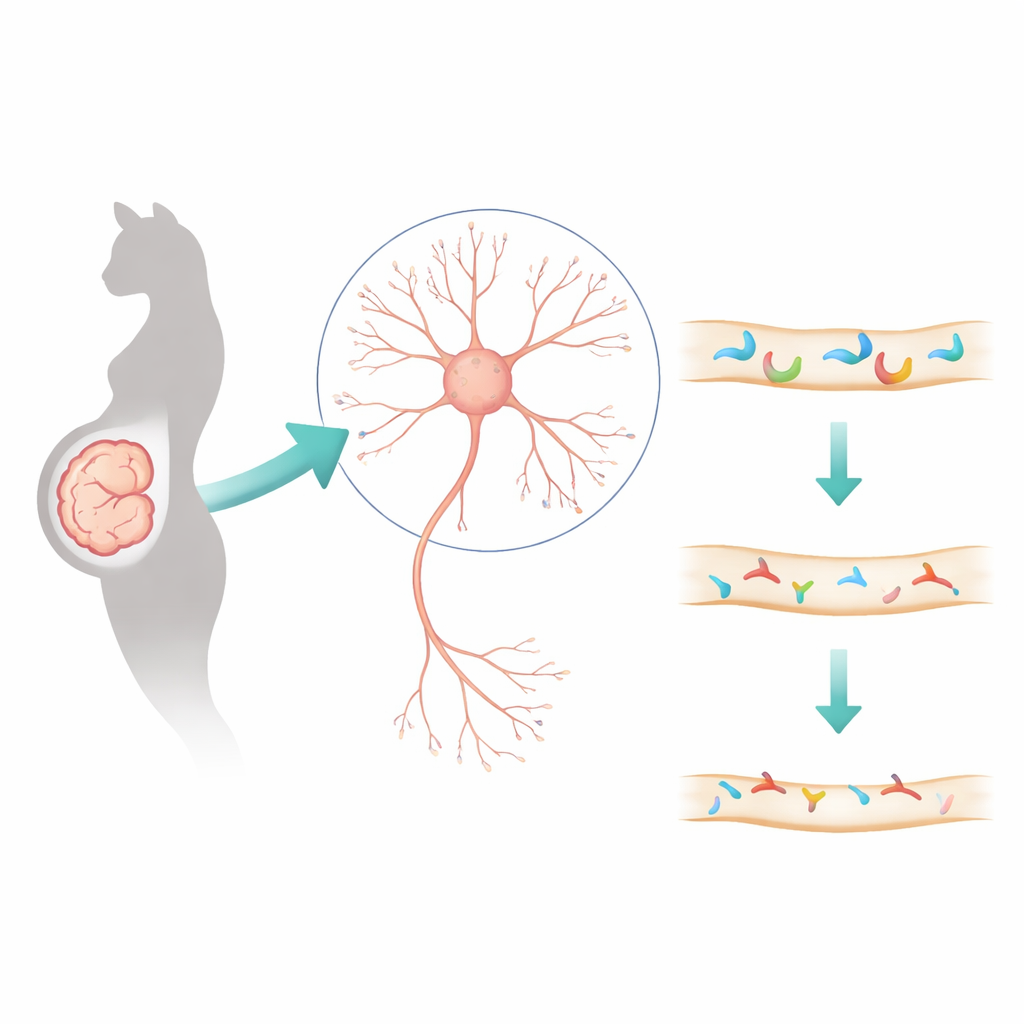
Soorten overstijgend zoeken naar gedeelde kwetsbare plekken
Om betrouwbare aanwijzingen te vinden, vertrouwde het team niet op één diermodel. Ze vergeleken hersenen of hersenachtige weefsels van menselijke corticale organoïden, apen, ratten en muizen die tijdens de zwangerschap aan valproïnezuur waren blootgesteld. Met grootschalige gen‑ en eiwitanalyses identificeerden ze een kleine set genen die in al deze systemen veranderden en die verband hielden met synapsen en isolatie van zenuwvezels. Eén gen sprong eruit: Dlgap2, een steuneiwit dat helpt bij het organiseren van de postsynaptische zijde van exciterende synapsen. Bij muizen die prenataal valproïnezuur kregen, daalden de Dlgap2‑niveaus in de cortex en, specifieker, binnen kleine synaptische compartimenten, wat suggereert dat dit structuurbehoudende molecuul een belangrijk slachtoffer is van medicijnblootstelling.
Van moleculaire verschuivingen naar gedragsveranderingen
De auteurs onderzochten vervolgens of verlies van Dlgap2 op zichzelf voldoende is om hersenfunctie te verstoren. Ze gebruikten virussen die short hairpin RNA dragen om Dlgap2 te verminderen in gekweekte muisneuronen en in pasgeboren muizen. In kweek hadden neuronen met minder Dlgap2 kortere vertakkingen en minder postsynaptische puncta, tekenen van verzwakte verbindingen. In levende dieren leidde gerichte knockdown van Dlgap2 in de hersenen tot autismelijk gedrag: jonge mannelijke muizen hadden moeite de locatie van een verborgen platform in een waterlabyrint te leren en toonden verminderde belangstelling voor sociale partners en sociale nieuwigheid in een driedeurtest. Deze veranderingen bootsen de leer‑ en sociale tekorten na die gezien worden in aan valproïnezuur blootgestelde dieren, en versterken het beeld dat verlies van Dlgap2 niet slechts een bijverschijnsel is maar een drijvende factor achter veranderd gedrag.
Het vinden van een kwetsbare partner in de synaps
Om te begrijpen hoe verlies van Dlgap2 doorwerkt in de synaps, bekeken de onderzoekers de eiwitten in de postsynaptische dichtheid, het dichte moleculaire paneel dat chemische signalen ontvangt. Met proteomics vonden ze dat vermindering van Dlgap2 de hoeveelheid van honderden synaptische eiwitten veranderde, vooral die betrokken bij het organiseren van synapsen en het recyclen van blaasjes via endocytose. Eén eiwit, Intersectin‑1 (Itsn1), daalde bijzonder sterk. Verdere biochemische analyses toonden aan dat Dlgap2 en Itsn1 fysiek binnen dezelfde eiwitcomplexen in synaps‑verrijkte fracties aanwezig zijn en dat beide voorkomen bij genen die met autisme geassocieerd zijn. Dit wees op een gerichte regulerende samenwerking tussen de twee moleculen binnen het drukke synaptische landschap. 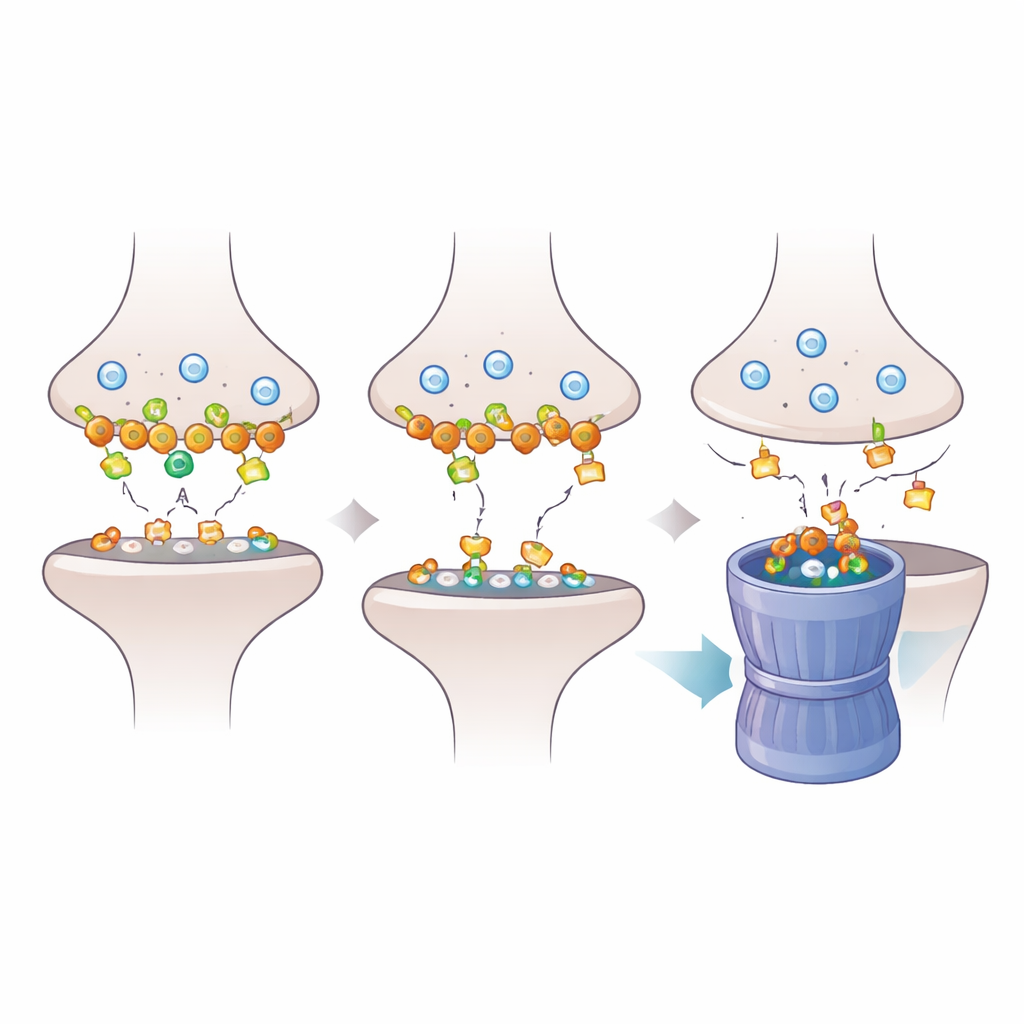
Een verborgen afvoerroute komt aan het licht
Het team vroeg zich vervolgens af waarom Itsn1‑niveaus dalen wanneer Dlgap2 ontbreekt. Ze zagen dat in synaptische compartimenten Dlgap2‑knockdown een vorm van eiwitlabeling veroorzaakte die bekendstaat als K48‑gekoppelde ubiquitinatie, een tag die eiwitten markeert voor afbraak door het proteasoom, de cellulaire "versnipperaar." Het blokkeren van dit afbraaksysteem met het middel MG132 voorkwam het verlies van Itsn1, wat aangeeft dat Dlgap2 normaal Itsn1 beschermt tegen tagging en vernietiging. Zonder Dlgap2 wordt Itsn1 steeds vaker getagd, naar het proteasoom gevoerd en uitgeput uit synapsen, waardoor endocytisch recyclen en de balans van synaptische activiteit worden ondermijnd. Het werk suggereert dat subtiele verschuivingen in de snelheid waarmee sleutel‑eiwitten worden afgebroken synapsen tijdens hersenontwikkeling kunnen destabiliseren.
Wat dit betekent voor autisme en toekomstige behandelingen
Samengevat stelt de studie een eenvoudig maar krachtig idee voor niet‑specialisten voor: prenatale blootstelling aan valproïnezuur kan een structureel "balk"‑eiwit (Dlgap2) bij synapsen verzwakken. Wanneer die balk verloren gaat, wordt het partnereiwit (Itsn1) te veel blootgesteld aan cellulair afvalbeheer, wat leidt tot gebrekkig recyclen van synaptische componenten en uiteindelijk tot verkeerd bedrade circuits en autismelijke gedragingen bij muizen. Hoewel veel genen en omgevingsfactoren bijdragen aan autisme, biedt deze Dlgap2–Itsn1‑as een concrete moleculaire keten van prenatale medicijnblootstelling naar veranderde hersenfunctie. Op de lange termijn zouden strategieën die deze samenwerking behouden of de eiwitafbraakmachines bij synapsen fijner afstellen kunnen helpen ontwikkelende hersenen tegen vergelijkbare vormen van verstoring te beschermen.
Bronvermelding: Guo, X., Zhang, L. & Zhuang, K. Dlgap2 deficiency disrupts synaptic homeostasis by promoting ubiquitin-mediated Itsn1 degradation in a valproic acid-induced autism-like model. Sci Rep 16, 8305 (2026). https://doi.org/10.1038/s41598-026-39099-x
Trefwoorden: valproïnezuur en zwangerschap, synaptische steuneiwitten, mechanismen van autismespectrum, ubiquitine‑proteasoomroute, muismodellen van autisme