Clear Sky Science · nl
Zebravis casr beïnvloedt hartstructuur en -functie
Waarom vissenharten van belang zijn voor de menselijke gezondheid
Onze harten vertrouwen op calcium, een eenvoudig mineraal, om goed te kloppen. Wanneer calciumsignalen ontsporen, kan dat leiden tot hartfalen of andere ernstige aandoeningen. Deze studie gebruikt kleine zebravissen—doorzichtige zoetwatervissen die vaak in laboratoria worden gebruikt—om te onderzoeken hoe een calcium-sensor in cellen de hartkracht en overleving beïnvloedt. Door één gen uit te schakelen dat cellen helpt calcium te detecteren, vonden de onderzoekers een keten van problemen in de pompwerking van het hart, de lichaamsvorm en zelfs de met lucht gevulde zwemblaas van de vis. Hun werk laat ook zien dat het bredere genetische achtergrond van een dier de impact van een schadelijke mutatie sterk kan verzachten of verergeren, een les met duidelijke echo’s in de menselijke geneeskunde.
Een cellulaire "thermostaat" voor calcium
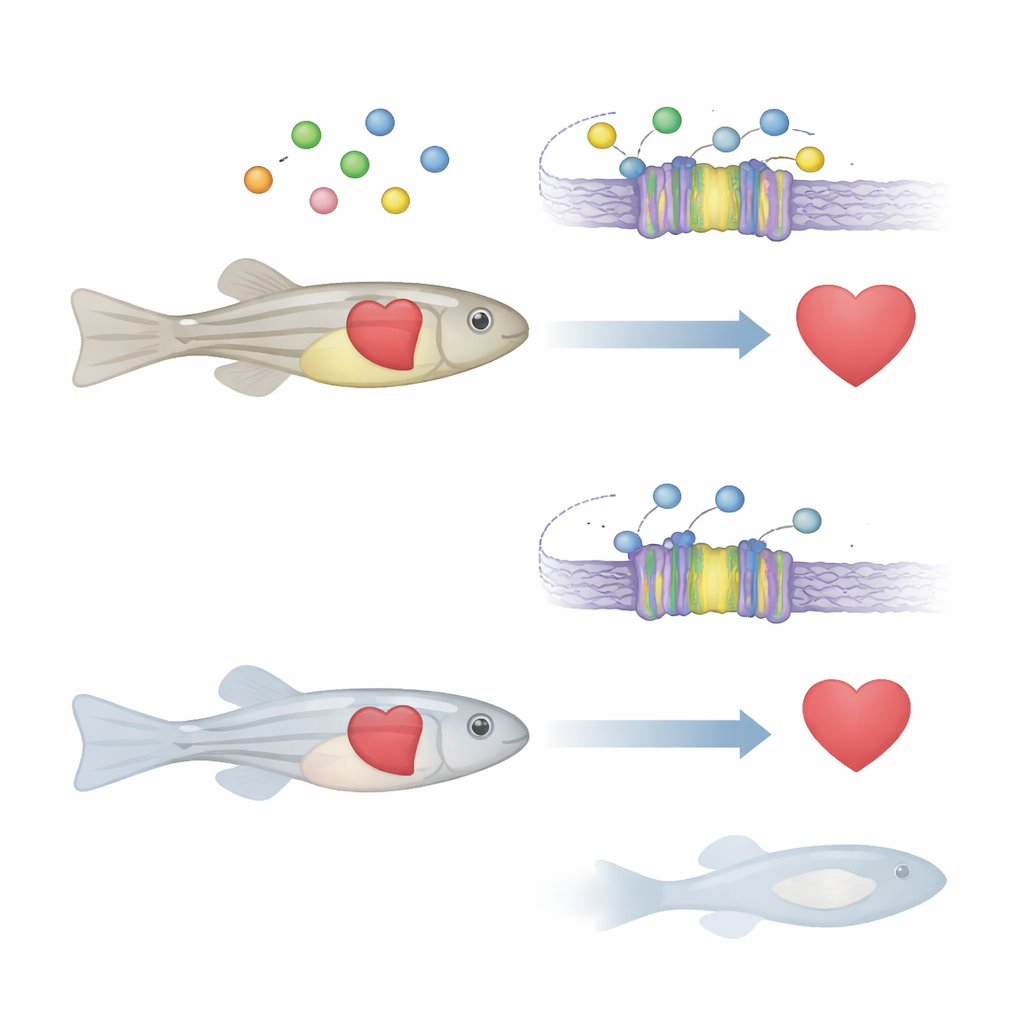
Calcium binnen en buiten cellen fungeert als een universeel signaal dat spierbeweging, hormoonafgifte en zelfs welke genen aan- of uitgezet worden, reguleert. Veel organen vertrouwen op een eiwit dat de calcium-sensorreceptor wordt genoemd; dit werkt als een thermostaat voor calciumniveaus. Wanneer het calcium buiten de cel verandert, past deze receptor de hormoonafgifte en andere processen aan om het evenwicht te herstellen. Bij mensen worden defecten in deze receptor al gekoppeld aan bot- en mineraalstoornissen en ze worden verdacht betrokken te zijn bij hartziekten en sommige vormen van kanker. Hoe deze calciumsensor precies hartontwikkeling en -functie in een heel dier beïnvloedt, bleef echter onduidelijk.
Wat gebeurt er als de calcium-sensor wordt uitgeschakeld
Het team richtte zich op de zebravisversie van dit gen, genaamd casr, die sterk bewaard is ten opzichte van zijn menselijke tegenhanger. Met moderne genbewerkingstools maakten ze zebravissen waarin beide kopieën van casr werden uitgeschakeld. In het begin leken de jonge vissen bijna normaal. Maar vijf dagen na bevruchting slaagden veel mutanten er niet in hun zwemblaas te laten opblazen, een klein met gas gevuld orgaan dat de drijfkracht regelt. Deze vissen zonken naar de bodem, zwommen slecht, ontwikkelden al snel een kromming van de wervelkolom en stierven allemaal binnen twee weken. Deze uiterlijke tekenen wezen op ernstige interne problemen die meer dan één orgaansysteem troffen.
Een zwakker, kleiner en langzamer hart
Hoge-snelheidsvideo’s en beeldanalyse van kloppende harten toonden aan hoe ingrijpend het ontbreken van de calcium-sensor de cardiale prestaties aantastte. Bij normale zebravislarven vult en leegt de hartventrikel zich in een sterk ritmisch patroon. Bij de mutanten was de ventrikel merkbaar kleiner tijdens het vullen, klopte het hart trager en per slag werd er minder bloed weggepompt. Maten van hoeveel het hartspier samentrekt en hoeveel de oppervlakte van de pompkamer per slag verandert, waren beide verminderd, wat op verzwakte contractie wijst. Het totale hartminuutvolume—het bloedvolume dat per minuut wordt verplaatst—daalde sterk. Op geniveau veranderden honderden transcripties en belangrijke netwerken die calciumbehandeling en de machinerie van spiercontractie regelen, werden omlaag bijgesteld, waarmee de genbewerking werd gekoppeld aan zowel moleculair als mechanisch hartfalen.
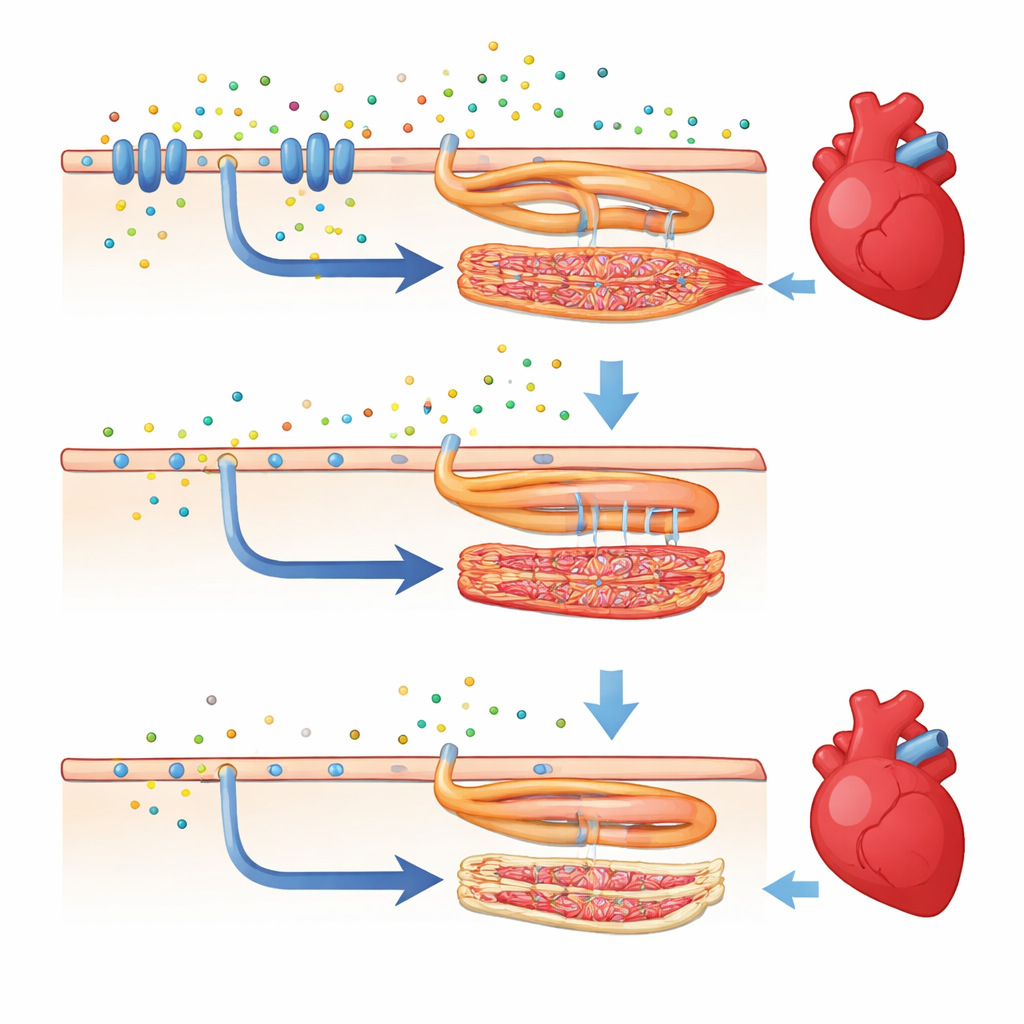
Hoe achtergrondgenen een ziek hart kunnen redden
Verrassend genoeg gedroeg dezelfde casr-mutatie zich heel anders in een andere veelgebruikte zebravissenstam, bekend als TL (Tupfel long-fin). Toen de genknock-out in deze nieuwe genetische achtergrond werd ingebracht, konden de vissen hun zwemblaas opblazen, volwassen worden en toonden ze veel betere pompfunctie van het hart. Hun harten waren nog steeds enigszins aangetast—de hartslag bleef lager dan normaal—maar maten van hoe krachtig de ventrikel samentrok en de hoeveelheid bloed per minuut bijna gelijk kwamen te liggen met gezonde vissen. In deze 'geredde' dieren herstelden veel van de genen die verbonden zijn met calciumsignalering en hartspiercontractie zich tot tussenniveaus, hoger dan in de oorspronkelijke zieke lijn. Dit laat zien dat andere genen verspreid over het genoom de impact van een schadelijke verandering kunnen bufferen of versterken.
Signalen die harten en drijfvermogen vormen
Buiten het hart verstoorde het verlies van de calcium-sensor ook grote groeiregulerende systemen in het embryo. Genen in de Wnt- en Hedgehog-signaleringswegen—bekende architecten van orgaanvorming—werden omlaag gezet in de mutanten. Deze veranderingen dragen waarschijnlijk bij aan het mislukken van het opblazen van de zwemblaas, wat op zijn beurt de overleving kan verslechteren door het lastiger te maken voor de vis om efficiënt te eten en zich te bewegen. Merkers van differentiatie van hartspiercellen waren ook verminderd en de ventrikels waren kleiner, wat erop wijst dat de calcium-sensor helpt bepalen hoe hartspiercellen groeien en rijpen.
Wat dit betekent voor het begrijpen van ziektarisico
Alles bij elkaar toont dit werk aan dat de calcium-sensorreceptor een cruciale beschermer is van zowel hartfunctie als correcte orgaanontwikkeling in zebravissen. Wanneer deze sensor verloren gaat, haperen calciumsignalen, trekt het hartspierweefsel zwak samen, faalt de zwemblaas en sterven de dieren jong. Toch benadrukt de dramatische redding in een andere genetische stam een belangrijke boodschap: de rest van het genoom kan sterk beïnvloeden hoe gevaarlijk een bepaalde mutatie werkelijk is. Voor de menselijke gezondheid onderstreept dit waarom mensen met vergelijkbare risicovarianten heel verschillende ziekte-uitkomsten kunnen ervaren en waarom het begrijpen van zowel kernziegenen als hun genetische achtergrond essentieel is om hartziekten te voorspellen en te behandelen.
Bronvermelding: Liu, L., Hu, Y., Xie, B. et al. Zebrafish casr modulates cardiac structure and function. Sci Rep 16, 8543 (2026). https://doi.org/10.1038/s41598-026-39063-9
Trefwoorden: calciumsignalering, hartontwikkeling, zebravismodel, genetische achtergrond, cardiale functie