Clear Sky Science · nl
In silico-identificatie van inhaleerbare kleine-molecuul IL-33/ST2-antagonisten voor ernstige type-2-high astma-endotopen
Waarom dit van belang is voor ademen
Voor miljoenen mensen met ernstig astma laten zelfs moderne inhalatoren en geavanceerde injecties hen vaak nog naar adem happend achter en lopen ze risico op gevaarlijke aanvallen. Deze studie onderzoekt of bekende, pilachtige geneesmiddelen opnieuw ontworpen kunnen worden als inhaleerbare behandelingen die een van de vroegste "alarmsignalen" in de longen blokkeren. Met behulp van alleen computersimulaties zochten de onderzoekers naar kleine moleculen die op een sleutelreceptor betrokken bij ernstige, door allergie gedreven astma zouden kunnen passen, waarmee ze de basis leggen voor toekomstige laboratoriumtesten in plaats van een direct inzetbaar medicijn te bieden.
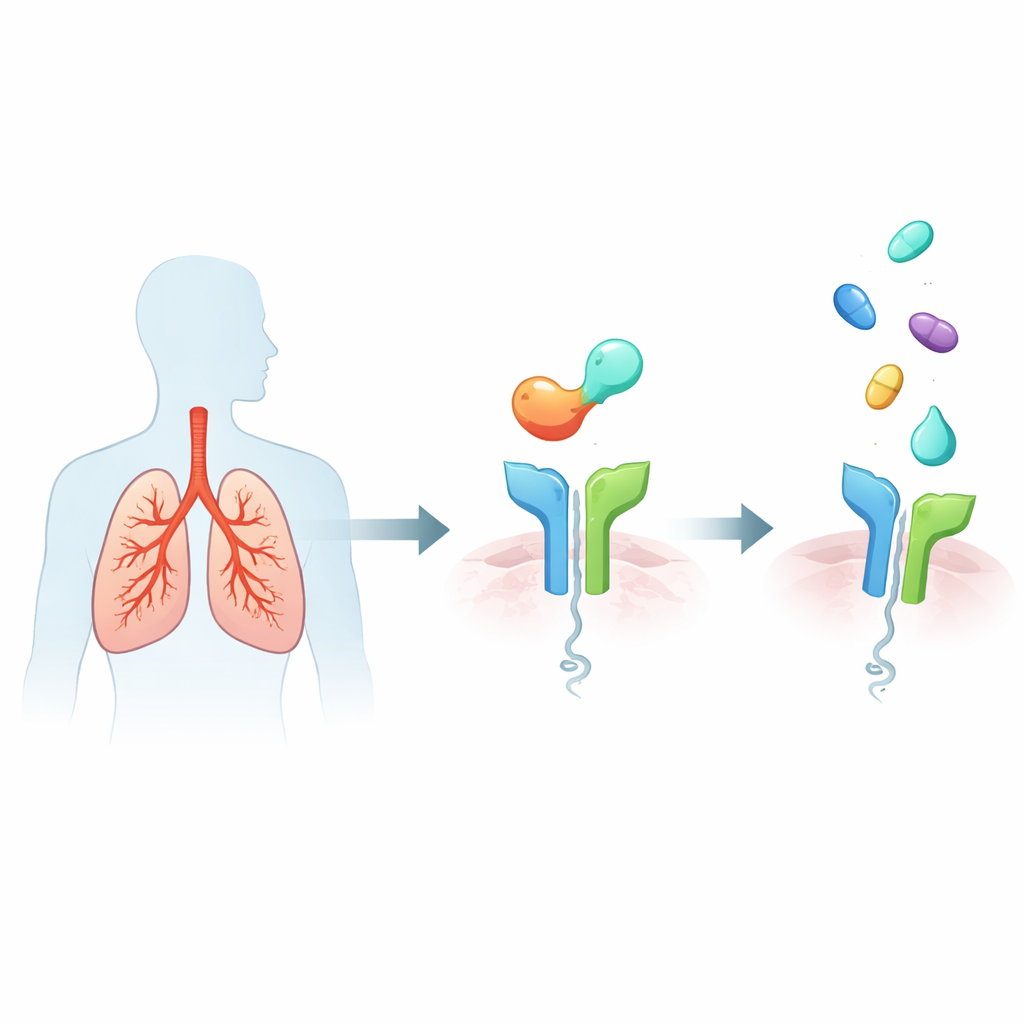
Het alarmsysteem binnen astmatische longen
Ernstig type-2-high astma wordt gekenmerkt door een overactieve immuunreactie die de luchtwegen vult met slijm en ontstekingscellen, de ademhalingsbuizen vernauwt en na verloop van tijd longstructuur beschadigt. Een belangrijke trigger is een eiwit dat IL-33 heet, vrijgegeven door gestreste cellen van het luchtwegepitheel. IL-33 bindt aan een receptor genaamd ST2 op verschillende immuuncellen, die vervolgens krachtige boodschapperstoffen loslaten die kenmerkende astma-symptomen aandrijven zoals piepende ademhaling, opvlammingen en langdurige hermodellering van de luchtwegen. Omdat verhoogde IL-33/ST2-activiteit samenhangt met ernstigere symptomen en frequentere aanvallen, is ST2 naar voren gekomen als een aantrekkelijk upstream-doel: blokkeer ST2 en mogelijk demp je veel downstream-ontstekingssignalen tegelijk.
Van antilichamen naar alledaagse geneesmiddelen
Meerdere huidige therapieën voor ernstig astma gebruiken geïnjecteerde antilichamen die ontstekingsproteïnen in het bloed opvangen of hun receptoren blokkeren. Hoewel effectief voor sommige patiënten, zijn deze biologische geneesmiddelen duur, moeten ze via injectie worden toegediend en richten ze zich vooral op signalen verder stroomafwaarts in de route. Daarentegen kunnen kleine-molecuulgeneesmiddelen — meer zoals traditionele tabletten of inhalatoren — op schaal worden geproduceerd, gemakkelijk worden opgeslagen en mogelijk direct in de longen worden toegediend. De uitdaging is dat ST2 IL-33 bindt via een breed eiwit-eiwit oppervlak, wat moeilijker is voor kleine moleculen om te verstoren dan een nette, diepe pocket op een enzym. De auteurs gebruikten daarom hoogwaardige structurele gegevens voor het ST2–IL-33-complex en moderne in silico-hulpmiddelen om te onderzoeken of bekende ontstekingsremmers onverwacht een deel van dit interface zouden kunnen grijpen.
De receptoroppervlakte doorzoeken met de computer
Met behulp van de kristalstructuur van menselijk ST2 gebonden aan IL-33 verwijderde het team eerst IL-33 om het bindingsoppervlak van de receptor bloot te leggen en gebruikte een pocket-vindend programma om het veelbelovendste gebied aan te wijzen waar een klein molecuul zich zou kunnen nestelen. Ze selecteerden vervolgens tien klinisch relevante kleine moleculen die al worden gebruikt bij astma of aanverwante immuunziekten — zoals de leukotrieenremmers Montelukast en Zafirlukast, immuunmodulerende thalidomideverwanten en JAK-remmers — plus een eerder gerapporteerd ST2-gericht molecuul als referentie. Met virtuele dockingsoftware werd elk verbinding duizenden keren op het ST2-oppervlak gepositioneerd en werden de best passende posities gescoord op voorspelde bindingssterkte. Zafirlukast kwam naar voren als de hoogst gerangschikte scaffold, iets beter presterend dan Montelukast en de bekende ST2-gerichte comparator.
Een leidend molecuul op het scherm bijstellen
Aangezien Zafirlukast de meest veelbelovende balans van voorspelde binding en algemeen medicijnachtig gedrag vertoonde, gebruikten de auteurs een AI-gestuurd ontwerpinstrument om een gewijzigde versie van dit molecuul te creëren. Het doel was zijn grip op ST2 te behouden terwijl het voorspelde veiligheidsprofiel werd verbeterd. Het herontworpen analoog had een zeer vergelijkbare docking-score en werd in silico als minder toxisch voorspeld. Gedetailleerde contactkaarten suggereerden dat zowel het ouder- als het gemodificeerde verbinding meerdere van dezelfde ST2-aminozuren raken die normaal IL-33 contacteren, wat erop wijst dat ze functioneel belangrijke delen van het interface bezetten. Uitgebreide moleculaire dynamics-simulaties — een halve microseconde aan virtuele beweging in water en zout — toonden aan dat de receptor en ligand beide flexibel bleven, waarbij het kleine molecuul verschillende posities langs het oppervlak aannam in plaats van star op één plek te vergrendelen. Berekeningen van interactie-energieën in de tijd wezen op een betekenisvolle maar dynamische associatie, consistent met een molecuul dat een relatief vlak eiwit-eiwit oppervlak aftast.
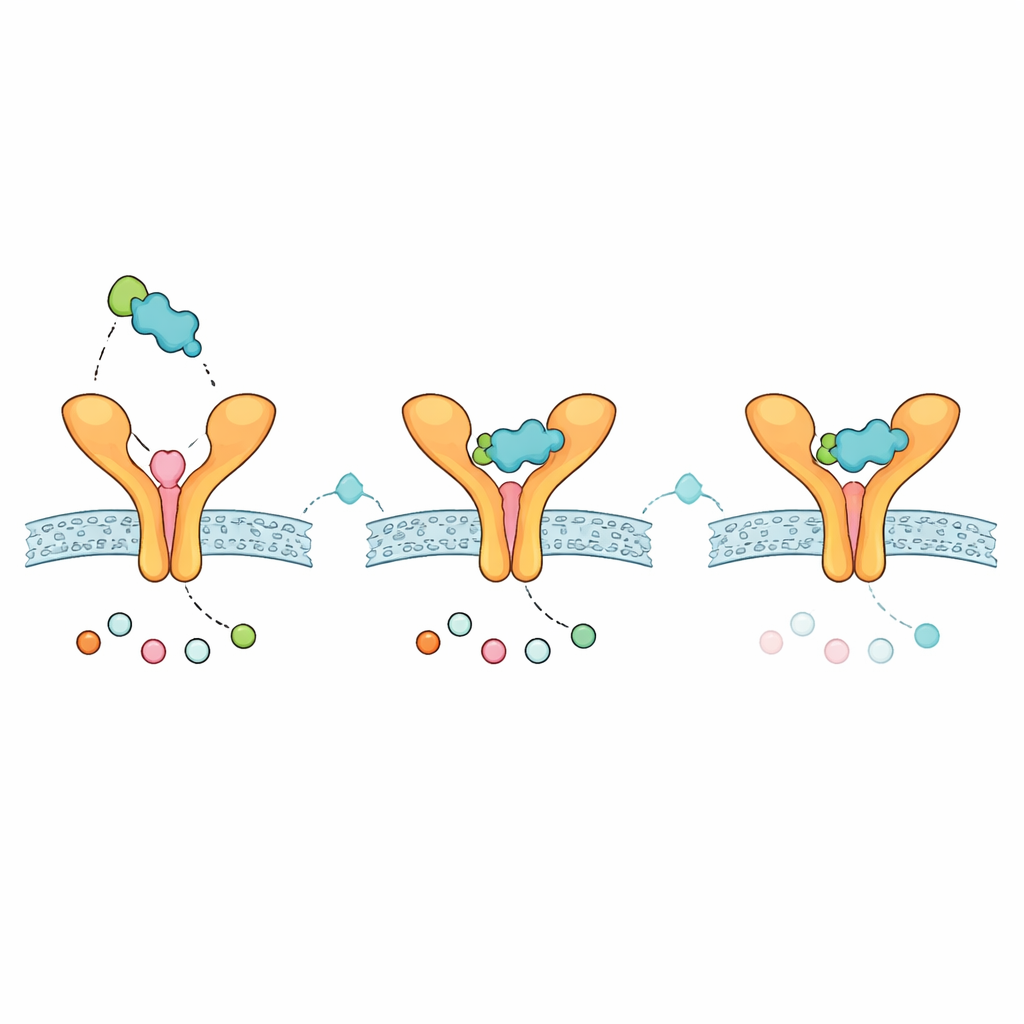
Winkjes over hoe een toekomstige inhalator zich zou kunnen gedragen
Om te onderzoeken of het gemodificeerde Zafirlukast plausibel als geneesmiddel zou kunnen functioneren, voerde het team standaard computationele controles uit voor absorptie, distributie, metabolisme, excretie en toxiciteit. Het analoog voldeed aan gangbare regels voor orale drug-likeness, vertoonde een matige grootte en lipofilie, en werd voorspeld de hersenen te mijden — eigenschappen die gunstig kunnen zijn voor een op de long gerichte behandeling met beperkte systemische bijwerkingen. Schattingen van oplosbaarheid varieerden per model, wat impliceert dat zorgvuldige formulering nodig zou zijn, vooral voor niet-orale toedieningsroutes zoals inhalatie. De verbinding werd ook voorspeld te interageren met bepaalde leverenzymen, wat suggereert dat potentiële geneesmiddel–geneesmiddelinteracties aandacht zouden vergen als het ooit naast andere medicijnen zou worden gebruikt.
Wat dit werk werkelijk aantoont
In plaats van een nieuw astmamedicijn te leveren, toont deze studie een stapsgewijze computationele strategie voor het vinden en verfijnen van kleine moleculen die het IL-33/ST2-alarmssysteem aan het oppervlak van luchtwegcellen kunnen verstoren. Het belicht Zafirlukast en een AI-geoptimaliseerde verwant als plausibele uitgangspunten voor laboratoriumexperimenten, en laat zien dat ze sleutelgebieden van het ST2-interface kunnen bezetten en brede voorspelbare veiligheid en medicijnachtige eigenschappen hebben. Alle bewijzen zijn echter virtueel: het werk bewijst niet dat deze moleculen IL-33 blokkeren in zijn binding aan ST2, ontstekingssignaalering dempen of patiënten helpen makkelijker te ademen. Die antwoorden vereisen biochemische testen, celstudies, diermodellen en uiteindelijk klinische proeven. Vooralsnog biedt de studie een computationele routekaart en een korte lijst van kandidaat-scaffolds voor wetenschappers die het lichaamseigen astma-alarm willen omzetten in een praktisch, inhaleerbaar medicijndoel.
Bronvermelding: Sun, G., Liu, Q., Yu, M. et al. In Silico identification of inhalable small-molecule IL-33/ST2 antagonists for severe type-2-high asthma endotypes. Sci Rep 16, 7996 (2026). https://doi.org/10.1038/s41598-026-39027-z
Trefwoorden: ernstig astma, IL-33 ST2-route, kleine-molecuulantagonisten, in silico geneesmiddeldesign, ingeademde therapieën