Clear Sky Science · nl
Analyse van het mechanisme en de prognostische waarde van PRKCQ-AS1 bij het remmen van de progressie van longadenocarcinoom via regulatie van de PD-1/PD-L1-route
Waarom dit verborgen molecuul ertoe doet
Longadenocarcinoom is de meest voorkomende vorm van longkanker, en zelfs met moderne immunotherapie krijgt te veel patiënten te maken met terugkeer van de ziekte of therapieresistentie. Deze studie richt zich op een weinig bekend RNA-molecuul, PRKCQ-AS1, dat geen eiwitten produceert maar mogelijk stilletjes beïnvloedt of longtumoren ongecontroleerd groeien of onder controle worden gehouden door het immuunsysteem. Inzicht in deze onzichtbare speler kan nieuwe mogelijkheden openen voor vroegere prognose en betere inzet van immunotherapie.
Een stille signaalgever in longtumoren
De onderzoekers begonnen met het doorzoeken van een grote openbare kanker-database om te bepalen hoeveel PRKCQ-AS1 aanwezig is in tumormonsters van honderden mensen met longadenocarcinoom. Ze vonden dat dit RNA consequent lager is in tumorweefsel dan in normaal longweefsel, en dat de niveaus nog verder dalen naarmate tumoren naar latere stadia vorderen. Patiënten van wie de tumoren minder van dit RNA bevatten, bleken in de loop van de tijd slechter af te zijn, wat suggereert dat PRKCQ-AS1 zich meer gedraagt als een natuurlijke rem op kanker dan als brandstof. Het team bevestigde dit patroon vervolgens in echte patiëntweefselmonsters die in de kliniek waren verzameld, wat het idee versterkt dat PRKCQ-AS1 als nuttig waarschuwingssignaal voor agressieve ziekte kan dienen.
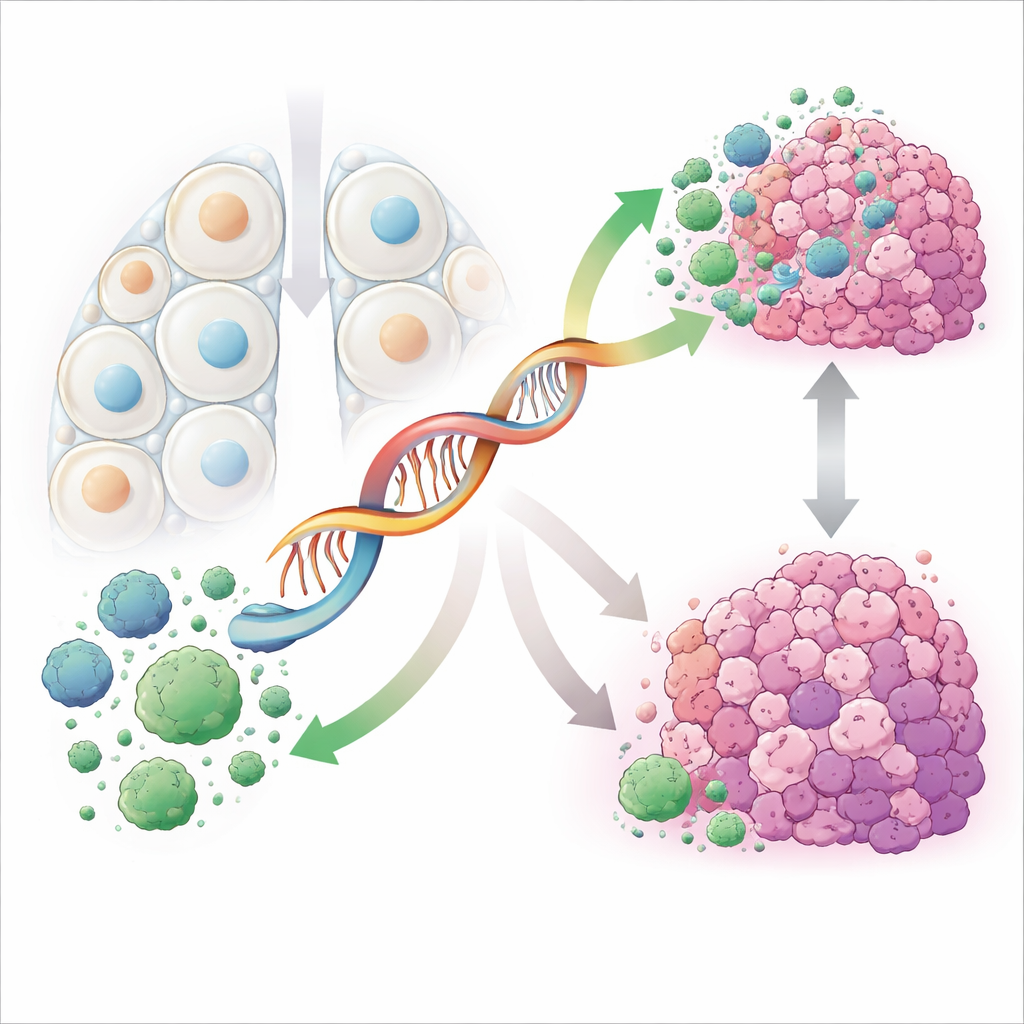
Onderzoeken hoe het molecuul het gedrag van kankercellen vormt
Om van databasepatronen naar biologie te gaan, onderzochten de wetenschappers longadenocarcinoomcellen die in het laboratorium werden gekweekt. Ze verhoogden of verlaagden kunstmatig de PRKCQ-AS1-niveaus en observeerden hoe de cellen reageerden. Wanneer ze dit RNA verminderden, vermenigvuldigden kankercellen zich sneller, bewogen ze zich gemakkelijker over kunstmatige barrières en drongen ze agressiever door membranen heen. Tegelijkertijd ondergingen minder cellen geprogrammeerde celdood, het zelfvernietigingsproces dat normaal beschadigde cellen onder controle helpt houden. Het verhogen van PRKCQ-AS1 had het tegenovergestelde effect: de groei vertraagde, beweging en invasie namen af en meer cellen stierven. Gezamenlijk tonen deze experimenten aan dat PRKCQ-AS1 rechtstreeks verschillende kernachtige eigenschappen die longtumoren gevaarlijk maken, in toom houdt.
Verbindingen met de verdediging van het lichaam
De studie onderzocht ook hoe dit RNA de bredere omgeving rond de tumor kan beïnvloeden, met name immuuncellen die patrouilleren op zoek naar abnormale groei. Met behulp van computationele hulpmiddelen bouwden de auteurs een regulatoir kaartwerk dat PRKCQ-AS1 verbindt met andere RNA-moleculen en genen die betrokken zijn bij kanker en immuniteit. Ze ontdekten dat genen die aan dit RNA zijn gekoppeld clusteren in routewegen gerelateerd aan immuunreacties en celsignalering. In patiëntgegevens bleken tumoren met meer PRKCQ-AS1 hogere niveaus te huisvesten van bepaalde gunstige immuuncellen, waaronder cytotoxische T-cellen die kankercellen direct kunnen vernietigen. Tumoren met minder PRKCQ-AS1 vertoonden een andere samenstelling van immuuncellen die mogelijk minder effectief of zelfs uitgeput zijn, wat suggereert dat dit RNA helpt bepalen hoe gastvrij—or vijandig—de tumoromgeving is voor de afweer van het lichaam.
Beheersen van een sleutel-immuuncontrolepunt
Een van de krachtigste verdedigingsmechanismen die tumoren gebruiken om te overleven is het PD-1/PD-L1-controlesysteem, dat fungeert als een moleculaire vermomming die immuuncellen zegt zich terug te trekken. Moderne immunotherapie medicijnen werken door dit signaal te blokkeren. De auteurs ontdekten een sterke verbinding tussen PRKCQ-AS1 en dit controlepunt. In patiëntweefsels en in gekweekte cellen ging laag PRKCQ-AS1 samen met hogere niveaus van PD-1 en PD-L1, terwijl het verhogen van het RNA die controlesignalen naar beneden duwde. Dit suggereert dat wanneer PRKCQ-AS1 overvloedig aanwezig is, tumorcellen minder “val niet aan”-signalen op hun oppervlak tonen, waardoor ze zichtbaarder worden voor immuuncellen. Wanneer PRKCQ-AS1 schaars is, is het controlepunt actiever, waardoor het voor tumoren gemakkelijker wordt zich te verbergen voor immuunaanvallen en te blijven groeien.
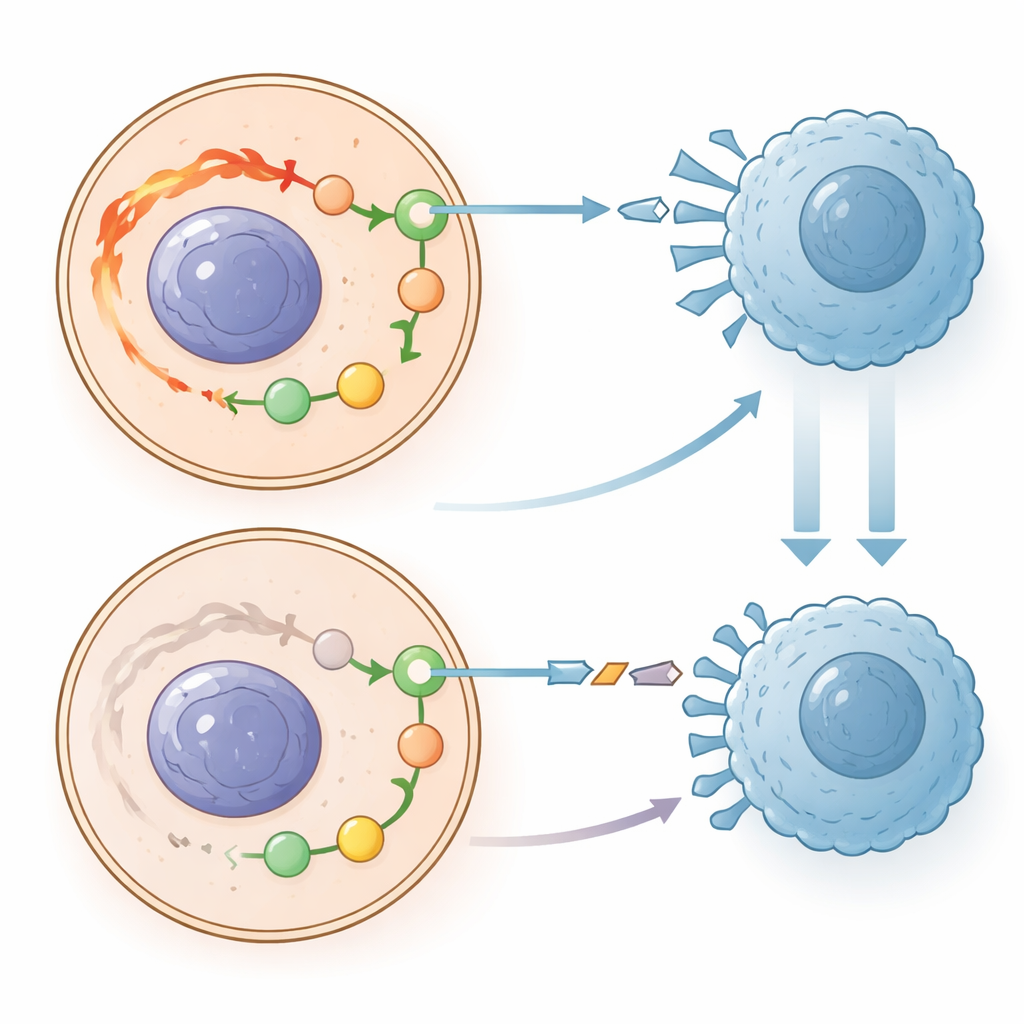
Wat dit kan betekenen voor toekomstige zorg
Hoewel dit werk nog steeds steunt op celmodellen en een relatief kleine klinische groep, wijst het op PRKCQ-AS1 als een natuurlijke tumorsuppressor bij longadenocarcinoom. Door de groei van kankercellen te remmen en een belangrijke route voor immuunontsnapping te dempen, kan dit niet-coderende RNA zowel beïnvloeden hoe snel tumoren vorderen als hoe goed ze reageren op immunotherapie. In de toekomst kan het meten van PRKCQ-AS1 artsen helpen de prognose van een patiënt beter in te schatten, en behandelingen die de activiteit ervan herstellen of nabootsen zouden immuun-gebaseerde geneesmiddelen effectiever kunnen maken. Voor nu voegt deze studie een belangrijk stuk toe aan de puzzel waarom sommige longkankers weerstand bieden aan de verdediging van het lichaam—en biedt het een nieuwe moleculaire aanzet om ze aan te pakken.
Bronvermelding: Wu, M., Wang, Y., He, G. et al. Analysis of the mechanism and prognostic value of PRKCQ-AS1 in inhibiting the progression of lung adenocarcinoma via regulating the PD-1/PD-L1 pathway. Sci Rep 16, 9782 (2026). https://doi.org/10.1038/s41598-026-39024-2
Trefwoorden: longadenocarcinoom, immuuncontrolepunt, lange niet-coderende RNA, tumormicro-omgeving, PD-1 PD-L1