Clear Sky Science · nl
Structuurgebaseerde modellering onthult de moleculaire basis voor de nieuwe activiteit van CYP153A6 richting tolueenderivaten
Lastige chemische taken overlaten aan de natuur
Chemici en de industrie zijn afhankelijk van reacties die zuurstof toevoegen aan hardnekkige koolstof–waterstofbindingen, bijvoorbeeld om verontreinigingen te reinigen of bouwstenen voor geneesmiddelen en geuren te maken. Dit op een schone manier doen, zonder agressieve chemicaliën of afval met zware metalen, is lastig. Deze studie kijkt naar een natuurlijk katalysator, een enzym genaamd CYP153A6 uit een bodembacterie, en stelt een eenvoudige vraag met grote implicaties: kan dit enzym gestuurd worden om selectief tolueenachtige stoffen—veel voorkomende componenten van brandstoffen en oplosmiddelen—om te zetten in nuttigere en milieuvriendelijkere producten?
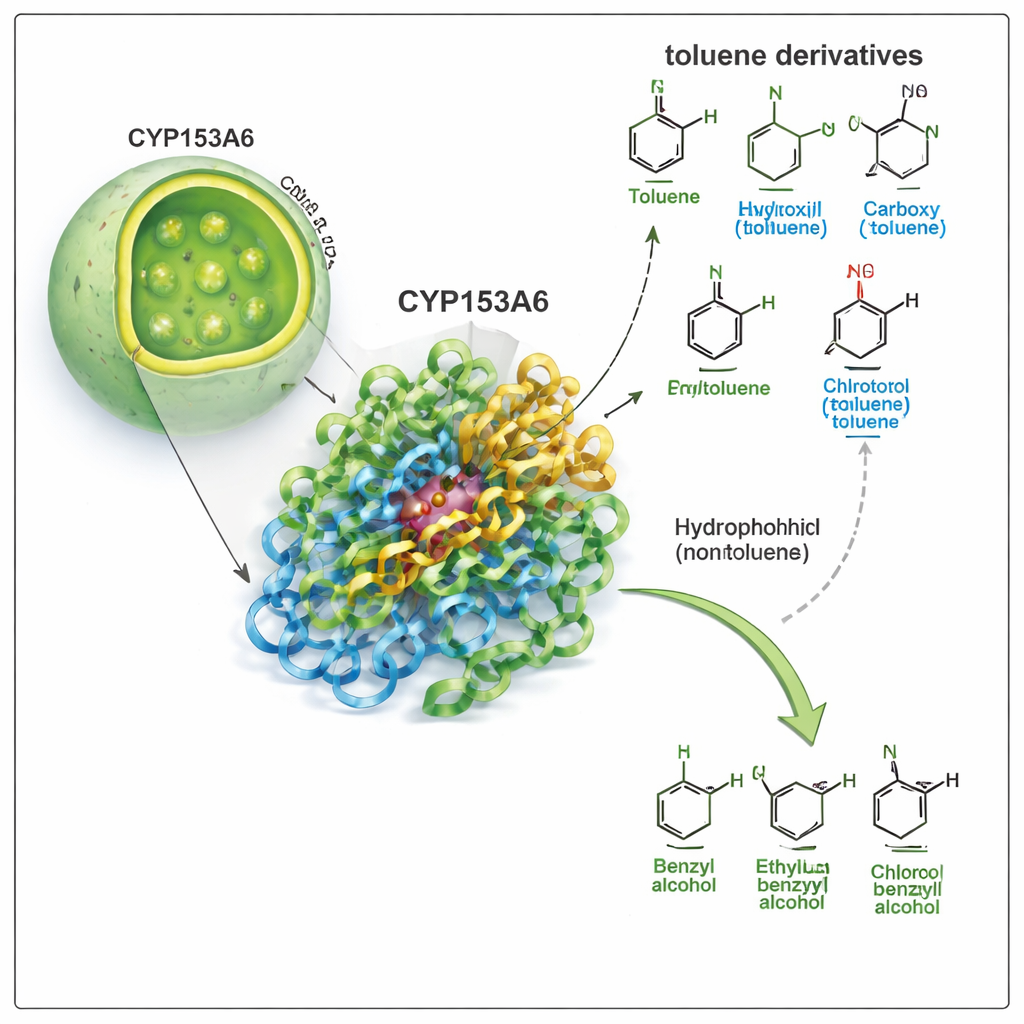
Een enzym dat één specifieke plek kiest
CYP153A6 behoort tot de grote cytochroom P450-familie, de veelzijdige oxidatiespecialisten uit de natuur. In tegenstelling tot veel industriële katalysatoren werkt dit enzym in water, bij matige temperatuur, en kiest het zeer specifieke posities op een molecuul. Eerder werk toonde dat CYP153A6 zuurstof toevoegt aan de uiteinden van eenvoudige koolwaterstofketens en aan bepaalde plantaardige geurstoffen. Hier vragen de auteurs of het ook het ‘benzylïsche’ koolstofatoom—de kleine zijketen aan een benzeenring—kan aanvallen in tolueen en verwante verbindingen. Die transformatie zet tolueenderivaten om in benzylalcoholen, waardevolle bouwstenen voor geneesmiddelen, smaakstoffen en fijne chemicaliën.
Testen welke moleculen het enzym prefereert
Het team voerde eerst biotransformatie-experimenten uit met gemodificeerde E. coli-cellen die CYP153A6 produceren, zowel als hele cellen als in celvrije extracten. Ze zetten het enzym bloot aan een reeks tolueenderivaten, waarbij ze de groep aan de aromatische ring veranderden (zoals methyl, chloor, methoxy, hydroxyl of nitro) en de positie ervan (para, meta of ortho). Het enzym werkte erg goed op apolaire of slechts licht polaire verbindingen, zoals p-cymeen, p-xyleen, p-methylanisool en p-chloor tolueen, en zette consequent de benzylïsche methylgroep om in een benzylalcohol. Opvallend genoeg negeerde het volledig sterkere polaire moleculen zoals p-cresol, p-methylbenzylalcohol en p-nitrotolueen, hoewel deze structureel vergelijkbaar zijn. Dit patroon suggereert dat de bindingspocket van het enzym sterk hydrofoob is en polaire groepen afstoot.
Een 3D-kaart van het moleculaire werktuig bouwen
Aangezien de driedimensionale structuur van CYP153A6 niet experimenteel was bepaald, bouwden de onderzoekers een hoogwaardig computermodel met behulp van een nauw verwant P450 waarvan de structuur wel bekend is. Ze valideerden dit model door de geometrie te controleren en lange moleculaire dynamicasimulaties uit te voeren om te zien of het eiwit in de tijd stabiel bleef, wat het deed. De simulaties toonden een begraven actieve centrum dat via smalle tunnels met de buitenwereld verbonden is, waarlangs substraten binnenkomen en producten naar buiten gaan. Deze tunnels worden gevormd en gecontroleerd door flexibele lussen aan het eiwitoppervlak, wat helpt verklaren hoe het enzym hydrofobe moleculen naar het reactieve heemijzercenter kan leiden en tegelijkertijd water en geoxideerde producten laat ontsnappen.
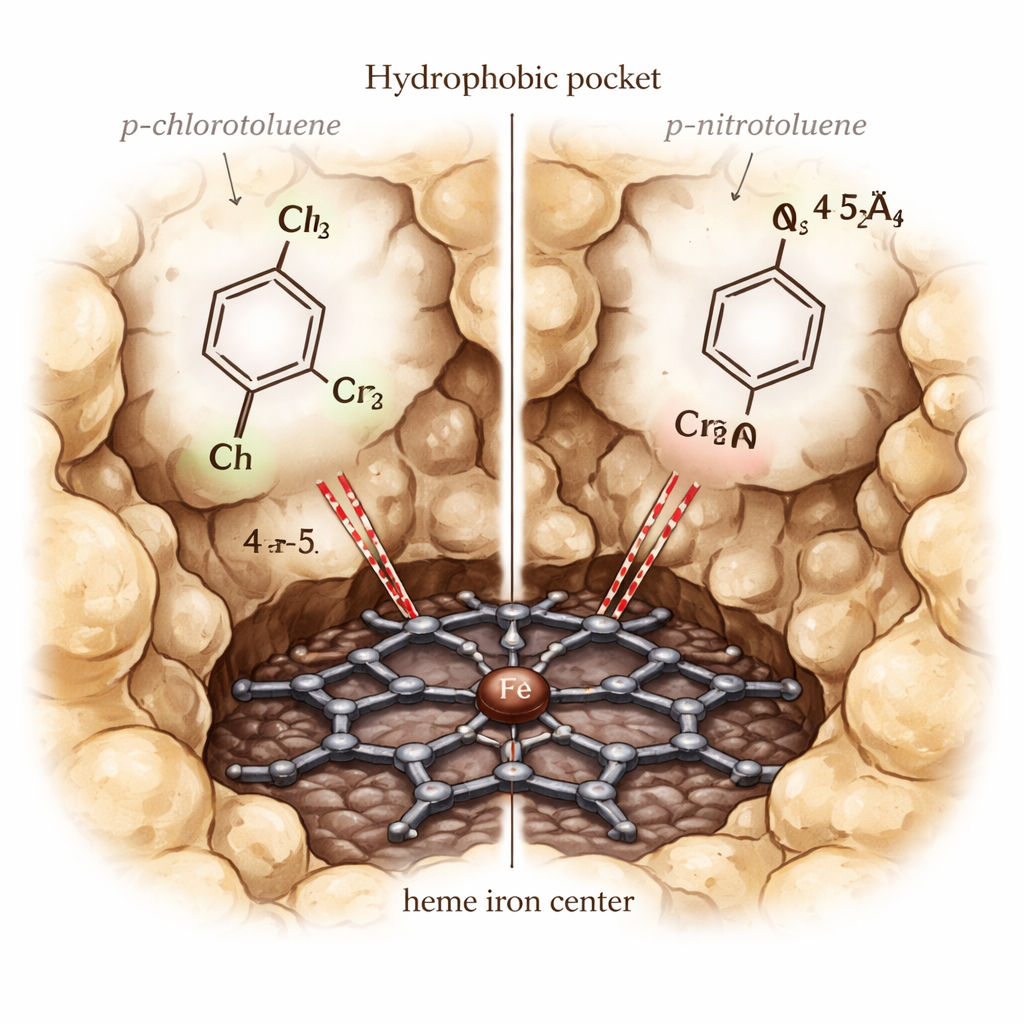
Zien hoe moleculen docken, bewegen en reageren
Met het model konden de auteurs simuleren hoe verschillende tolueenderivaten binden binnen CYP153A6. Ze gebruikten een aanpak genaamd ensemble-docking, waarbij ze vele subtiel verschillende eiwitvormen en meerdere elektronische toestanden van het heemijzer probeerden om te bepalen welke configuraties echte substraten van niet-substraten het beste onderscheiden. Het winnende scenario gebruikte het ijzer in zijn rustende ferrische staat en geen extra watermoleculen in de pocket, en het begunstigde correct bekende substraten. Vervolgsimulaties volgden, frame voor frame, hoe elk molecuul zich ten opzichte van het heem positioneerde. Goede substraten zoals p-cymeen en p-xyleen bleven dicht bij het ijzer met hun benzylïsche methylgroep naar het ijzer gericht, en hun voorspelde bindingsenergieën waren sterk gunstig. Slechte substraten dreven vaak weg, namen ongemakkelijke oriëntaties aan of interageerden ongunstig met de grotendeels olieachtige zijketens die de pocket bekleden.
Waarom de ene look-alike reageert en de andere niet
Één raadsel viel op: p-chloortolueen wordt efficiënt geoxideerd door CYP153A6, terwijl p-nitrotolueen dat niet is, hoewel beide in de pocket passen en in de simulaties vergelijkbaar sterk binden. Om dit te verklaren voerden de auteurs meer gedetailleerde quantummechanica/moleculaire mechanica (QM/MM)-berekeningen uit op de zeer reactieve “Compound I”-toestand van het enzym. Deze berekeningen lieten zien dat de nitrogroep zo veel elektronen dichtheid wegtrekt van het benzylïsche koolstofatoom dat dat veel moeilijker te oxideren is, ondanks dat het geometrisch dicht genoeg ligt. Daarentegen staat de chloorgroep betere elektronische communicatie tussen het heem en het substraat toe, wat zich uit in hogere spindichtheid op de aromatische ring en de methylgroep en een reactiever uitgelijnde toestand voor de kritieke waterstofabstractiestap.
Wat dit betekent voor schonere chemie
Simpel gezegd gedraagt CYP153A6 zich als een klein, olieachtig handschoentje dat bepaalde brandstofachtige moleculen precies zo vasthoudt dat zuurstof op een specifiek punt kan worden toegevoegd—waardoor ze meer in water oplosbaar, nuttiger en uiteindelijk beter afbreekbaar worden. De studie toont dat het enzym apolaire substituenten prefereert en dat zowel vorm als elektronenstroom bepalen of een gegeven tolueenderivaat zal worden getransformeerd. Door te verduidelijken hoe CYP153A6 deze moleculen herkent en activeert, levert het werk een blauwdruk voor het ontwerpen van verbeterde versies die kunnen helpen aromatische verontreinigingen op te ruimen of complexe chemicaliën duurzamer te produceren.
Bronvermelding: Wei, Y., Donzella, S., Foiadelli, S. et al. Structure-based modeling reveals molecular basis for CYP153A6’s novel activity toward toluene derivatives. Sci Rep 16, 7570 (2026). https://doi.org/10.1038/s41598-026-38986-7
Trefwoorden: biokatalyse, cytochroom P450, tolueenhydroxylatie, enzymengineering, groene chemie