Clear Sky Science · nl
De expressie van MALAT1 lange niet-coderende RNA hangt samen met een goede prognose bij mantelcellymfoom
Waarom deze kankerstudie ertoe doet
Mantelcellymfoom is een agressieve vorm van bloedkanker die vaak terugkeert na behandeling en moeilijk onder controle te krijgen kan zijn. Deze studie onderzoekt een weinig bekend type genetisch materiaal, MALAT1, een lang niet‑coderend RNA dat geen eiwitten aanmaakt maar toch invloed kan hebben op het gedrag van cellen. Door meer dan 200 patiënten te volgen, ontdekten de onderzoekers dat hogere niveaus van MALAT1 — en een partnermolecuul genaamd TALAM1 — samenhangen met trager groeiende tumoren en langere overleving. Hun bevindingen kunnen artsen helpen betere voorspellingen te doen en wijzen mogelijk op nieuwe manieren om behandelingen effectiever te maken.
Een verborgen RNA met een verrassende boodschap
De meeste mensen kennen genen die eiwitten coderen, maar ons DNA produceert ook veel lange niet‑coderende RNA’s die meer als managers dan als arbeiders functioneren. MALAT1 is zo’n RNA en heeft aandacht gekregen omdat het in veel kankers veranderd voorkomt. In verschillende solide tumoren is extra MALAT1 gekoppeld aan agressiever ziekteverloop, waardoor velen het zagen als een kankerverwekkend molecuul. De onderzoekers wilden weten of dit ook geldt voor mantelcellymfoom, een B‑celkanker die doorgaans snel groeit en grotendeels ongeneeslijk is. Ze onderzochten ook TALAM1, een natuurlijk “spiegel”transcript van MALAT1 dat helpt MALAT1 te verwerken naar zijn actieve vorm.
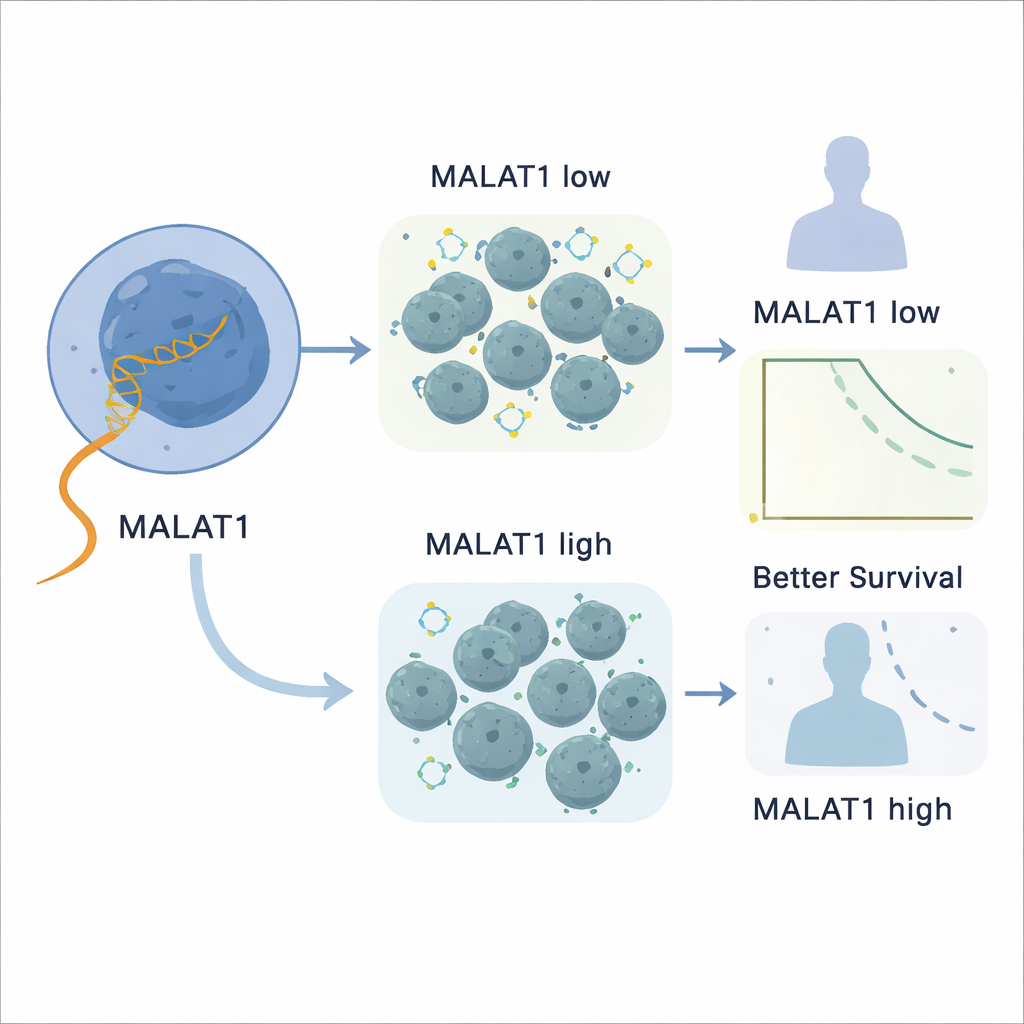
Het volgen van patiëntuitkomsten en tumorgedrag
Het team analyseerde MALAT1‑ en TALAM1‑niveaus in drie onafhankelijke groepen mantelcellymfoompatiënten, samen goed voor 219 primaire tumoren uit lymfeklieren en bloed. Ze vergeleken RNA‑niveaus met klinische gegevens zoals hoe lang patiënten leefden na monsterafname, hoe de tumorcellen er onder de microscoop uitzagen, en of ze bekende hoogrisico‑genetische veranderingen droegen. In twee goed gekarakteriseerde cohorten leefden patiënten wiens tumoren hoge expressie van MALAT1 of TALAM1 hadden significant langer dan degenen met lage niveaus. Dit voordeel trad op in zowel nodale als leukemische vormen van de ziekte en was onafhankelijk van markers zoals SOX11‑status of TP53‑alteraties, wat suggereert dat MALAT1 en TALAM1 aanvullende prognostische informatie geven in plaats van simpelweg andere risicofactoren te spiegelen.
Langzamere groei en stillere signalering
Om te begrijpen waarom hoge MALAT1‑ en TALAM1‑waarden voordelig lijken, bestudeerden de wetenschappers genexpressie‑“handtekeningen” die vastleggen hoe actief bepaalde cellulaire programma’s zijn. In lymfekliersamples gebruikten ze een gevalideerd paneel van 35 genen dat scoret hoe snel mantelcellymfoomcellen prolifereren. Tumoren met hogere MALAT1‑ en TALAM1‑waarden hadden vaak lagere proliferatiescores en groepeerden bij een genengroep die eerder werd gekoppeld aan betere patiëntuitkomsten. In bloedmonsters onderzochten ze een 27‑genenhandtekening voor B‑celreceptorsprikking, een pad dat bij hoge activiteit leidt tot agressiever ziektegedrag. Ook hier hadden gevallen met sterke signalering lagere MALAT1, terwijl die met hogere MALAT1 stillere signaalpatronen vertoonden. Al met al stonden de moleculaire gegevens in lijn met het klinische beeld: meer MALAT1/TALAM1 ging samen met minder agressief tumorgedrag.
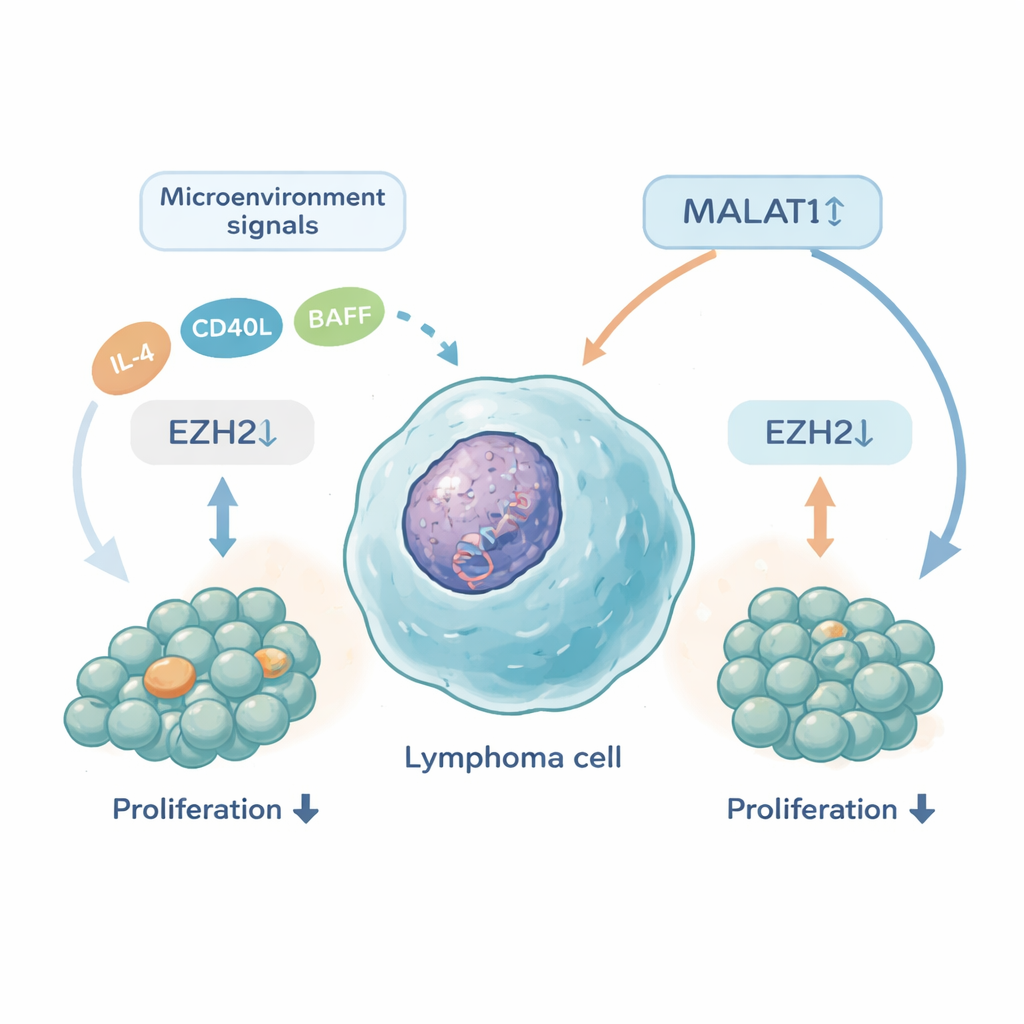
Oorzaak en gevolg testen in 3D‑tumormodellen
Associatie alleen bewijst niet dat MALAT1 het groeigedrag van lymfoomcellen beïnvloedt, dus gingen de onderzoekers over op driedimensionale “sferoïd”culturen gemaakt van de tumorcellen van patiënten. In dit model worden cellen blootgesteld aan groeisignalen en overlevingsfactoren die het micro‑milieu van de lymfeklier nabootsen. Wanneer alleen een overlevingsfactor (BAFF) aanwezig was, vertraagde de celgroei en steeg MALAT1; het toevoegen van sterke groeisignalen (IL‑4 en CD40L) keerde dit patroon om, met meer celdeling en lagere MALAT1. Het team bestudeerde ook EZH2, een epigenetisch enzym dat eerder werd gekoppeld aan slechte prognose. Onder pro‑groeiomstandigheden nam EZH2 toe en daalde MALAT1, terwijl het blokkeren van EZH2‑activiteit met een geneesmiddel MALAT1‑niveaus deed stijgen en celgroei verminderde. Directe onderdrukking van MALAT1 duwde cellen richting meer proliferatie en hogere EZH2, wat het idee versterkt dat MALAT1 in deze context helpt de tumorgroei te remmen in plaats van te stimuleren.
Wat het betekent voor patiënten en toekomstige therapieën
Voor mensen met mantelcellymfoom suggereren deze bevindingen dat het meten van MALAT1 en TALAM1 kan helpen patiënten te onderscheiden wiens ziekte waarschijnlijk rustiger zal verlopen van patiënten met hoger risico, en dat bovenop wat huidige genetische tests laten zien. Algemeen laat het werk zien dat hetzelfde RNA‑molecuul in sommige weefsels als kankerbevorderaar kan werken en in andere als rem, afhankelijk van de omgevingssignalen. Bij mantelcellymfoom lijkt hoge MALAT1 micro‑omgevingsgestuurde groeiprogramma’s en het kankergeassocieerde enzym EZH2 tegen te werken. Hoewel het nog te vroeg is om MALAT1‑gerichte therapieën klinisch toe te passen, zouden strategieën die de activiteit ervan behouden of versterken op termijn bestaande behandelingen kunnen aanvullen en kunnen helpen de krachtige groeisignalen die tumorcellen uit hun omgeving ontvangen, te weerstaan.
Bronvermelding: Fernández-Garnacho, E.M., Martínez-Muñoz, C., Nadeu, F. et al. The expression of MALAT1 long non-coding RNA is associated with good prognosis in mantle cell lymphoma. Sci Rep 16, 7655 (2026). https://doi.org/10.1038/s41598-026-38971-0
Trefwoorden: mantelcellymfoom, MALAT1, lange niet-coderende RNA, EZH2, prognostische biomarker