Clear Sky Science · nl
Transplastomische biofabriek voor de productie van functioneel menselijk α-lactalbumine voor voedings- en therapeutische toepassingen
Planten omvormen tot producenten van melkeiwitten
Moderne diëten zijn sterk afhankelijk van melkeiwitten, maar het grootbrengen van koeien op wereldschaal brengt milieuverliezen en ethische vragen met zich mee. Deze studie verkent een heel andere manier om een belangrijk menselijk melkproteïne te produceren: door plantbladeren te leren het te maken. Het werk laat zien dat tabaksplanten zodanig kunnen worden herschakeld dat ze menselijk α‑lactalbumine produceren, een eiwit dat belangrijk is voor de voeding van zuigelingen en potentieel antikankereigenschappen heeft, wat een weg opent naar diervrije ingrediënten voor zuigelingenvoeding en nieuwe kankerbestrijdende voedingscomponenten.
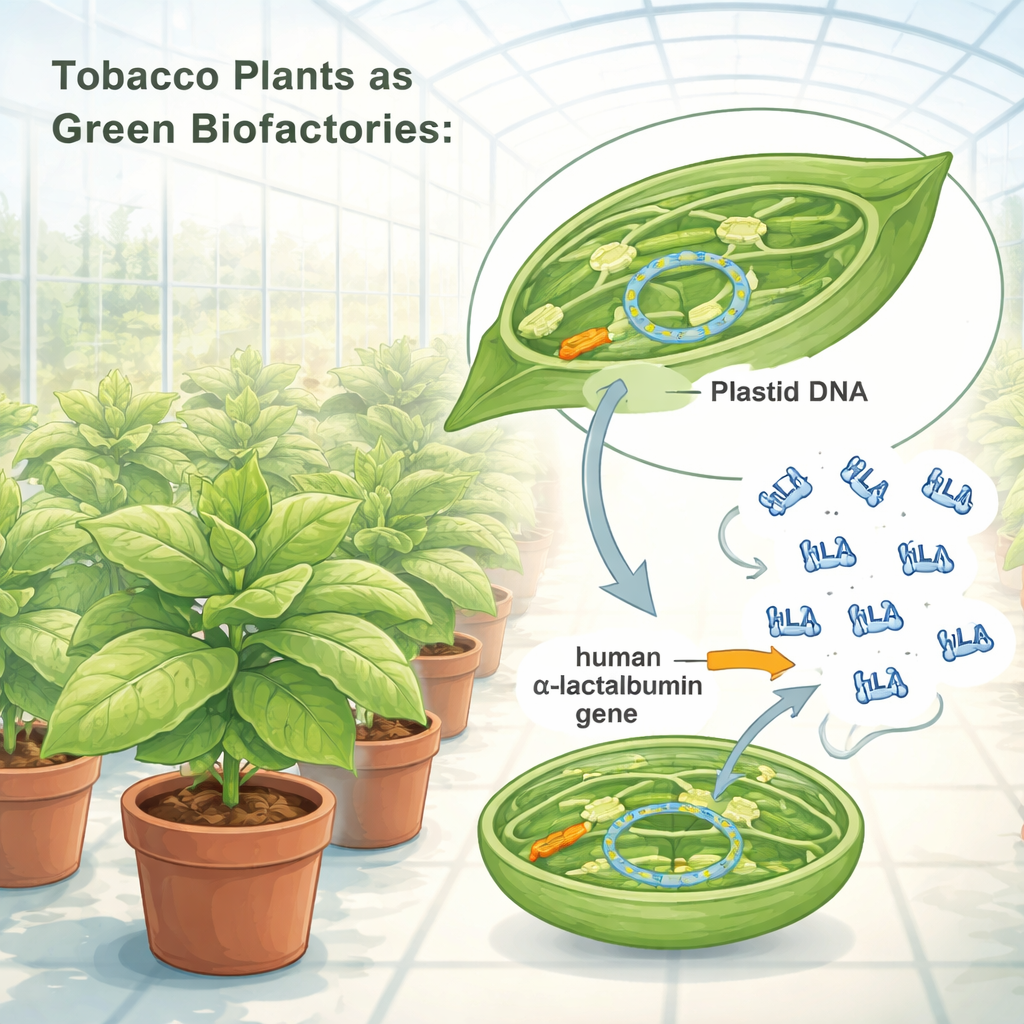
Waarom dit melkeiwit belangrijk is
Moedermelk is meer dan alleen voedsel; het is een fijn afgestelde mix van eiwitten, vetten en suikers die verandert naarmate een zuigeling groeit. Een van de belangrijkste eiwitten is α‑lactalbumine, dat helpt bij de opbouw van lactose, de belangrijkste melksuiker en een cruciale energiebron voor baby’s. α‑Lactalbumine is rijk aan essentiële aminozuren, waaronder tryptofaan, een bouwsteen voor het ‘‘feel‑good’’ hersenchemische serotonine, en wordt in verband gebracht met betere stressbestendigheid en mogelijke bescherming tegen bepaalde vormen van kanker. Omdat het gemakkelijk te verteren is, een milde smaak heeft en stabiel blijft over een breed zuurtegraadbereik, wordt het veel gebruikt in zuigelingenvoeding en nutritionele dranken—en de vraag neemt toe.
Het probleem met traditionele zuivel
Afhankelijkheid van koeien voor melkeiwitten heeft nadelen. Vee draagt aanzienlijk bij aan de wereldwijde uitstoot van broeikasgassen, en grootschalige melkveehouderij vereist grote hoeveelheden land, water en veevoer. Bovendien kunnen bedrijfspraktijken zorgen baren over hormonen, antibiotica en ziekteverwekkers in de melk. Deze druk heeft de interesse aangewakkerd in ‘‘cellulaire landbouw’’-benaderingen, waarbij melkeiwitten worden geproduceerd door microben of gekweekte cellen in plaats van dieren. Veel van die systemen zijn echter nog duur, moeilijk op te schalen of leveren eiwitten die niet precies overeenkomen met de menselijke versies. Planten, met name hun bladchloroplasten—de kleine groene fabriekjes die fotosynthese aandrijven—bieden een veelbelovend alternatief platform.
Chloroplasten herprogrammeren als biofabrieken
De onderzoekers herschreven de genetische instructies voor menselijk α‑lactalbumine zodat tabakschloroplasten ze efficiënt konden aflezen. Ze voegden dit geoptimaliseerde gen in het chloroplast-DNA in, met een ‘‘gencassette’’ opgebouwd uit sterke plantaardige regulatorische elementen die als krachtige aan/uit‑schakelaars werken. Met een particle‑bombardementmethode brachten ze deze cassette in tabaksbladcellen in en selecteerden vervolgens plantjes waarvan de chloroplasten de nieuwe genen volledig hadden overgenomen. Genetische tests bevestigden dat alle kopieën van het chloroplast-DNA in deze planten nu het menselijke eiwit‑blauwdruk droegen. De gewijzigde planten groeiden normaal onder kasomstandigheden, produceerden zaden en toonden geen zichtbare nadelen in grootte, vorm of vruchtbaarheid, wat suggereert dat de extra eiwitbelasting de plantengezondheid niet schaadde.
Aantonen dat het plantaardige eiwit werkt
Vervolgens vroegen de onderzoekers of het plantaardig geproduceerde α‑lactalbumine zich gedroeg als het echte menselijke eiwit. Ze extraheerden oplosbare eiwitten uit de bladeren, zuiverden het α‑lactalbumine en onderzochten de structuur met een techniek die rapporteert hoe eiwitten vouwen. De spectrale ‘‘vingerafdruk’’ van het plantaardige eiwit viel vrijwel samen met die van commercieel menselijk α‑lactalbumine, wat op een vergelijkbare vouwing wijst. Functioneel activeerde het plantaardige eiwit het lactoseproducerende enzym bijna even goed als de native versie en dreef het de lactosevorming aan tot ongeveer 93% van het tempo van het standaardeiwit. Opmerkelijk was dat α‑lactalbumine ophoopte tot ongeveer 23% van alle oplosbare eiwitten in de bladeren—een van de hoogste niveaus gerapporteerd voor menselijke eiwitten geproduceerd in plantchloroplasten—wat suggereert dat dit systeem industriële opbrengsten kan leveren.
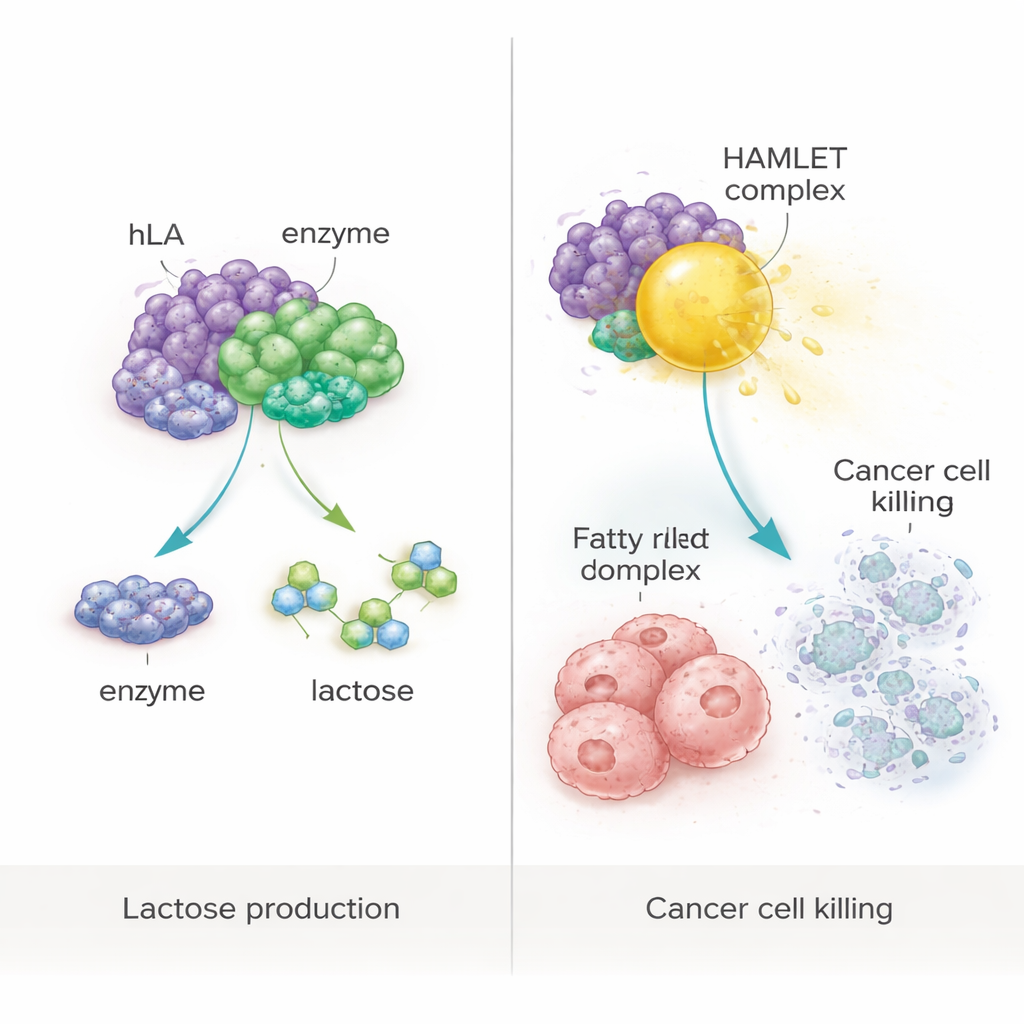
Van voeding naar kankerbestrijdende complexen
De studie testte ook een ambitieuzer idee: het gebruiken van het plantaardige eiwit als bouwsteen voor een bekend antikankercomplex genaamd HAMLET, gevormd wanneer α‑lactalbumine sterk bindt aan oliezuur, een veelvoorkomend vetzuur. Door het gezuiverde plantaardige eiwit zachtjes te verhitten met oliezuur onder gecontroleerde omstandigheden, creëerden de onderzoekers een HAMLET‑achtig complex. Toegepast op menselijke darmkanker (WiDr) en borstkanker (MCF‑7) cellen in kweek, verminderde dit complex de overleving van cellen dramatisch tot onder de 10%. Vervolgonderzoek toonde aan dat de meeste aangetaste cellen apoptose ondergingen, een vorm van geprogrammeerde celdood in plaats van ongecontroleerde ruptuur. Belangrijk is dat noch het eiwit alleen, noch het vetzuur alleen, noch extracten van niet‑gewijzigde planten significante celdood veroorzaakten, wat bevestigt dat het kanker‑dodend effect afhankelijk was van het specifieke complex.
Wat dit kan betekenen voor toekomstige voeding en medicijnen
Gezamenlijk tonen de resultaten aan dat plantchloroplasten betrouwbaar grote hoeveelheden van een menselijk melkeiwit kunnen produceren dat zowel voedingskundig relevant als therapeutisch actief is. Voor leken betekent dit dat toekomstige zuigelingenvoedingen, functionele voedingsmiddelen of supplementen mogelijk gemaakt kunnen worden met eiwitten geteeld in bladeren in plaats van gewonnen uit koeien, waarmee de milieu-impact vermindert terwijl de biologische overeenstemming met de mens verbetert. Tegelijkertijd kan datzelfde plantaardige eiwit in het laboratorium worden omgezet in een gericht antikankercomplex, wat wijst op plantaardige productieketens voor betaalbare biotherapeutica. Hoewel verder onderzoek nodig is om veiligheid en werkzaamheid bij dieren en mensen te bevestigen—en om deze technologie over te zetten naar eetbare gewassen—biedt de studie een overtuigende blik op planten als mini‑fabrieken voor de volgende generatie voeding en geneeskunde.
Bronvermelding: Ehsasatvatan, M., Kohnehrouz, B.B. Transplastomic biofactory for the production of functional human α-lactalbumin for nutritional and therapeutic applications. Sci Rep 16, 7359 (2026). https://doi.org/10.1038/s41598-026-38965-y
Trefwoorden: melkeiwitten gemaakt in planten, chloroplast biofabriek, menselijk alpha-lactalbumine, duurzame zuivelalternatieven, HAMLET kankertherapie