Clear Sky Science · nl
Integrine αv draagt bij aan de regulatie van de stijfheid van vasculaire gladde spiercellen
Waarom de “veerachtigheid” van een slagader belangrijk is
Na verloop van tijd of bij hoge bloeddruk verliezen onze grote slagaders geleidelijk hun natuurlijke veerkracht en worden ze stijver. Deze verandering dwingt het hart harder te werken en vergroot het risico op hartaanvallen, beroertes en andere cardiovasculaire problemen. Wetenschappers weten al lange tijd dat de materialen waaruit de vaatwand is opgebouwd — eiwitten zoals elastine en collageen — de stijfheid beïnvloeden. Deze studie stelt een subtielere vraag: kunnen de spiercellen in de vaatwand zelf stijver worden, en draagt een kleine familie van oppervlaktereceptoren, integrine αv, eraan bij dat die cellen, en daarmee onze slagaders, flexibeler blijven?
De spiercellen die de bloedstroom vormgeven
Grote slagaders zijn niet zomaar passieve buizen. Hun middelste laag bevat veel vasculaire gladde spiercellen die kunnen samentrekken en ontspannen om de bloedstroom en de druk fijn af te stemmen. Deze cellen zijn verankerd aan een omringend geraamte, het extracellulaire matrix. De onderzoekers concentreerden zich op een groep verankeringsmoleculen, integrine αv, die het celoppervlak overspant en het interne skelet van de cel fysiek koppelt aan dat externe geraamte. Vroegere studies suggereerden dat integrine αv betrokken is bij littekenvorming en hermodellering van bloedvaten, maar het was onduidelijk of het ook reguleert hoe stijf de spiercellen zelf worden, vooral onder de invloed van hormonen zoals angiotensine II die de bloeddruk verhogen en fibrose bevorderen.
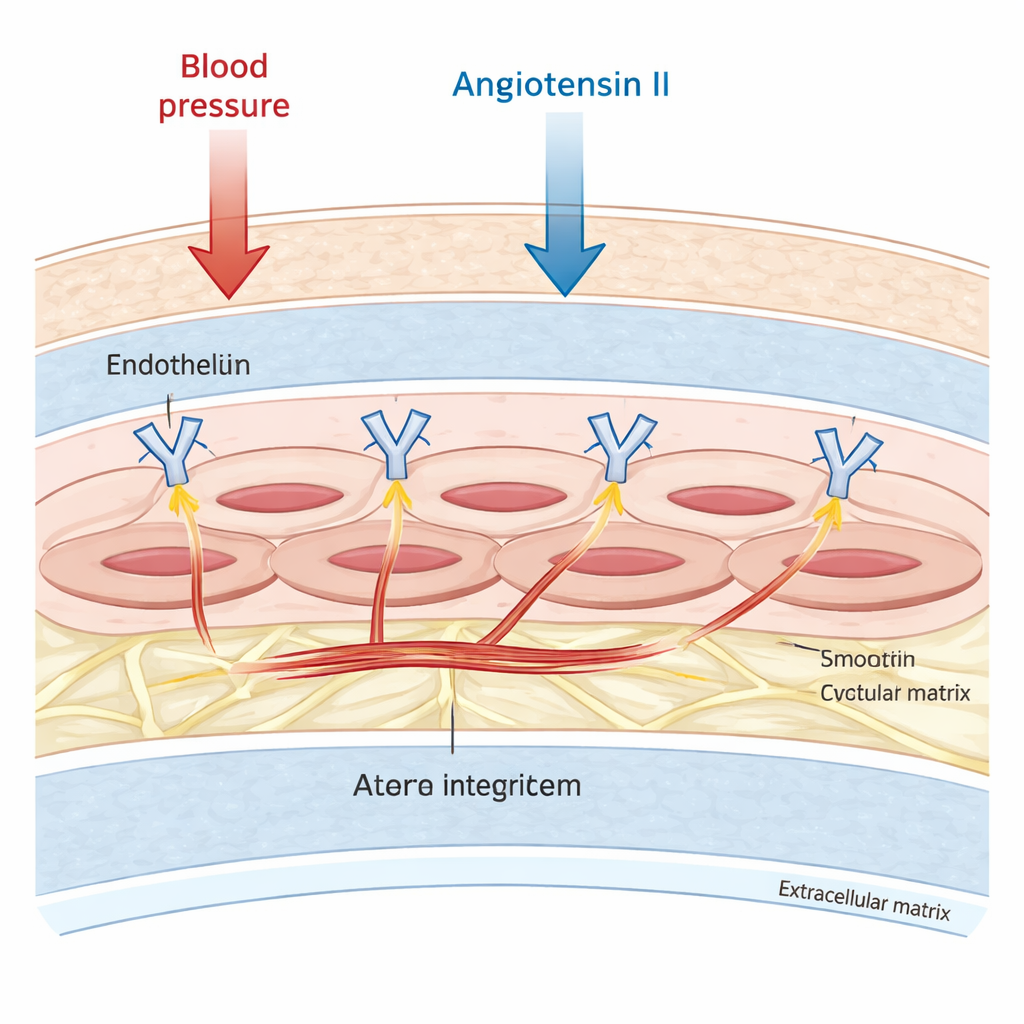
Stijfheid meten, cel voor cel
Om dit te onderzoeken gebruikten het team muisgladde spiercellen gekweekt in het laboratorium en muizen die zodanig waren gemodificeerd dat ze geen integrine αv in hun vasculaire spiercellen hadden. Ze bepaalden de stijfheid van cellen met atomic force microscopy, een techniek waarbij een ultrafijne punt zachtjes in het celoppervlak drukt en registreert hoeveel kracht daarvoor nodig is. Cellen zonder integrine αv waren onder rustige omstandigheden meer dan twee keer zo stijf als controles. Na blootstelling aan angiotensine II gedurende twee dagen werden deze deficientie‑cellen ongeveer drie keer zo stijf, terwijl normale cellen nauwelijks veranderden. Omdat hun metingen zeer oppervlakkige indringing gebruikten, bouwden de auteurs een gedetailleerd computermodel van een gladde spiercel en simuleerden ze dieper prikken. De simulaties lieten zien dat oppervlakkige tests het aandeel van de buitenste schil en de corticale regio van de cel benadrukken, en nog binnen het bereik vielen van de stijve mutantcellen, wat de biologische bevindingen ondersteunt.
Een hervormd intern skelet
De volgende stap was de binnenkant van de cellen te bekijken. Met fluorescente kleurstoffen en microscopie onderzochten de onderzoekers actine, een belangrijk filament dat het interne geraamte van de cel vormt. Controle‑gladde spiercellen toonden een relatief diffus actinenetwerk, zelfs na behandeling met angiotensine II. Cellen zonder integrine αv daarentegen vormden dikke stressvezels die de cel doorkruisten en, na blootstelling aan het hormoon, een intense band van actine net onder het celmembraan — bekend als corticaal actine. Een kwantitatieve maat voor hoeveel actine zich bij de rand van de cel ophoopte bevestigde dat deze corticale laag sterk verrijkt was alleen in de integrine‑deficiënte cellen. Deze cellen ontwikkelden ook ongewoon lange adhesiestructuren waar ze zich aan de omringende matrix vastgrijpen, wat overeenkomt met een overgang naar meer spanningsdragende, fibrillaire adhesies die de cel in een stijve toestand kunnen vergrendelen.
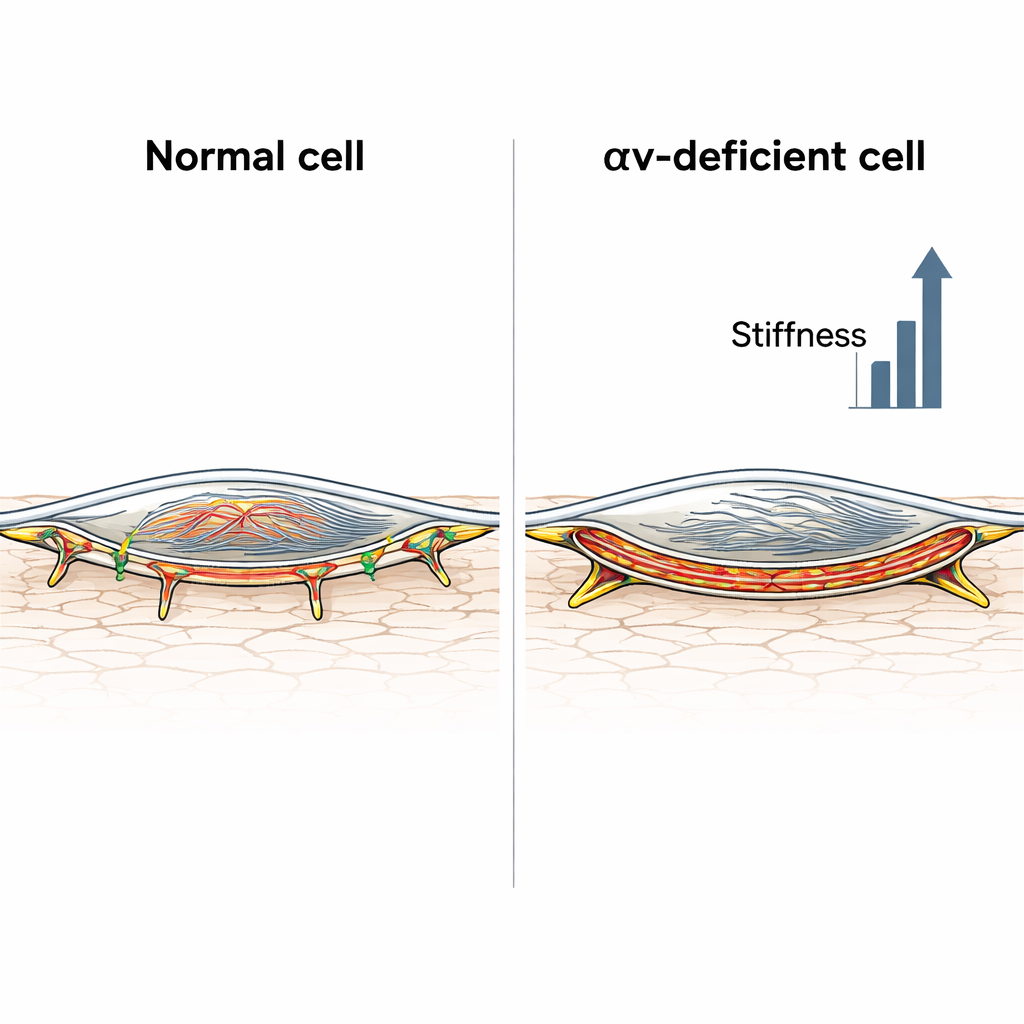
Wanneer de wand er hetzelfde uitziet maar anders gedraagt
Aangezien slagaders meer zijn dan alleen hun spiercellen, maten de wetenschappers ook mechanische eigenschappen van de halsslagaders in levende muizen, zowel met als zonder integrine αv in hun vasculaire spiercellen, en met of zonder chronische toediening van angiotensine II. Verrassend genoeg waren de algehele arteriële druk en wandstijfheid — afgeleid uit echografie‑gebaseerde druk‑diametercurven — vergelijkbaar in beide muizenstammen, zowel in rust als na hormoonbehandeling. Toch verschilden de microscopische samenstelling van de wand. Onder angiotensine II lieten controlemuizen minder elastine en meer collageen zien, klassieke tekenen van een stijver matrix, terwijl integrine‑deficiënte muizen relatief minder collageenverandering hadden maar veel stijvere spiercellen. Met andere woorden: bij normale muizen deed de matrix het grootste deel van de verharding; bij integrine‑deficiënte muizen werden de spiercellen zelf zo rigide dat ze de meer bescheiden matrixveranderingen effectief compenseerden.
Wat dit betekent voor verouderende slagaders
Voor leken is de kernboodschap dat arteriële stijfheid niet alleen te maken heeft met versleten elastische vezels; het hangt ook af van hoe de spiercellen in de wand hun kleine interne kabels organiseren. Integrine αv helpt normaal gesproken te voorkomen dat deze cellen te stijf worden wanneer ze uitgedaagd worden door hormonen zoals angiotensine II. Wanneer deze rem ontbreekt, herschikken de cellen hun actineskelet — vooral de cortex net onder het membraan — en vergrendelen ze in een stijvere toestand die de arteriële verharding kan aansturen, zelfs zonder dramatische veranderingen in het omringende materiaal. Deze bevinding wijst op nieuwe behandelideeën: geneesmiddelen die het corticale actinenetwerk voorzichtig versoepelen of reorganiseren, of die integrine‑gekoppelde signaalroutes moduleren, zouden op termijn een aanvulling kunnen vormen op bloeddrukverlagende therapieën om de “veer” van verouderende slagaders directer te herstellen.
Bronvermelding: Bascetin, R., Belozertseva, E., Regnault, V. et al. Integrin αv contributes to the regulation of vascular smooth muscle cell stiffness. Sci Rep 16, 7682 (2026). https://doi.org/10.1038/s41598-026-38948-z
Trefwoorden: arteriële stijfheid, vasculaire gladde spiercellen, integrine alpha v, actine-cytoskelet, angiotensine II