Clear Sky Science · nl
Microbioom in de darm en metabole routeprofielen bij geïnfecteerde en niet-geïnfecteerde harttransplantatiepatiënten voor en na de operatie
Waarom je darm ertoe doet na een nieuw hart
Harttransplantatie kan mensen met ernstig hartfalen een tweede kans op leven bieden, maar infecties in de weken na de operatie blijven een groot risico. Deze studie stelt een ogenschijnlijk eenvoudige vraag met belangrijke implicaties: hoe verandert de gemeenschap van microben in onze darmen rond het moment van harttransplantatie, en kunnen die veranderingen helpen verklaren wie geïnfecteerd raakt en wie niet?
Het kleine ecosysteem in transplantatiepatiënten
Onze darmen herbergen biljoenen bacteriën die helpen voedsel te verteren, het immuunsysteem trainen en binnendringende ziekteverwekkers op afstand houden. Chirurgie, sterke immuunsuppressieve medicijnen en breedspectrumantibiotica kunnen dit fragiele ecosysteem flink verstoren. Om te volgen wat er gebeurt bij harttransplantatiepatiënten, volgden onderzoekers in China 20 volwassenen die donorharten ontvingen. Ze verzamelden stoelgangmonsters ongeveer een week voor de operatie en opnieuw 30 dagen erna, en gebruikten DNA-sequencing om te inventariseren welke bacteriën aanwezig waren en computertools om te voorspellen welke metabole activiteiten die microben mogelijk uitvoeren.
Vier patiëntengroepen, vier microbiële patronen
Het team verdeelde patiënten in vier groepen: met en zonder infecties vóór de operatie, en met en zonder infecties in de eerste maand na de operatie. Voor de transplantatie leken de algemene diversiteit en structuur van het darmmicrobioom verrassend vergelijkbaar, ongeacht of patiënten al een infectie hadden. Mensen zonder vooroperatieve infecties werden vooral gekoloniseerd door een bekend geslacht genaamd Bacteroides, vaak geassocieerd met een stabiele darmgezondheid. Daarentegen lieten geïnfecteerde patiënten een mix zien waarin mogelijk schadelijke Enterococcus casseliflavus voorkwam naast bacteriën die vaak als vriendelijk worden gezien, zoals Limosilactobacillus en Weissella cibaria, wat wijst op een darmgemeenschap in een delicate, verschuivende balans.
Na de operatie: een splitsing in de microbiële route
30 dagen na de ingreep vertoonde het microbioom van patiënten die infecties wisten te vermijden één herkenbaar patroon, terwijl diegenen die infecties ontwikkelden er heel anders uitzagen. Niet-geïnfecteerde patiënten hadden rijkere, meer evenwichtige microbiële gemeenschappen, met veel leden van het geslacht Blautia en verwante bacteriën die butyraat produceren, een korteketenvetzuur dat bekendstaat om het voeden van darmcellen en het ondersteunen van immuunstabiliteit. Hun darmecosystemen leken divers en in balans. Bij patiënten die infecties kregen, daalde de diversiteit echter en werd de gemeenschap gedomineerd door Enterococcus faecium, een taaie bacterie die vaak bij ziekenhuisinfecties wordt aangetroffen en bekendstaat om antibioticaresistentie. Statistische analyses lieten zien dat het microbioom van deze geïnfecteerde groep apart clusterde van alle anderen, wat wijst op duidelijke postoperatieve microbiële verstoring, of dysbiose.
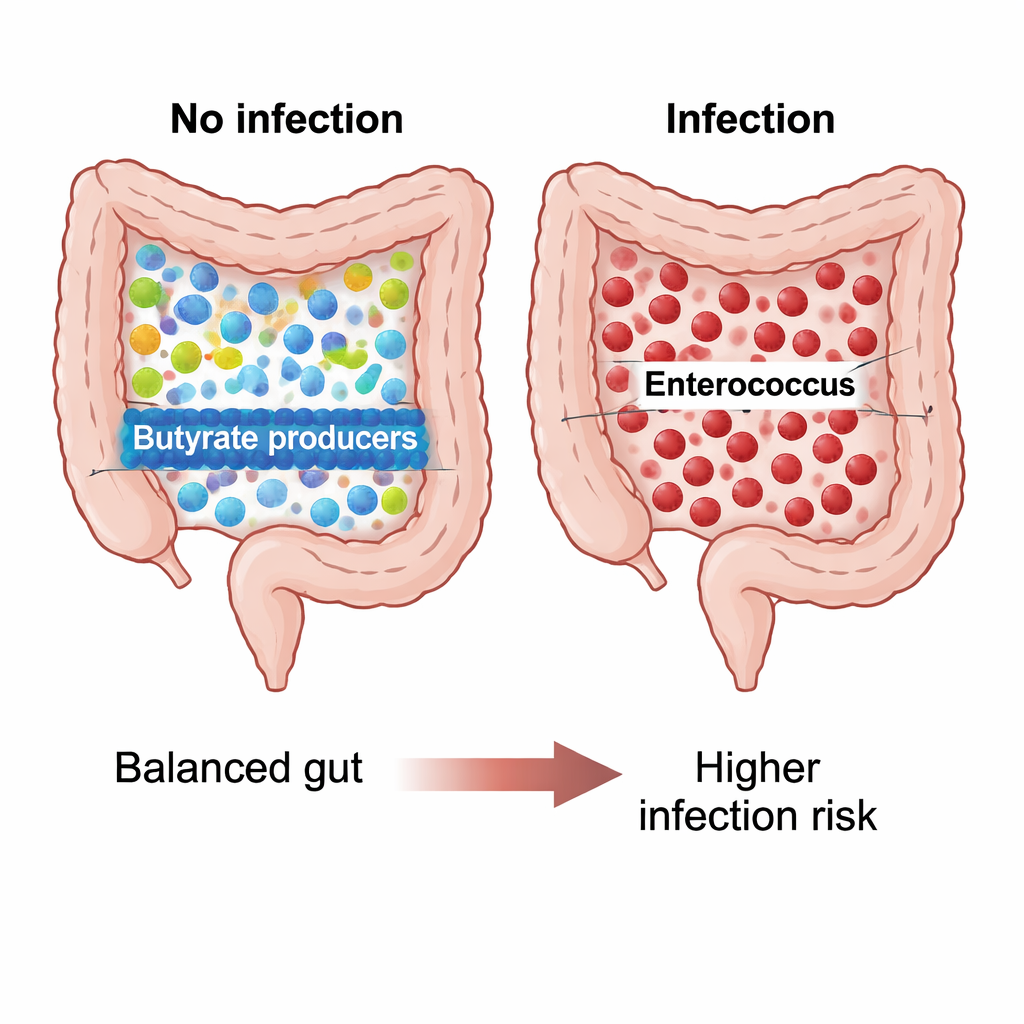
Microbiële chemie gekoppeld aan bescherming of risico
De onderzoekers onderzochten ook welke chemische taken deze microben mogelijk uitvoeren. Met voorspellende software vonden ze dat bij de niet-geïnfecteerde, postoperatieve groep Blautia gekoppeld was aan routes die een verbinding afbreken genaamd L-1,2-propaanediol, een tussenproduct in de fermentatie van vezels dat uiteindelijk de productie van gunstige vetzuren zoals propionaat voedt. Bij geïnfecteerde patiënten was dit voorspelde metabole potentieel aanzienlijk lager, wat overeenkomt met een darmgemeenschap die minder in staat is beschermende moleculen te maken. Voor de operatie werd Enterococcus casseliflavus bij geïnfecteerde patiënten in verband gebracht met ongebruikelijke fermentatieroutes die kunnen wijzen op een gestreste, energiehongerige microbieële omgeving, hoewel dit directe laboratoriumbevestiging vereist.
Wat dit betekent voor patiënten en zorgteams
Voor mensen die een harttransplantatie tegemoet gaan, suggereren deze bevindingen dat de darm niet slechts een toeschouwer is; ze kan helpen het risico op gevaarlijke infecties te beïnvloeden. De studie wijst op een dynamische verschuiving van Bacteroides-dominantie vóór de operatie naar ofwel beschermende verrijking van Blautia of schadelijke overgroei van Enterococcus daarna, afhankelijk van hoe de vroege herstelperiode verloopt. Zware infectiegerelateerde stress en antibioticagebruik lijken de darmgemeenschap te duwen naar de Enterococcus-gedomineerde, laag-diverse toestand die bij geïnfecteerde patiënten is waargenomen. De auteurs stellen een "tweevoudige" strategie voor: het ondersteunen van het herstel van butyraat-producerende bacteriën — mogelijk door dieet of zorgvuldig gekozen probiotica — terwijl Enterococcus-niveaus nauwgezet worden gevolgd. Hoewel grotere en langere studies nodig zijn, opent dit werk de deur naar toekomstige transplantatiezorg waarin het afstemmen van het darmmicrobioom een routineonderdeel wordt van het beschermen van patiënten tegen levensbedreigende infecties.
Bronvermelding: Han, J., Hua, L., Yang, B. et al. Gut microbiota and metabolic pathway profiles in infected and non-infected heart transplant patients before and after surgery. Sci Rep 16, 7697 (2026). https://doi.org/10.1038/s41598-026-38911-y
Trefwoorden: harttransplantatie, darmmicrobioom, postoperatieve infectie, antibiotica, butyraat-producerende bacteriën