Clear Sky Science · nl
Verbeterde kinetische prestaties en stabiliteit van katalase geïmmobiliseerd op epoxy-gefunctionaliseerde kaolieniet
Een natuurlijke klei omvormen tot een slimme reiniger
Waterstofperoxide wordt veel gebruikt om te desinfecteren, bleken en water te behandelen, maar achtergebleven peroxide in industriële afvalstromen kan levende cellen en het milieu schaden. De natuur biedt al een krachtige opruimoplossing: het enzym katalase, dat waterstofperoxide omzet in onschadelijk water en zuurstof. Vrije enzymen zijn echter kwetsbaar en moeilijk herbruikbaar. Deze studie laat zien hoe een veelvoorkomend kleimineraal, kaolieniet, zacht kan worden aangepast zodat katalase er sterk aan hecht en zo een steviger, herbruikbaar "opruimoppervlak" wordt dat industriële processen en afvalwaterzuivering veiliger en duurzamer zou kunnen maken. 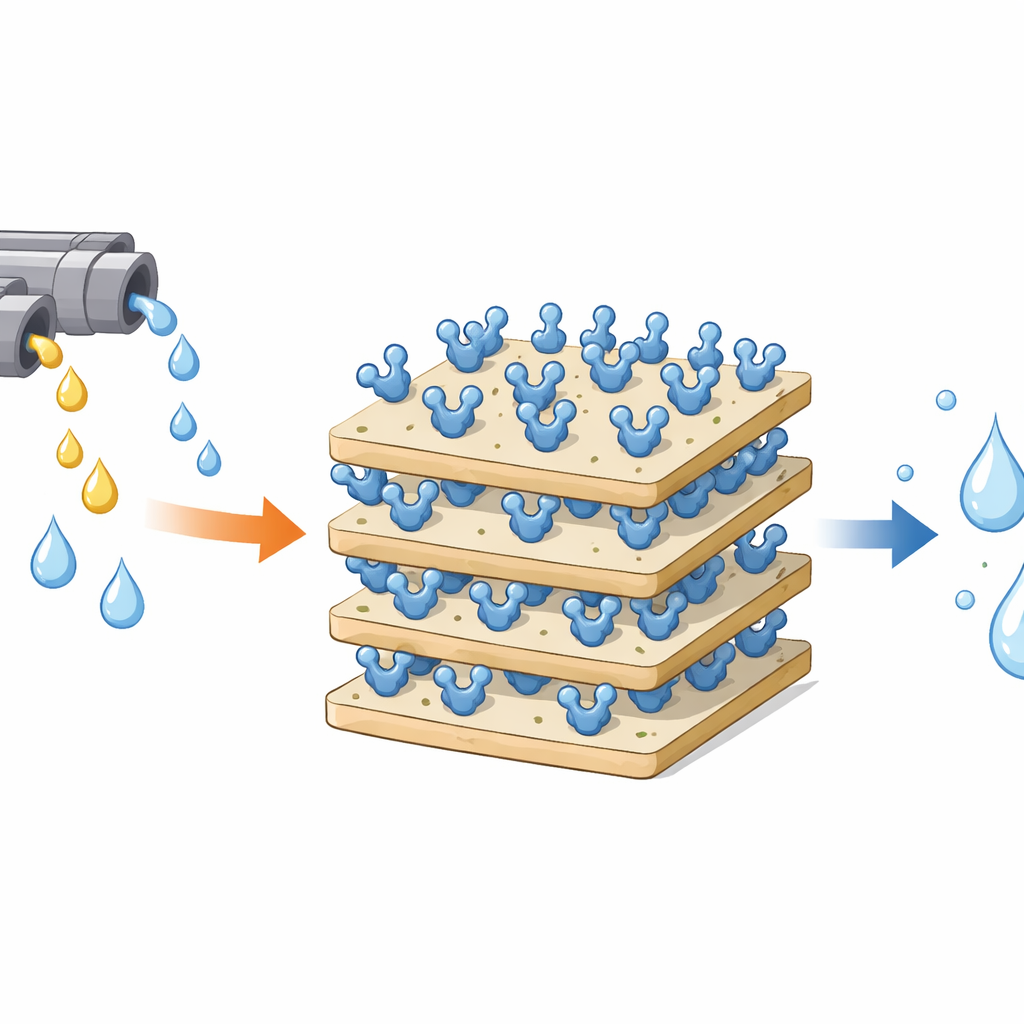
Een veelvoorkomend mineraal met verborgen potentieel
Kaolieniet is een goedkope, ruim beschikbare witte klei die wordt gebruikt in papier, keramiek en zelfs geneeskunde. Het heeft een gelaagde structuur die mechanisch sterk en chemisch stabiel is, maar het oppervlak is relatief inert, waardoor enzymen er niet goed aan hechten en gemakkelijk weggespoeld worden. Eerdere pogingen om katalase op onbehandelde kaolieniet vast te houden berustten grotendeels op zwakke aantrekkingskrachten. Deze systemen konden wat enzym opnemen maar leden aan lage belading, gemakkelijk uitlogen en verlies van activiteit in de loop van de tijd. De onderzoekers redeneerden dat als ze meer reactieve plaatsen op kaolieniet konden introduceren zonder de structuur te vernietigen, de klei als een robuust, duurzaam platform voor katalase zou kunnen dienen.
Een kleverige maar zachte coating toevoegen
Om kaolieniet te verbeteren, bedekten de onderzoekers het oppervlak met een klein molecuul genaamd GPTMS, een type silaan met een epoxygroep. In water-alcoholmengsels onder licht zure omstandigheden zet GPTMS eerst om in silanolgroepen die aan de natuurlijke hydroxylgroepen van de klei kunnen binden en zo een dunne, duurzame organische laag vormen. De epoxy-delen blijven intact en steken als kleine reactieve ringen uit het oppervlak. Een reeks technieken bevestigde deze transformatie: infraroodspectra toonden nieuwe koolstof–waterstof- en epoxy-gerelateerde vibraties; elektronenmicroscoopbeelden lieten zien dat de oorspronkelijk compacte plaatachtige klei opener en poreuzer werd; thermische analyse detecteerde extra massaverlies bij matige temperaturen door de nieuw aangebrachte organische laag; en oppervlakspectroscopie toonde veel meer koolstof op de gemodificeerde klei terwijl het onderliggende mineraalkader behouden bleef.
Het enzym aanmeren op de klei
Wanneer katalase werd gemengd met deze epoxy-dragende kaolieniet, hechtte het enzym zich snel aan het oppervlak. Binnen het eerste uur waren de meeste bindingsplaatsen al bezet en na ongeveer vier uur was er in wezen evenwicht bereikt. De gemodificeerde klei kon ongeveer 300 milligram katalase per gram drager vasthouden—veel meer dan eerdere systemen op basis van kaolieniet. Het team ontdekte dat neutrale pH en gematigde temperaturen (rond kamertemperatuur tot lichaamstemperatuur) het beste waren voor belading, wat een balans weerspiegelt tussen enzymstabiliteit en de reactiviteit van aminogroepen op het eiwit met de epoxyringen op het oppervlak. Op moleculair niveau vallen nucleofiele groepen op katalase de gespannen epoxyringen aan en vormen meerdere sterke bindingen. Deze meervoudige aanhechting beperkt schadelijke bewegingen terwijl het actieve centrum toegankelijk blijft. 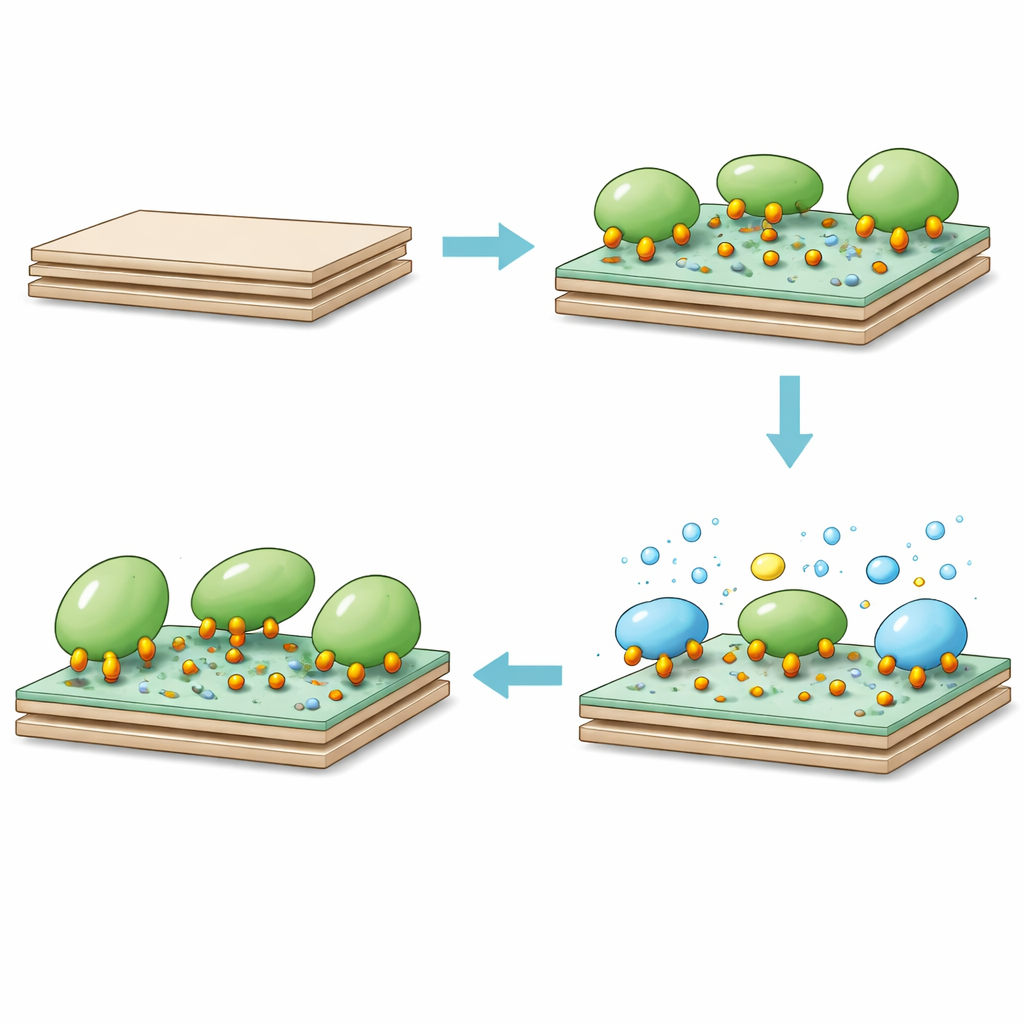
Snel, robuust en langdurig werkzaam
Het vastzetten van katalase op de gemodificeerde klei veranderde de manier waarop het enzym op waterstofperoxide reageerde. Het geïmmobiliseerde enzym vertoonde een veel lagere schijnbare "vraag" naar substraat dan het vrije enzym, wat betekent dat het efficiënt kan werken zelfs wanneer de peroxideconcentraties bescheiden zijn. Hoewel de maximale reactiesnelheid enigszins daalde—waarschijnlijk omdat diffusie door de vaste laag en verminderde flexibiliteit van het enzym het proces vertragen—stegen de algehele katalytische efficiëntie met ongeveer 80 procent. Even belangrijk was dat de geïmmobiliseerde katalase herhaald gebruik en langdurige opslag veel beter doorstond dan de vrije vorm. Het behield hoge activiteit na vele reactierondes en hield een veel groter deel van zijn initiële vermogen over na weken in koude opslag. De kleidrager zelf kon ook worden geregenereerd en meerdere keren opnieuw worden beladen met enzym met slechts geleidelijk verlies van capaciteit.
Waarom dit van belang is voor het dagelijks leven
In eenvoudige bewoordingen verandert de studie een bekende, goedkope klei in een slim, herbruikbaar houder voor een natuurlijk ontgiftend enzym. Door het oppervlak van de klei zorgvuldig te ontwerpen met een dun epoxy-rijke laag, creëerden de onderzoekers een platform dat katalase stevig vastgrijpt, helpt het zijn doel gemakkelijker te herkennen en het beschermt tegen beschadiging. Dit betekent dat we mogelijk peroxidebelaste industriële stromen kunnen reinigen, geavanceerde oxidatieprocessen kunnen ondersteunen of veiligere behandelingen in voedsel- en farmaceutische toepassingen kunnen ontwerpen met kleinere hoeveelheden enzymen over langere perioden. Het werk laat zien hoe het afstemmen van de interface tussen mineralen en eiwitten nieuwe, duurzame tools voor groenere technologieën kan ontsluiten.
Bronvermelding: Erol, K., Veyisoğlu, A., Tatar, D. et al. Enhanced kinetic performance and stability of catalase immobilized on epoxy-functionalized kaolinite. Sci Rep 16, 8196 (2026). https://doi.org/10.1038/s41598-026-38910-z
Trefwoorden: enzymimmobilisatie, katalase, kaolienietklei, rioolwaterzuivering, epoxy-functioneel oppervlak