Clear Sky Science · nl
Evaluatie van de evolutionaire relatie van het TATA-bindend eiwit (TBP) met verschillende vouwingpatronen van proteïnedomeinen met behulp van support vector machine (SVM)
Hoe een DNA "aan"-schakelaar-eiwit verbinding maakt met veel anderen
Het TATA-box bindende eiwit, of TBP, is een werkpaard van onze cellen: het helpt genen aanzetten door DNA vast te pakken bij veel promotoren. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote consequenties: bestaan er andere eiwitten met heel andere taken die stilletjes hetzelfde onderliggende vormpatroon als TBP delen? Door 3D-structuurvergelijking, sequentieanalyse en moderne machine-learningtools te combineren, traceren de auteurs verborgen familierelaties tussen TBP en eiwitten die betrokken zijn bij stofwisseling, neurotransmittersynthese en zelfs kankergerelateerde routes.
Een sleuteleiwit in het hart van genregulatie
TBP zit aan de toegangspoort van genexpressie in organismen van gist tot mens. Het herkent een korte DNA-sequentie die de TATA-box heet en buigt het DNA om te helpen bij de assemblage van het grote transcriptieapparaat dat genen naar RNA kopieert. Omdat deze stap zo centraal is, is de vouwing — de driedimensionale ordening — van het TBP-kerngebied sterk geconserveerd gedurende de evolutie. De auteurs concentreren zich op een goed bestudeerde TBP-structuur bekend als 1tba en gebruiken die als sonde om naar andere eiwitten te zoeken die mogelijk hetzelfde architectonische blauwdruk delen, zelfs als hun aminozuursequenties en dagelijkse functies op het eerste gezicht heel verschillend lijken.
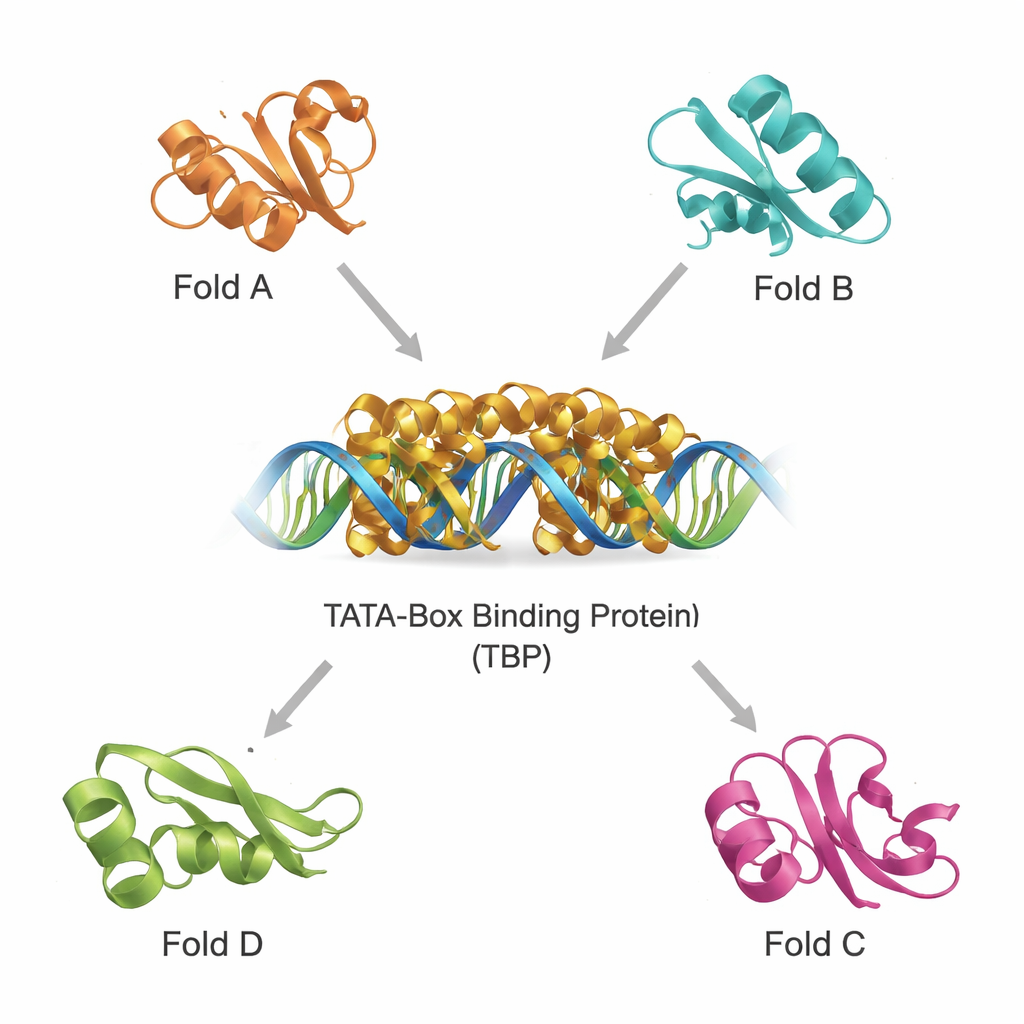
Structurele verwanten vinden in een druk eiwituniversum
Moderne databases bevatten honderden duizenden eiwitstructuren, waardoor het mogelijk is verre verwanten op te sporen op basis van 3D-vorm in plaats van alleen sequentie. Met twee krachtige tools, DALI en TOP-search, haalde het team eerst eiwitten naar voren waarvan de vouwingen op die van TBP leken. Daarna classificeerden ze deze kandidaten met een evolutionaire domeincatalogus en beperkten ze de selectie tot een kleine set structureel gelijkaardige maar functioneel diverse voorbeelden. Daartoe behoren een glutamine-producerend enzym dat belangrijk is in de stofwisseling, een domein dat voorkomt in meerdere tRNA-verwerkende enzymen, een enzym met een kenmerkende "hot-dog" vouwing betrokken bij vetzuurchemie, en eiwitten die helpen bij de aanmaak van tetrahydrobiopterine, een molecuul cruciaal voor hersenfunctie. Het op elkaar plaatsen van hun structuren op TBP liet zien dat ze, ondanks verschillende taken, herkenbare kernmotieven delen.
Machines leren verborgen eiwitfamilies te herkennen
Om verder te gaan dan individuele inspectie, bouwden de auteurs machine-learningmodellen die automatisch TBP-achtige vouwingen konden signaleren. Ze stelden grote verzamelingen eiwitsequenties samen die bekend zijn als behorend tot TBP of tot elk van de gerelateerde vouwingen, samen met een brede "achtergrond"set van niet-gerelateerde eiwitten. Elk eiwit werd omgezet in eenvoudige numerieke samenvattingen: hoe vaak elk aminozuur voorkomt en hoe vaak elk mogelijk paar aminozuren in de sequentie voorkomt. Deze profielen voedden support vector machines (SVMs) en random-forestmodellen, die leerden om één vouwingstype van alle anderen te scheiden. Met strikte cross-validatie bereikten de modellen zeer hoge nauwkeurigheid — vaak boven de 95 procent — zelfs wanneer ze alleen op delen van de sequenties werden getraind die overeenkomen met geconserveerde regio's.
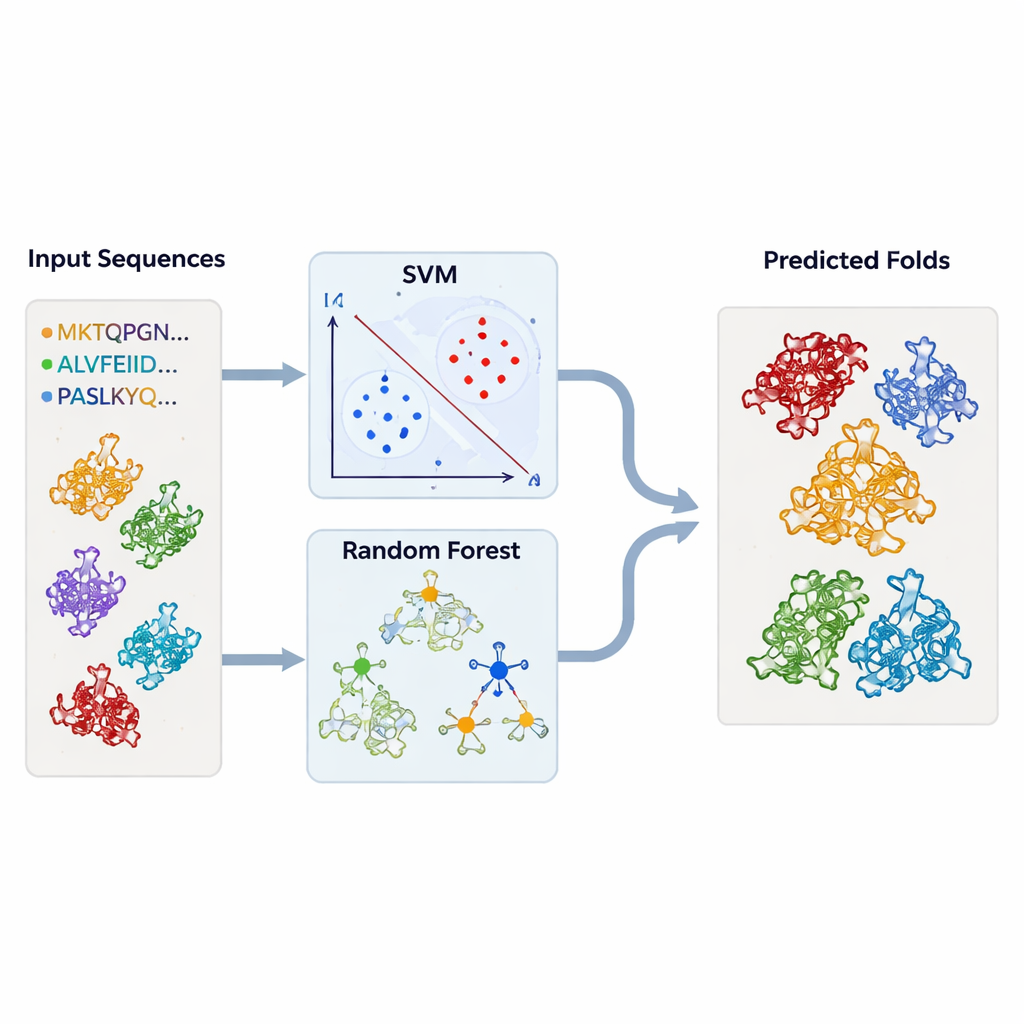
De modellen testen op duizenden onbekende structuren
Gewapend met deze getrainde classificeerders keerde het team terug naar de structurele databases. Ze voerden duizenden eiwitketens — opgehaald uit DALI en TOP-search — door hun modellen om te zien welke de statistische kenmerken van TBP-achtige of verwante vouwingen droegen. De SVM- en random-forestbenaderingen kwamen grotendeels overeen en selecteerden vele kandidaten die ook door structurele tools als vergelijkbaar waren aangewezen. In sommige gevallen groepeerden enzymen met ogenschijnlijk ongerelateerde activiteiten toch sterk met TBP of met elkaar, wat het idee versterkt dat evolutie hetzelfde onderliggende raamwerk kan herbestemmen voor veel verschillende biochemische rollen.
Waarom deze verborgen verbanden ertoe doen
De studie concludeert dat TBP diepe structurele verwantschap deelt met meerdere enzymfamilies, waaronder glutamine-synthetase-achtige eiwitten en editiedomeinen van tRNA-verwerkende enzymen. Zelfs wanneer sequenties zijn afgedreven en functies zijn gediversifieerd, behouden deze eiwitten gemeenschappelijke architectonische motieven, wat wijst op afstamming van een gedeelde voorouder. Voor de niet-specialist is de kernboodschap dat de natuur neigt naar het hergebruiken van succesvolle ontwerpen: één vouwing kan herhaaldelijk worden aangepast om heel verschillende problemen op te lossen, van het aanzetten van genen tot het fijnregelen van stofwisseling en hersenchemie. Door 3D-structuurvergelijking te combineren met machine learning bieden de auteurs een praktisch gereedschap om dergelijke relaties te onthullen, wat biologen helpt voorspellen wat onbekende eiwitten mogelijk doen en farmaceutische ontwikkelaars wijst op nieuwe, evolutionair-geïnformeerde doelwitten in ziekte‑relevante routes.
Bronvermelding: Selvaraj, M.K., Kaur, J. Evaluating the evolutionary relationship of TATA binding protein (TBP) with various folding patterns of protein domains using support vector machine (SVM). Sci Rep 16, 7696 (2026). https://doi.org/10.1038/s41598-026-38883-z
Trefwoorden: TATA-box bindend eiwit, proteïne-evolutie, machine learning, proteïnestructuur, support vector machine