Clear Sky Science · nl
Massadichtheidsmetingen van individuele cellen met microkanaal‑gradiëntcentrifugatie
Waarom het wegen van piepkleine cellen ertoe doet
Elke levende cel is meer dan een zakje met moleculen; haar gewicht en compactheid vertellen iets over de gezondheid ervan. Fijne veranderingen in hoe dicht een cel is opgevuld kunnen aangeven of ze groeit, sterft, een infectie bestrijdt of kankerachtig wordt. Toch is het meten van de massadichtheid van duizenden individuele cellen lang traag, technisch ingewikkeld en duur gebleven. Dit artikel beschrijft een nieuwe, veel eenvoudigere manier om individuele cellen te "wegen" door te observeren hoe ze drijven of zinken in een gecontroleerde vloeistof binnen een haardun glaskanaal dat in een centrifuge wordt rondgedraaid.
Een nieuwe draai aan een oude labtruc
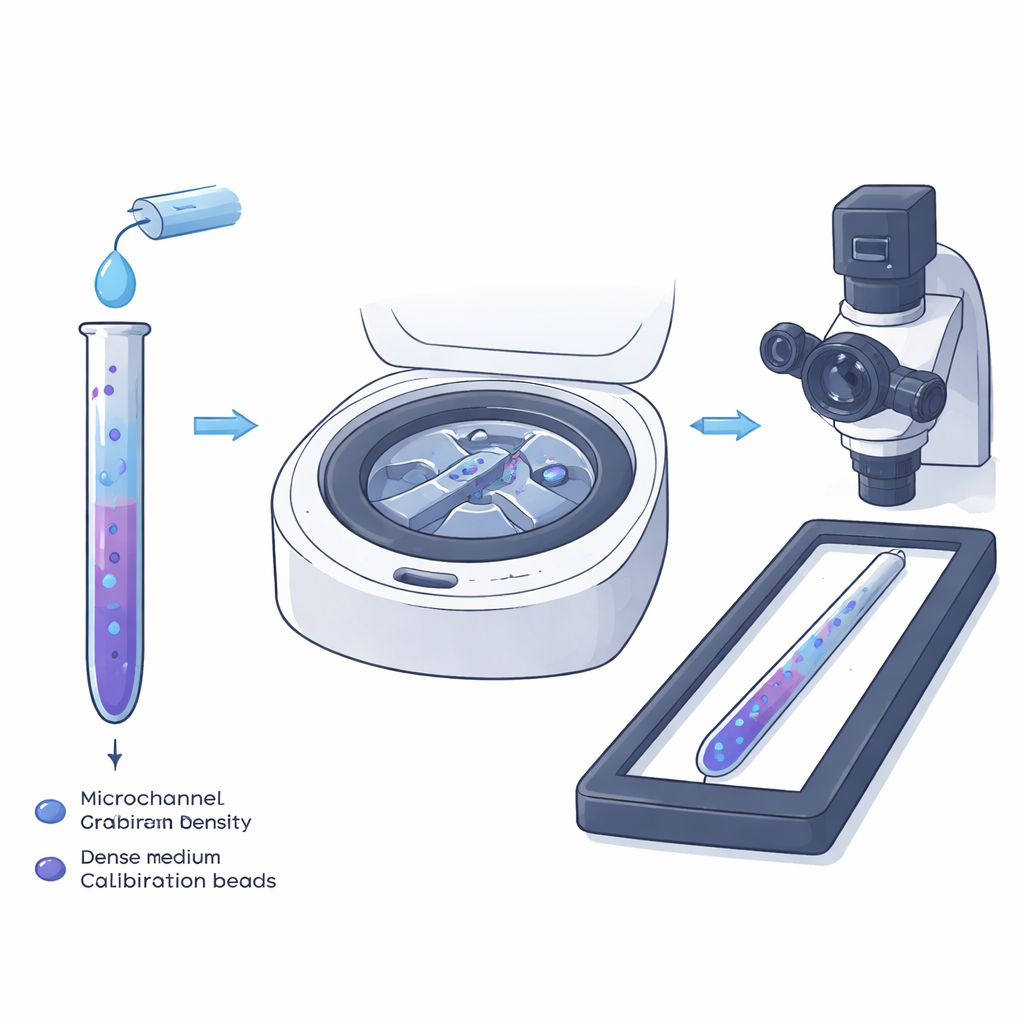
Traditionele dichtheidsgraadcentrifugatie wordt al lang in reageerbuizen gebruikt om mengsels van cellen te scheiden: bij draaien zakken cellen naar de plek in een gelaagde vloeistof waar hun eigen dichtheid die van de omringende vloeistof evenaart. De auteurs verkleinen dit idee tot een smal microkanaal zodat individuele cellen, en niet alleen lagen, rechtstreeks onder een microscoop kunnen worden gemeten. Ze vullen het kanaal eerst met een lichte vloeistof met de cellen en daarna met een zwaardere vloeistof met kleine plastic deeltjes waarvan de dichtheden precies bekend zijn. Wanneer deze twee vloeistoffen elkaar ontmoeten en in het dunne kanaal vloeien, vormen ze vanzelf een vloeiende, eendimensionale dichtheidsgraad langs de lengte van het kanaal.
Een geleidelijke dichtheidsslope creëren
In zulke dunne kanalen stroomt de vloeistof langzaam en soepel, zonder turbulentie. Onder deze omstandigheden mengt het parabolische stromingsprofiel de lichte en zware vloeistoffen net genoeg om een geleidelijke overgang te maken, in plaats van een scherpe grens, ertussen. Het team bestudeerde dit proces zowel experimenteel met een fluorescent kleurstof als met computermodellen. Ze vonden dat binnen enkele seconden een vrijwel lineaire dichtheidsgraad van enkele millimeters lengte kan ontstaan. De kanaalhoogte bleek cruciaal: ondiepe kanalen houden de gradiënt stabiel en voorkomen door de zwaartekracht veroorzaakte schommelingen van de zwaardere vloeistof, wat de relatie tussen positie en dichtheid zou vervagen en fouten in de uiteindelijke celmetingen zou introduceren.
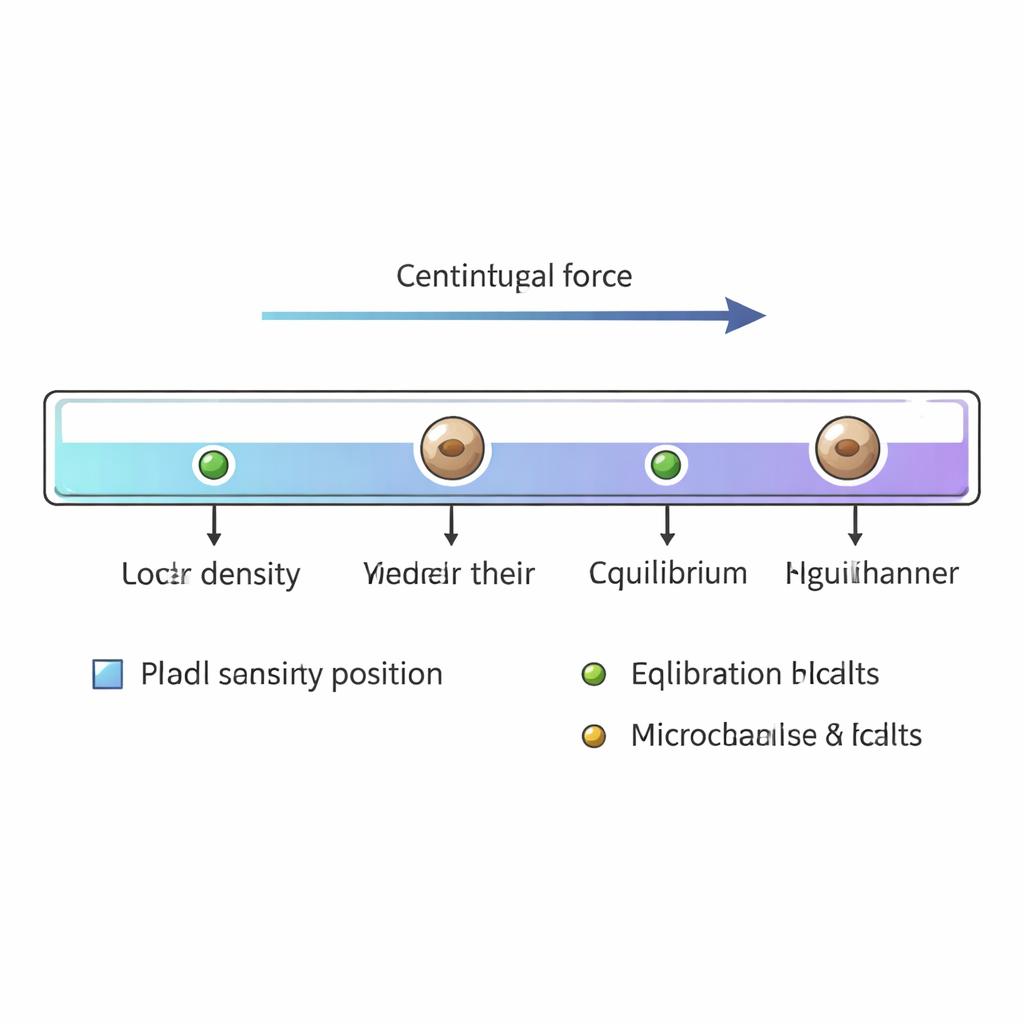
Cellen laten draaien naar hun evenwichtspunt
Zodra het kanaal is gevuld, worden de uiteinden afgesloten en wordt het in een kleine centrifuge geplaatst. Bij ongeveer 12.000 omwentelingen per minuut bewegen cellen en kalibratieparels langs het kanaal totdat de naar buiten gerichte kracht door het draaien precies in evenwicht is met de opwaartse kracht voor hun specifieke dichtheid. Gistcellen groter dan ongeveer drie micrometer in diameter bereiken dit evenwicht in minder dan 20 seconden. Na ruwweg anderhalve minuut draaien wordt het kanaal verwijderd en onder een standaardmicroscoop gescand. De onderzoekers registreren de posities van duizenden individuele gistcellen en de referentieparels, en zetten vervolgens elke positie langs de gradiënt om in een massadichtheidswaarde met behulp van de bekende dichtheden van de parels als ankerpunten.
Celgezondheid aflezen uit kleine verschillen
Met deze aanpak maten de auteurs de dichtheden van meer dan 20.000 gistcellen over meerdere kanalen. De typische meetonzekerheid voor een enkele cel was ongeveer 3,3 kilogram per kubieke meter — klein genoeg om echte biologische verschillen te onderscheiden, die in hun monsters ruwweg twee keer zo groot waren. Over vele uren observeerden ze dat de hoofdpopulatie gist een stabiele dichtheid behield, terwijl een tweede, dichtere en iets kleinere populatie geleidelijk verscheen. Deze dichtere groep bestond waarschijnlijk uit dode of beschadigde cellen die de zware vloeistof hadden opgenomen, waardoor ze compacter werden. De gemeten waarden kwamen goed overeen met resultaten van veel complexere en langzamere technieken zoals suspended microchannel resonators, optische methodes en magnetische levitatie.
Van laboratoriumprototype naar praktisch biomarker
De studie toont aan dat een eenvoudige combinatie van glasmicrokanalen, gangbare centrifuges en standaardmicroscopen hoge‑doorvoer massadichtheidsmetingen van individuele cellen kan leveren met snelheden van ongeveer 16.000 cellen per uur. Hoewel het nog niet gevoelig genoeg is om de allerkleinste medicijn‑geïnduceerde veranderingen te detecteren, is het al krachtig genoeg om verschillende celtypen of levende van dode cellen te onderscheiden op basis van hoe dicht ze zijn opgevuld. Door precies cel"wegen" toegankelijker en betaalbaarder te maken, kan deze microkanaal‑gradiëntmethode helpen om massadichtheid van cellen tot een routinematig biomarker te maken voor het monitoren van ziekte, het evalueren van therapieën en het verkennen van hoe cellen hun interne samenstelling regelen.
Bronvermelding: Soller, R., Augustsson, P. & Barnkob, R. Single-cell mass-density measurements using microchannel gradient centrifugation. Sci Rep 16, 6501 (2026). https://doi.org/10.1038/s41598-026-38872-2
Trefwoorden: dichtheid van individuele cellen, microfluidica, centrifugatie, gistcellen, celbiomerkers