Clear Sky Science · nl
Half-gestuurde meerklassenpneumonieclassificatie met een CNN-cascadeforest-framework
Waarom slimmere pneumoniescans ertoe doen
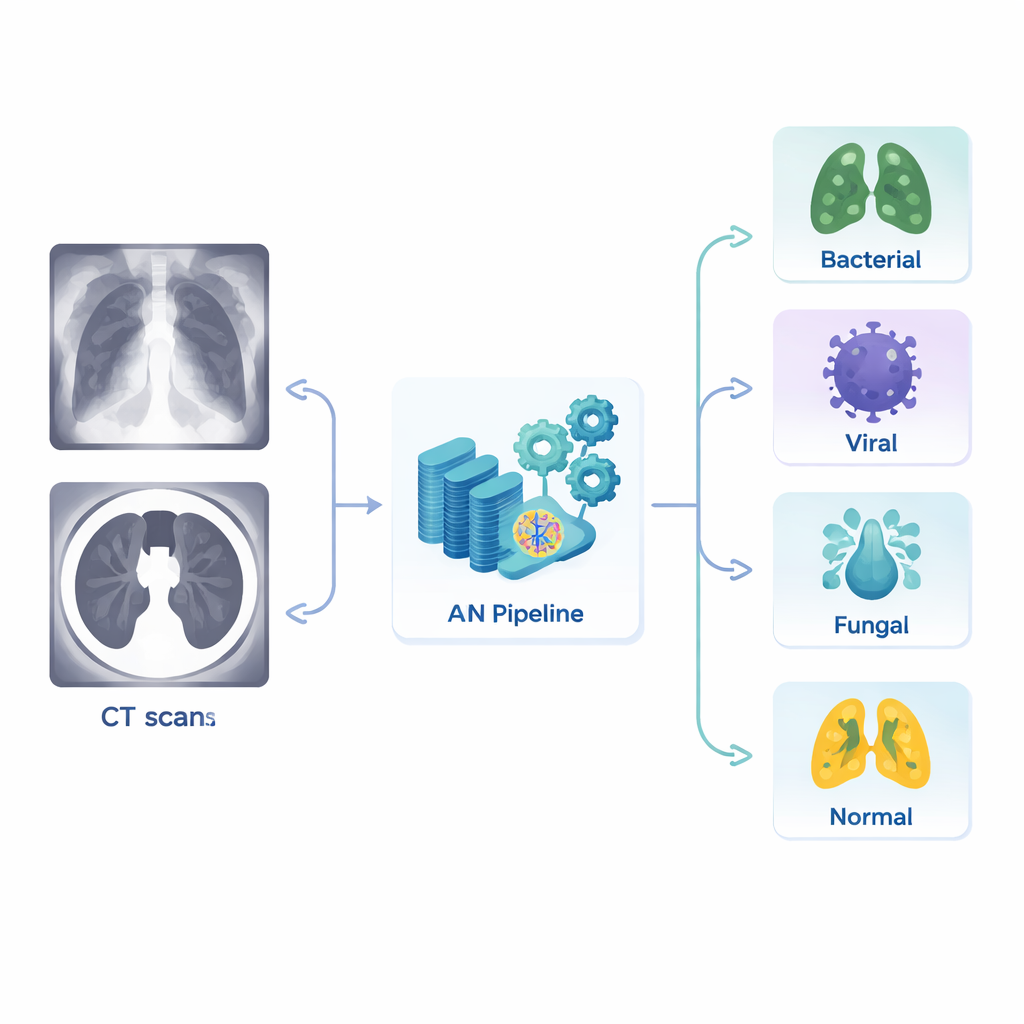
Pneumonie blijft een van de belangrijkste doodsoorzaken wereldwijd, maar veel ziekenhuizen—vooral die met minder specialisten—laten zich nog steeds leiden door drukbezette clinici die röntgenfoto’s of CT-scans van de borst visueel beoordelen. Dat bemoeilijkt niet alleen het opsporen van pneumonie, maar ook het vaststellen van het type: bacterieel, viraal, schimmel of een meer algemene ontstekingsafbeelding. Dit artikel beschrijft een nieuw systeem voor kunstmatige intelligentie (AI) dat daarvoor hulp biedt. Het gebruikt zowel röntgenfoto’s als CT-beelden, leert ook van scans die nooit door experts zijn gelabeld, en kan meerdere subtypes van pneumonie met opvallende nauwkeurigheid onderscheiden.
Van simpel ja/nee naar rijkere antwoorden
De meeste bestaande AI-hulpmiddelen voor longinfecties werken als een eenvoudige rookmelder: ze geven “pneumonie” of “geen pneumonie” aan en stoppen daar. Clinici hebben echter meer nuance nodig. Verschillende oorzaken van pneumonie reageren op verschillende geneesmiddelen, brengen verschillende risico’s met zich mee en zien er op beeldvorming vaak subtiel verschillend uit. De auteurs wilden een systeem bouwen dat vijf categorieën kan scheiden—bacterieel, viraal, schimmel, algemene pneumonie en normale longen—zodat geautomatiseerde hulpmiddelen richting kunnen geven die dichter bij wat een ervaren radioloog biedt liggen, in plaats van een eenvoudige rood‑vlagwaarschuwing.
Het koppelen van twee scanmethoden voor een vollediger beeld
Om hun methode te trainen en te testen, stelden de onderzoekers een dataset samen van 4.578 borstbeelden afkomstig uit openbare collecties: elke patiënt droeg zowel een röntgenfoto als een CT-scan bij die tijdens dezelfde klinische episode waren gemaakt. Röntgenfoto’s zijn snel en goedkoop maar vrij onscherp; CT-scans zijn langzamer en duurder maar tonen fijne structurele details. Door de twee modaliteiten zorgvuldig op patiëniveau te matchen en inconsistente of twijfelachtige gevallen te verwijderen, creëerde het team een realistische, ongelijke dataset die de dagelijkse geneeskunde weerspiegelt: sommige vormen van pneumonie, zoals schimmelinfecties, zijn veel zeldzamer dan andere.
Hoe de hybride AI leert van gelabelde en ongelabelde scans
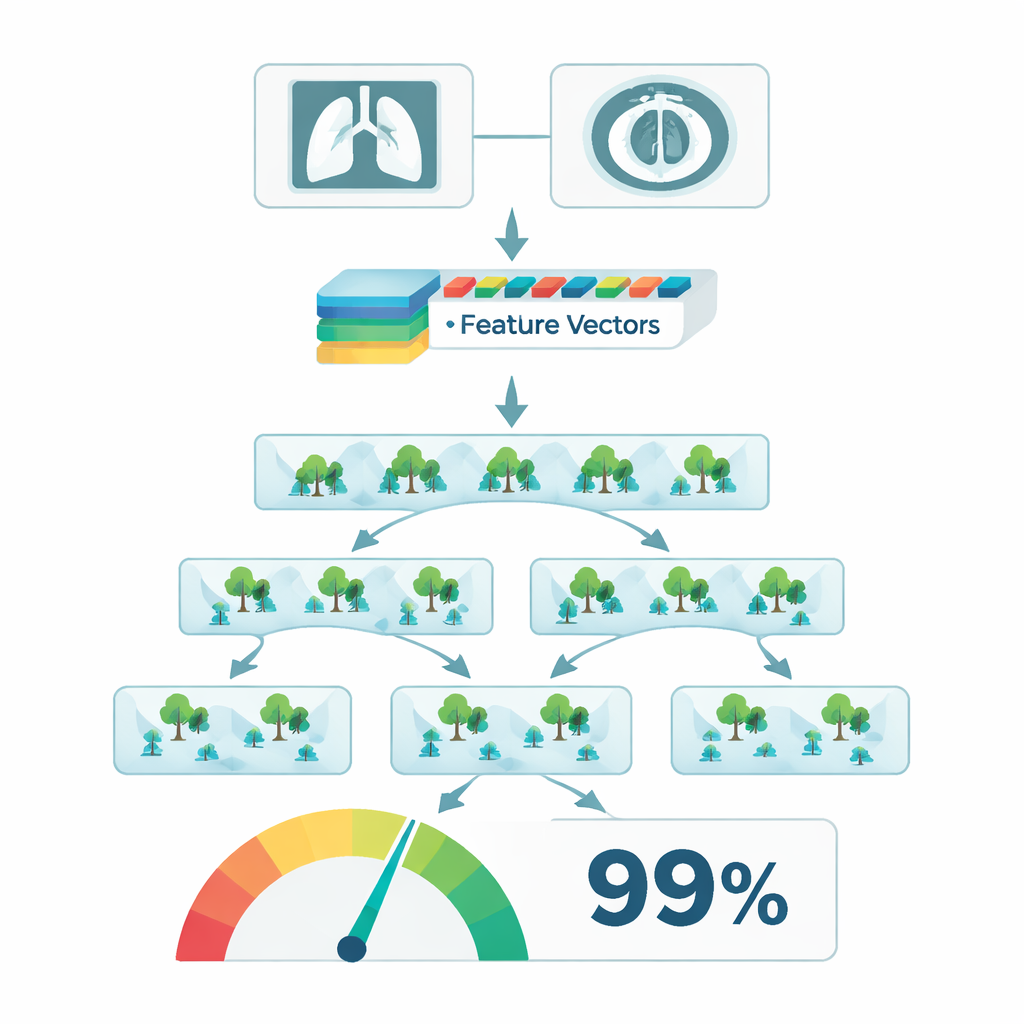
Het voorgestelde systeem, genoemd CNN‑Enhanced Cascade Forest (CE‑Cascade), combineert twee soorten machine learning. Ten eerste verwerkt een diep convolutioneel netwerk bekend als ResNet elk beeld en zet het om in een high‑dimensionale vingerafdruk die texturen, vormen en patronen vastlegt die met pneumonie samenhangen. In plaats van direct de diagnose te voorspellen, worden deze vingerafdrukken doorgegeven aan een "cascade forest"—meerdere lagen van decision‑tree-ensembles die het signaal herhaaldelijk verfijnen, inzoomen op lokale patches in het beeld en bij elke stap complexere patronen opbouwen. Cruciaal is dat de auteurs dit hybride model in een half‑gestuurd kader plaatsen: nadat een initiële versie is getraind op door experts gelabelde scans, mag het systeem “pseudo‑labels” toekennen aan ongelabelde beelden, maar alleen wanneer het erg zeker is. Die gevallen met hoge zekerheid worden vervolgens teruggevoerd in de training, waardoor de effectieve dataset zonder extra menselijk werk wordt uitgebreid.
Wat het systeem in de praktijk bereikte
Met deze aanpak behaalde het CE‑Cascade‑model een algehele classificatienauwkeurigheid van 98,86 procent over alle vijf categorieën, met eveneens hoge scores voor zowel röntgen‑ als CT‑gegevens. Het overtrof niet alleen eenvoudigere neurale netwerken, maar ook sterkere concurrenten, waaronder diepe convolutionele modellen met aandachtmechanismen en systemen op basis van transformers. Het toevoegen van pseudo‑gelabelde scans verbeterde consequent de kwaliteit van de voorspellingen, verhoogde meerdere evaluatiescores en maakte het model robuuster bij beperkte expertannotatie. De methode generaliseerde ook goed wanneer op de ene modaliteit werd getraind en op de andere werd getest, wat suggereert dat het ziektegerelateerde patronen had geleerd in plaats van eigenaardigheden van een bepaald scannertype.
Van labbenchmark naar hulp aan het bed
Voor niet‑specialisten is de belangrijkste conclusie dat dit werk AI‑ondersteunde borstbeeldvorming dichter bij iets brengt dat clinici daadwerkelijk kunnen gebruiken. In plaats van een black‑box‑hulpmiddel dat slechts “pneumonie: ja of nee” zegt, biedt het CE‑Cascade‑framework gedetailleerde, meerklassenuitvoer en doet dat efficiënt genoeg voor routinematige inzet. Door te leren van zowel gelabelde als ongelabelde scans en door kracht te putten uit de complementaire beelden van röntgenfoto’s en CT‑scans, zet het een hoge lat voor toekomstige systemen. Als het wordt vertaald naar klinische software en gecombineerd met duidelijke uitleg over welke beeldregio’s de beslissingen sturen, zou zo’n model artsen kunnen helpen patiënten sneller te triëren, meer passende behandelingen te kiezen en deskundigheidsniveau‑interpretatie naar ziekenhuizen uit te breiden die dat momenteel missen.
Bronvermelding: Muthukumaraswamy, P., Yuvaraj, T. & Krishnamoorthy, R. Semi-supervised multi-class pneumonia classification using a CNN-cascade forest framework. Sci Rep 16, 7448 (2026). https://doi.org/10.1038/s41598-026-38849-1
Trefwoorden: pneumonie-afbeeldingen, medische AI, borstkasröntgenfoto, CT-scan, half-gestuurd leren