Clear Sky Science · nl
Determinanten op residuniveau voor de thermische stabiliteit van het extremofiele Ts2631-endolysine
Waarom warmteminnende virussen relevant zijn voor toekomstige antibiotica
Naarmate antibioticaresistentie toeneemt, proberen wetenschappers nieuwe manieren te vinden om gevaarlijke bacteriën te doden. Een veelbelovende aanpak leent wapens van virussen die bacteriën infecteren, zogenaamde bacteriofagen. Deze virussen produceren enzymen, endolysinen genoemd, die gaten in bacteriële celwanden maken. De hier besproken studie richt zich op een opmerkelijk warmtestabiel endolysine, Ts2631, afkomstig van een virus dat leeft in IJslandse warmwaterbronnen. Door te achterhalen welke individuele bouwstenen van dit eiwit het zo stabiel maken bij bijna-kooktemperaturen, hopen onderzoekers robuustere, langduriger werkende antibacteriële enzymen te ontwerpen voor geneeskunde en biotechnologie. 
Een viraal gereedschap gesmeed in kokende warmwaterbronnen
Ts2631 komt van een bacteriofaag die de warmteminnende bacterie Thermus scotoductus infecteert, die floreert in water dat ruim boven 60 °C bereikt. Het Ts2631-enzym knipt een specifieke binding in peptidoglycaan, het stevige netwerk rond bacteriële cellen. Wat Ts2631 bijzonder maakt is de extreme thermostabiliteit: het blijft gevouwen tot ongeveer 100–105 °C, afhankelijk van de oplossing. Dat is ver boven de temperaturen waarop de meeste eiwitten uit elkaar vallen. De auteurs vergeleken Ts2631 met zijn best bestudeerde verwant uit een matig temperatuurvirus, het T7-lysozyme, om te achterhalen welke structurele trucs de natuur heeft gebruikt om Ts2631 onder zulke harde omstandigheden intact te houden.
Kortere lussen en een ander patroon van bouwstenen
Eiwitten zijn ketens van 20 typen aminozuren, gevouwen in ingewikkelde vormen. Toen de onderzoekers de 3D-structuren van Ts2631 en T7-lysozyme over elkaar legden, vonden ze dat de algemene architectuur zeer vergelijkbaar is: beiden hebben een compacte kern van helices en strengs. Het belangrijkste verschil ligt in de flexibele lusgebieden die deze elementen verbinden. Bij Ts2631 zijn deze lussen korter en tonen ze minder flexibiliteit, terwijl T7-lysozyme langere, lossere lussen heeft. Ts2631 bevat ook meer van bepaalde aminozuren die vaak met hittebestendigheid worden geassocieerd: het stijve proline; aromatische residuen zoals tyrosine en tryptofaan; en positief geladen arginine. Tegelijkertijd heeft het minder serine-, asparaginezuur- en glutaminezuur-residuen, die eiwitten bij hoge temperaturen kwetsbaarder kunnen maken. Dit patroon geldt niet alleen in vergelijking met T7-lysozyme, maar ook wanneer Ts2631 wordt vergeleken met honderden duizenden virale en vele miljoenen bacteriële eiwitten.
Individuele aminozuren verwisselen om hun belang te testen
Om van correlaties naar oorzaak-en-gevolg te gaan, verving het team systematisch 55 individuele aminozuren in Ts2631 en mat hoe elke mutatie de smelttemperatuur (Tm) en het vermogen van het enzym om bacteriële celwanden af te breken beïnvloedde. Sommige veranderingen rond het zink-bevattende actieve centrum waren bijzonder schadelijk. Toen ze drie zink-coördinerende residuen (H30, H131 en C139) altereerden, daalde de Tm met maximaal ongeveer 20 °C en ging de activiteit verloren. Twee geconserveerde tyrosines (Y60 en Y69) droegen ook bij aan stabiliteit. Verrassend genoeg verhoogde het verwijderen van een disulfidebrug — een type covalente verbinding tussen cysteïnes C80 en C90 — de smelttemperatuur zelfs, hoewel het de activiteit vernietigde. Dit laat zien dat zeer stabiel zijn in een buisje niet altijd betekent dat een eiwit beter functioneert onder reële omstandigheden. 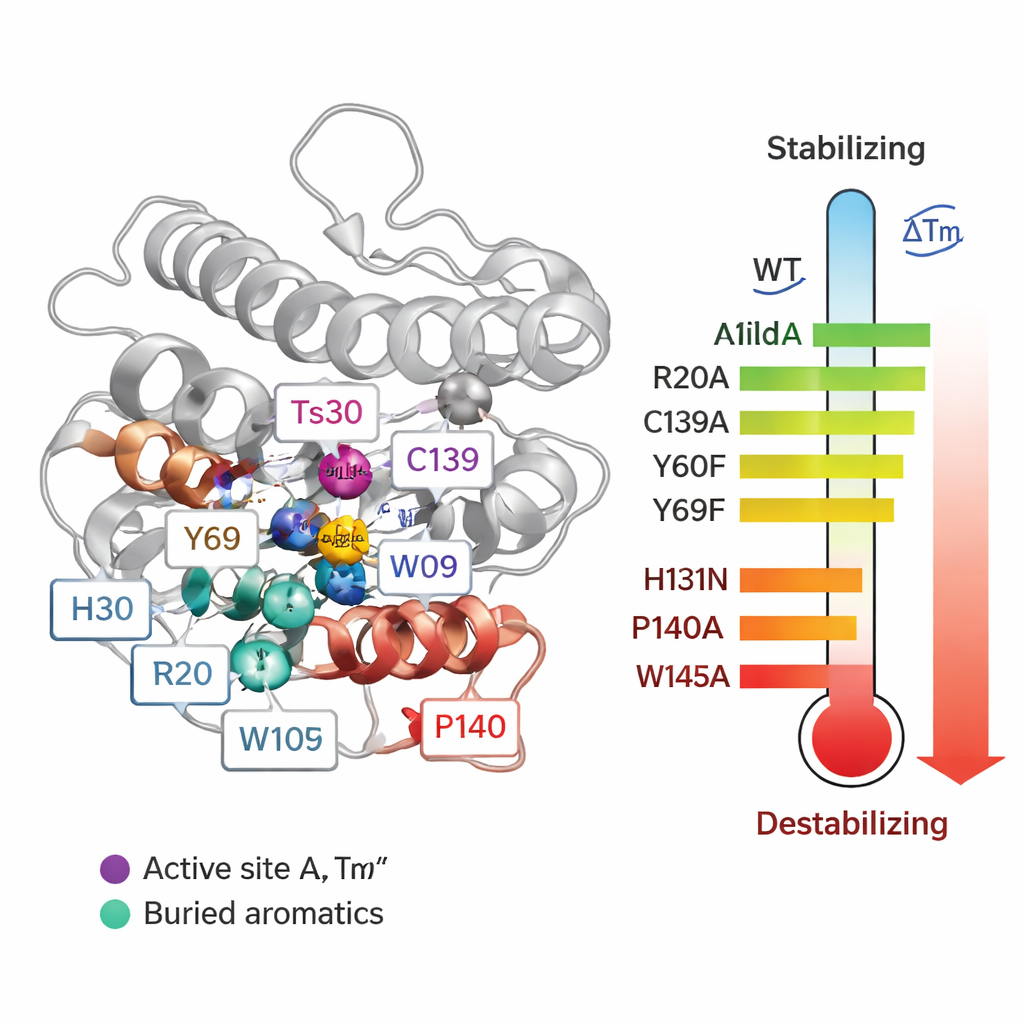
Verborgen aromatische “ankers” en een cruciale greep op de bacteriewand
De meest opvallende resultaten kwamen van mutaties in proline- en tryptofaanresiduen. Het veranderen van een enkel proline (P140), gelegen direct naast het zink-bindende C139, verlaagde de Tm met meer dan 21 °C en verzwakte de activiteit na verwarming, omdat de mutatie een speciale bindingsgeometrie verstoorde die nodig is voor correcte metaalbinding. Verschillende diep ingebedde tryptofanen (W102, W109 en vooral W145) bleken ook cruciaal: vervanging door alanine veroorzaakte Tm-dalingen van 14–24 °C en maakte het enzym veel gevoeliger voor hitte tijdens activiteitstests. Deze aromatische residuen fungeren als interne ankers die de kern van het eiwit op zijn plaats vergrendelen. Onder de arginines hadden de meesten weinig effect op stabiliteit, maar R20 bleek essentieel voor het vastgrijpen van peptidoglycaan. Toen R20 werd vervangen, bond het enzym slecht aan de bacteriële celwand en verloor het activiteit bij verwarming, wat aantoont dat sommige residuen meer bijdragen aan functie dan aan pure thermische robuustheid.
Van warmwater-enzymen naar robuustere antibacteriële middelen
Samengevat toont de studie dat Ts2631’s buitengewone hittebestendigheid steunt op een handvol welgekozen aminozuren in plaats van een uniforme versterking van het hele eiwit. Zink-bindende residuen, een geconserveerd proline nabij het actieve centrum en ingebedde aromatische zijgroepen vormen een stabiliserende kern, terwijl sommige klassieke stabiliserende kenmerken, zoals disulfidebruggen of zoutbruggen, hier minder belangrijk blijken dan verwacht. Voor het bredere veld suggereert dit werk dat mesofiele (matig temperatuur) endolysinen duurzamer gemaakt kunnen worden door geselecteerde posities zorgvuldig te vervangen door tryptofaan of proline zonder antibacteriële activiteit op te offeren. Met andere woorden: door te leren hoe de natuur enzymen bouwt die bijna-kooktemperaturen doorstaan, krijgen wetenschappers een praktisch ontwerpprincipe om betrouwbaardere, langduriger functioneren eiwitgebaseerde antibiotica te ontwikkelen.
Bronvermelding: Cieminska, K., Kaczorowska, AK., Kozlowski, L.P. et al. Residue-level determinants of the thermal stability of the extremophilic Ts2631 endolysin. Sci Rep 16, 7630 (2026). https://doi.org/10.1038/s41598-026-38786-z
Trefwoorden: thermostabiel endolysine, bacteriofaag-enzymen, eiwitthermostabiliteit, antibioticaresistentie, eiwitengineering