Clear Sky Science · nl
Studie naar biomarkers van homocysteïne‑geïnduceerde transformatie van vasculaire gladde spiercellen in schuimcellen
Waarom verstopte slagaders beginnen met kleine celveranderingen
Atherosclerose — het langzaam dichtslibben en verharden van slagaders — is een belangrijke oorzaak van hartaanvallen en beroertes. We horen meestal over cholesterol en voeding, maar minder over hoe individuele cellen in de vaatwand veranderen tijdens de ziekteontwikkeling. Deze studie bekijkt nauwkeurig één zo’n trigger, een bloedmolecuul genaamd homocysteïne, en laat zien hoe het normaal gesproken keurig functionerende spiercellen in de slagaders kan stimuleren om vet op te slaan en te veranderen in zogenoemde schuimcellen, de bouwstenen van gevaarlijke plaques.
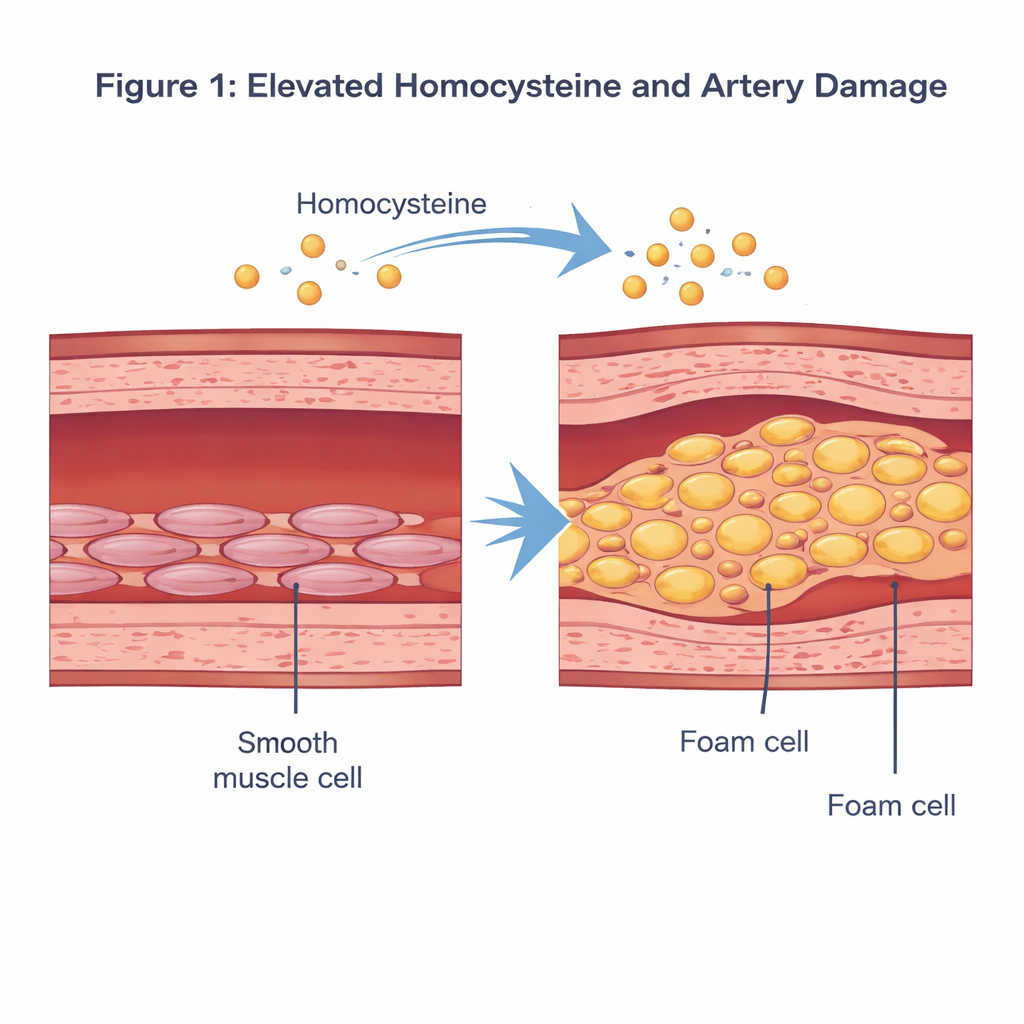
Aminozuur‑probleemmaker in de bloedbaan
Homocysteïne is een zwavelhoudend aminozuur dat ontstaat wanneer ons lichaam het voedingsstof methionine afbreekt. Onder normale omstandigheden is de concentratie in het bloed laag. Wanneer het stijgt boven ongeveer 15 micromol per liter — een toestand die hyperhomocysteïnemie wordt genoemd — hebben epidemiologische studies het gekoppeld aan een hoger risico op hart- en vaatziekten. Eerder onderzoek suggereerde dat overtollige homocysteïne de binnenste laag van de slagaders kan beschadigen, ontsteking kan aanwakkeren en het gedrag van vasculaire gladde spiercellen kan veranderen. Die cellen liggen in de middelste laag van de vaatwand en helpen de bloeddruk te reguleren door samen te trekken en te ontspannen.
Hoe vaatspiercellen veranderen in vetgevulde schuimcellen
De onderzoekers richtten zich op hoe homocysteïne deze gladde spiercellen vormt. In kweekschalen zetten ze menselijke vasculaire gladde spiercellen bloot aan een dosis homocysteïne die een ziektegerelateerde toestand nabootst en vergeleken die met onbehandelde cellen. Met behulp van standaardkleuringen en biochemische testen zagen ze dat homocysteïne‑behandelde cellen volraakten met roodgekleurde vetdruppels en dat hun cholesterol- en triglycerideniveaus sterk stegen. Tegelijkertijd daalden eiwitmarkers die bij hun gebruikelijke ‘contractiele’ identiteit horen, terwijl markers van een meer synthetische, plaque‑vormende staat toenamen. Samen tonen deze veranderingen aan dat homocysteïne gladde spiercellen kan wegduwen van hun normale rol en richting een schuimcelachtige, vetgeladen fenotype kan sturen dat direct bijdraagt aan plaquevorming.
Zoeken naar moleculaire vingerafdrukken binnen de cellen
Om te begrijpen welke eiwitten tijdens deze transformatie veranderen, zette het team moderne proteomica in, een technologie die duizenden eiwitten tegelijk kan meten. Ze vergeleken eiwitniveaus in homocysteïne‑behandelde cellen met controles en kwantificeerden betrouwbaar bijna 4.800 eiwitten. Hiervan vielen 54 op als significant veranderd: 13 namen toe en 41 namen af. Veel van de verschuivende eiwitten zijn betrokken bij vetstofwisseling, celdoorslag, oxidatieve stress en structurele remodellering van cellen. De auteurs gebruikten vervolgens bioinformatica‑tools om deze eiwitten in functionele paden te groeperen en om hun interacties in kaart te brengen, waarbij netwerken werden uitgelicht die verband houden met cholesterolmetabolisme en stressreacties in de vaatwand.
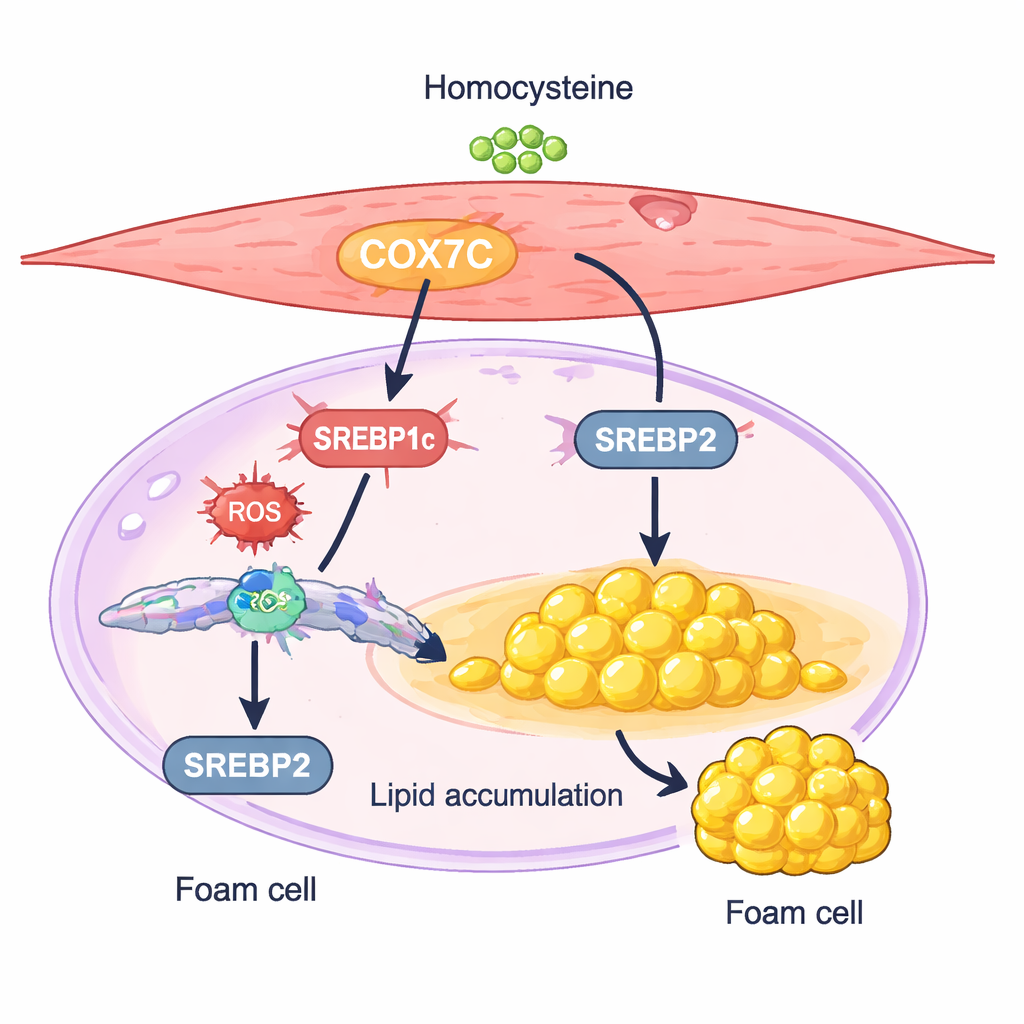
Een mitochondriale schakelaar die cellen aanzet tot vetopslag
Één eiwit, COX7C, kwam naar voren als een bijzonder interessante verdachte. COX7C is een component van de energiecentrales van de cel, de mitochondriën, waar het helpt bij de energieproductie. In de homocysteïne‑behandelde gladde spiercellen waren de COX7C‑niveaus hoger dan in de controles. De onderzoekers toonden aan dat het verder opvoeren van COX7C de cellen nog meer vet liet ophopen en leidde tot hogere expressie van twee hoofdregelaars van lipidenproductie, SREBP1c en SREBP2. Het uitschakelen van COX7C had het tegenovergestelde effect: het dempte SREBP‑activiteit, verminderde de ophoping van cholesterol en triglyceriden en beperkte de schuimcelachtige veranderingen. Deze resultaten ondersteunen een model waarin homocysteïne COX7C in mitochondriën opvoert, cellulaire stresssignalen verhoogt en daardoor SREBP‑gestuurde vetvorming activeert, waardoor gladde spiercellen overslaan naar een lipiden‑opslaghouding.
Wat dit betekent voor hartgezondheid en toekomstige therapieën
Dit werk bewijst nog niet wat er in menselijke slagaders gebeurt, en het is uitgevoerd in gekweekte cellen en niet in patiënten. Toch biedt het een gedetailleerd beeld van hoe verhoogde homocysteïne kan helpen bij het omzetten van nuttige vaatspiercellen in schadelijke schuimcellen, en identificeert het COX7C en aanverwante eiwitten als potentiële biomarkers of behandeldoelen. Voor de lezer is de kernboodschap dat los van ‘goed’ en ‘slecht’ cholesterol, kleine verschuivingen in de bloedchemie — zoals overtollige homocysteïne — de vaatwand van binnenuit kunnen herprogrammeren. Door moleculaire spelers als COX7C en het SREBP‑pad te pinpointen, legt deze studie het fundament voor toekomstige strategieën die plaques willen voorkomen door te voorkomen dat arteriële cellen veranderen in miniatuur vetopslagplaatsen.
Bronvermelding: Wang, X., Ma, X., Zhang, X. et al. Study on biomarkers of homocysteine-induced transformation of vascular smooth muscle cells into foam cells. Sci Rep 16, 7411 (2026). https://doi.org/10.1038/s41598-026-38763-6
Trefwoorden: atherosclerose, homocysteïne, schuimcellen, vasculaire gladde spiercellen, COX7C