Clear Sky Science · nl
Remming van immuuncheckpoints vergroot antigeenspecifieke T-celrespons bij hoofd-halskanker
De verdediging van het lichaam inzetten tegen hoofd-halskanker
Hoofd-halskankers blijven moeilijk te behandelen en zelfs krachtige nieuwe immunotherapieën helpen slechts een klein deel van de patiënten. Deze studie verkent een veelbelovend idee: immuuncellen beter leren cancer-specifieke signalen te herkennen en die cellen vervolgens vrijmaken van moleculaire “remmen” zodat ze tumoren effectiever kunnen aanvallen. Voor mensen met of met risico op hoofd-halskanker wijst dit werk op toekomstige vaccins en combinaties van geneesmiddelen die huidige behandelingen krachtiger en duurzamer zouden kunnen maken.
Waarom huidige immunotherapie zo weinig helpt
Moderne kankerimmunotherapie richt zich vaak op eiwitten die immuuncheckpoints worden genoemd en die als remmen op T-cellen fungeren — de witte bloedcellen die tumoren kunnen vernietigen. Bij plaveiselcelcarcinoom van hoofd en hals (HNSCC) worden middelen die het checkpoint PD-1 blokkeren — zoals nivolumab of pembrolizumab — al toegepast. Toch profiteert slechts ongeveer 20% van de patiënten en veel tumoren vorderen uiteindelijk. De auteurs wilden in een gecontroleerde laboratoriumopzet begrijpen hoe het blokkeren van PD-1 en aanverwante checkpoints T-cellen beïnvloedt die vooraf getraind zijn om tumor-specifieke merkers te herkennen, en of het combineren van meerdere checkpointmiddelen extra voordeel oplevert boven PD-1 alleen.
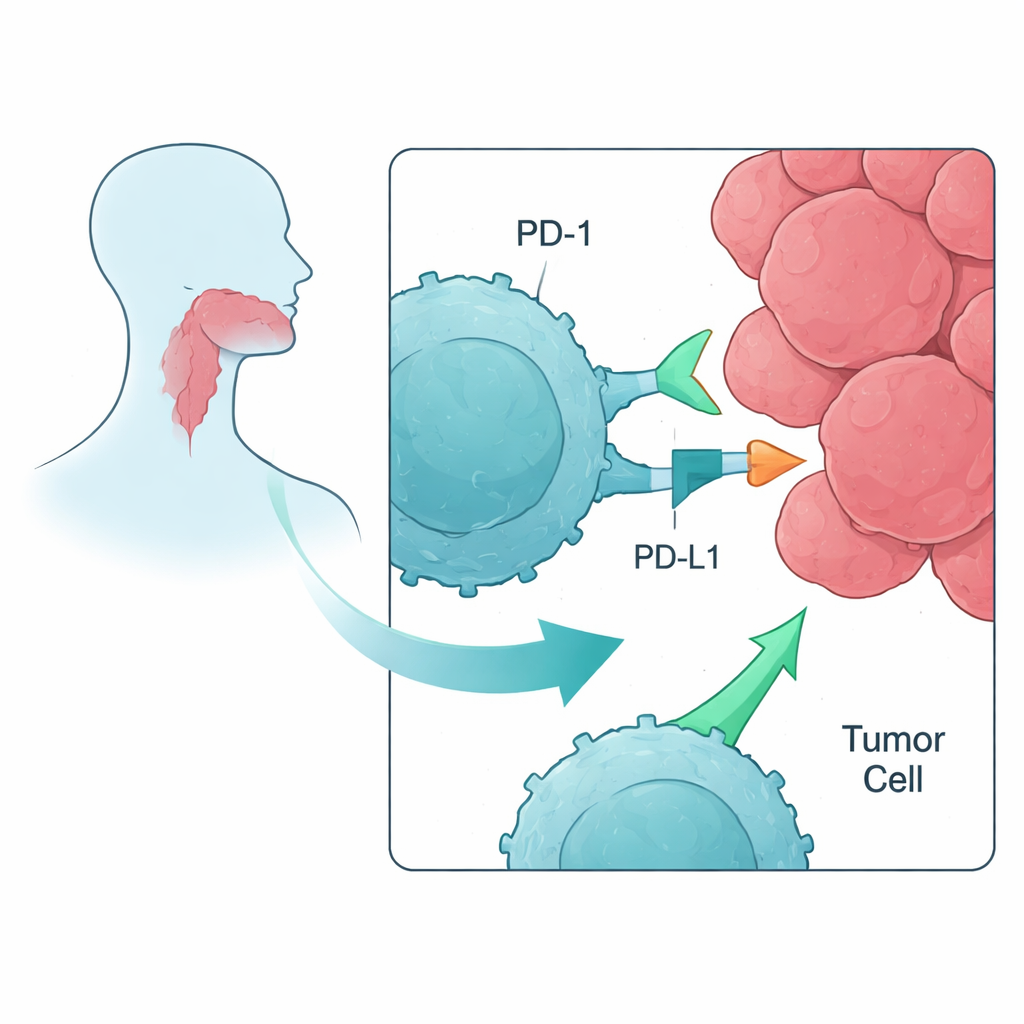
Immuuncellen trainen om kankerdetectie te verbeteren
De onderzoekers begonnen met bloedcellen van gezonde vrijwilligers in plaats van van patiënten, om te modelleren hoe een minder aangetast immuunsysteem vroeg in de ziekte zou kunnen reageren. Ze isoleerden perifere bloedmononucleaire cellen, waaronder T-cellen, en stelden deze bloot aan korte eiwitfragmenten — peptiden — afkomstig van tumorgeassocieerde antigenen die vaak in hoofd-halskankers voorkomen. Drie van die doelen bleken vooral goed in het activeren van T-cellen: MAGE, NY-ESO-1 en PRAME. Gedurende ongeveer een week in gemengde lymfocyt–peptideculturen fungeerden deze peptiden als kleine vaccins en breidden ze zeldzame T-cellen uit die elk specifiek het bijbehorende kankermarker konden herkennen.
De rem van getrainde T-cellen wegnemen
Vervolgens testte het team hoe deze getrainde T-cellen reageerden wanneer ze geconfronteerd werden met werkelijke hoofd-halskankercellen in aanwezigheid of afwezigheid van antilichamen die checkpoints blokkeren. Ze gebruikten een standaard labtest (ELISPOT) om de afgifte van interferon-gamma en granzyme B te meten — signalen dat T-cellen geactiveerd zijn en dodelijk kunnen zijn. Bij meerdere donoren verhoogde het toevoegen van het anti-PD-1-antilichaam consequent de respons van antigeenspecifieke T-cellen tegen de tumorcellijn, vaak met 60–100% of meer vergeleken met alleen peptide-stimulatie. Daarentegen leverde het blokkeren van andere checkpoints, zoals LAG-3 of TIM-3, hetzij alleen hetzij in combinatie met PD-1-blokkade, in dit systeem weinig tot geen extra voordeel op.
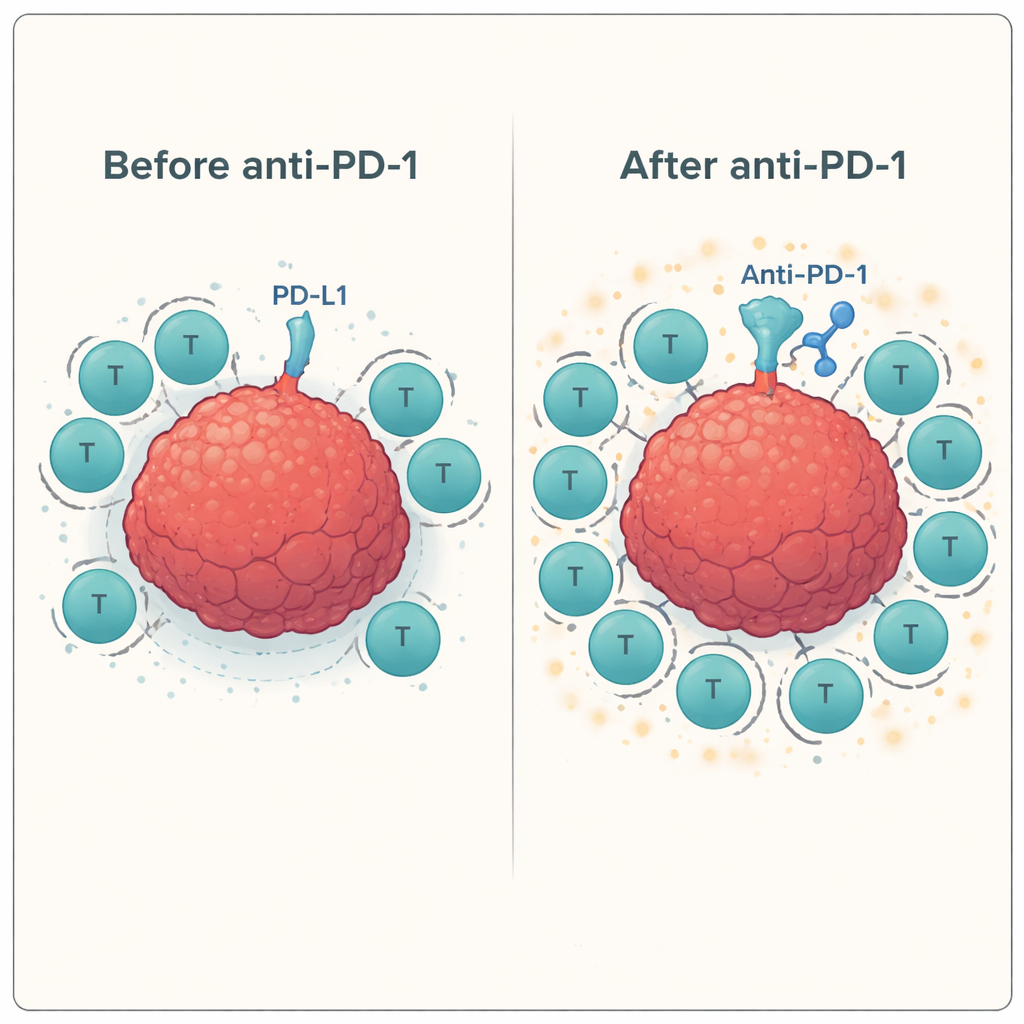
Het immuunlandschap in detail in kaart brengen
Om te begrijpen waarom sommige combinaties werkten en andere niet, gebruikten de onderzoekers flowcytometrie, een techniek die individuele cellen telt en karakteriseert. Ze toonden aan dat zowel T-cellen als tumorcellen PD-1 en diens liganden PD-L1 en PD-L2 op relevante niveaus tot expressie brengen, waardoor meerdere contactpunten ontstaan waar de PD-1-rem kan ingrijpen — en dus door geneesmiddelen kan worden geblokkeerd. Merkers geassocieerd met LAG-3 en TIM-3 waren ook aanwezig, maar de tumorcellijn bracht slechts een subset van hun partnermoleculen tot expressie, wat de beperkte impact van het richten op die checkpoints kan verklaren. Ze observeerden ook een trend naar verhoogde “gasgeven”-signalen (co-stimulerende moleculen zoals CD137 en GITR) op T-cellen na peptide-stimulatie en PD-1-blokkade, wat suggereert dat wanneer de belangrijkste rem wordt opgeheven, het gaspedaal meer druk kan zetten.
Wat dit voor toekomstige patiënten kan betekenen
Aangezien deze experimenten buiten het lichaam zijn uitgevoerd, kunnen ze de complexe tumoromgeving of de vaak verzwakte immuunsystemen van patiënten die chemotherapie en bestraling hebben ondergaan niet volledig nabootsen. Desalniettemin geven de bevindingen een duidelijke boodschap: wanneer T-cellen eerst worden geleerd specifieke kankerflags te herkennen (via een peptidevaccin) en vervolgens worden ontdaan van de PD-1-rem, worden ze veel beter in het aanvallen van hoofd-hals-tumorcellen. Het toevoegen van extra checkpointmiddelen bovenop PD-1 hielp in deze opzet niet. De auteurs concluderen dat een gerichte strategie — patiënten vaccineren met tumorgeassocieerde peptiden zoals MAGE, NY-ESO-1 of PRAME, gecombineerd met PD-1-blokkade — het testen in klinische trials verdient als manier om meer patiënten’ immuunsystemen in effectieve kankerbestrijders te veranderen.
Bronvermelding: Schuler, P.J., Oliveri, F., Puntigam, L. et al. Immune checkpoint inhibition increases antigen-specific T cell response in head and neck cancer. Sci Rep 16, 5583 (2026). https://doi.org/10.1038/s41598-026-38740-z
Trefwoorden: hoofd-halskanker, immuuncheckpointtherapie, PD-1-blokkade, kankervaccins, tumorantigenen