Clear Sky Science · nl
Chemische synthese van nieuwe aminopyrimidin-4-yl-1H-pyrazoolderivaten als remmers van spleen tyrosine kinase (SYK)
Waarom het blokkeren van één enzym kan helpen bij de strijd tegen kanker en ontsteking
Ons immuunsysteem is afhankelijk van snelle interne berichtgeving om cellen te laten weten wanneer ze indringers moeten aanvallen en wanneer ze moeten kalmeren. Als deze signalen verstoord raken, kunnen ze auto-immuunziekten en kanker aanwakkeren. Deze studie onderzoekt een veelbelovende manier om die foutieve signalen te dempen door het ontwerpen van kleine, geneesmiddelachtige moleculen die selectief een sleutelenzym blokkeren, spleen tyrosine kinase (SYK), dat dicht bij het hart van veel immuunreacties zit.
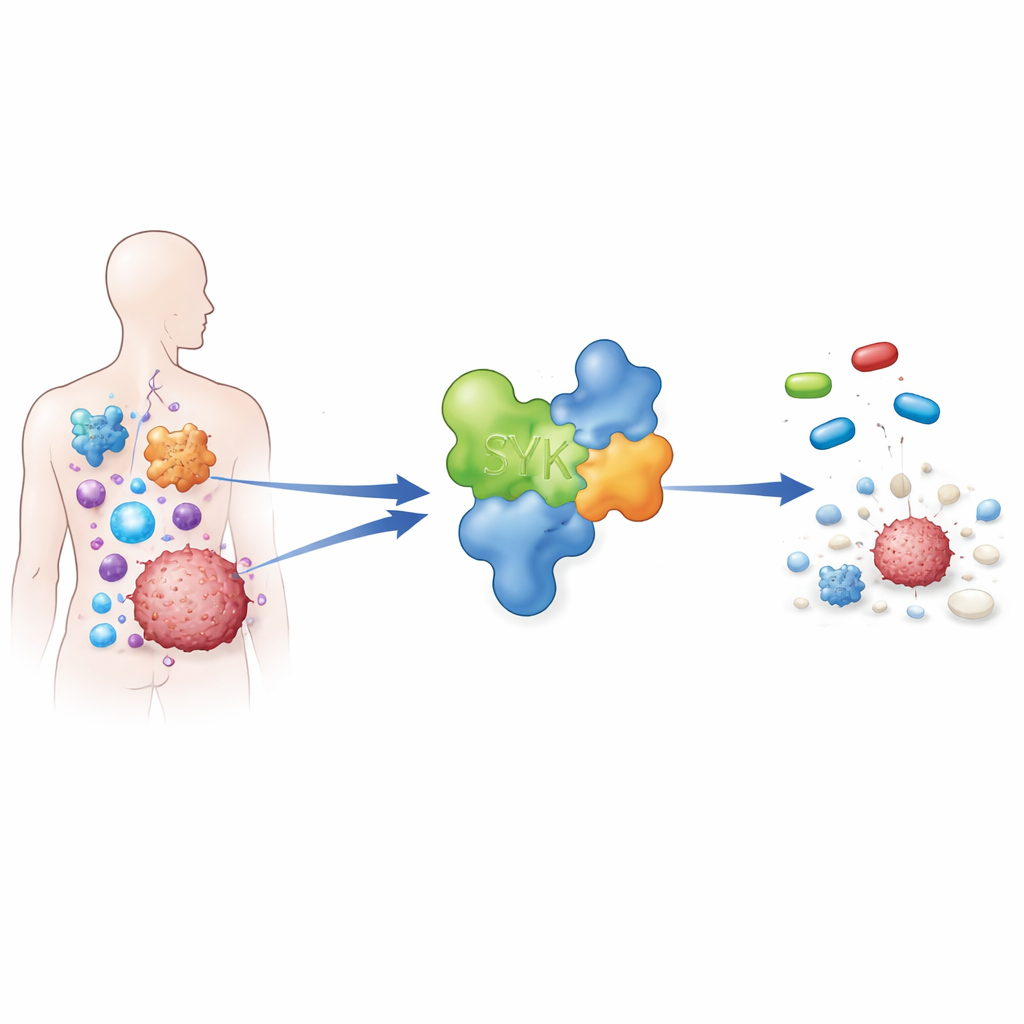
Een signaalschakelaar in het centrum van veel ziekten
SYK werkt als een hoofdschakelaar in bepaalde immuuncellen. Wanneer het geactiveerd wordt, draagt het bij aan ontsteking, de productie van antilichamen en celgroei. In gezonde situaties is dit nuttig om infecties te bestrijden. In aandoeningen zoals reumatoïde artritis, astma en verschillende bloed- en solide tumoren kan de activiteit van SYK echter te hoog worden, waardoor immuuncellen voortdurend geactiveerd blijven en tumoren worden gesteund. Vanwege deze centrale rol proberen onderzoekers wereldwijd geneesmiddelen te ontwikkelen die SYK blokkeren en tegelijkertijd krachtig genoeg zijn om te werken, maar precies genoeg om niet veel andere enzymen te raken en bijwerkingen te veroorzaken.
Het bouwen van een familie op maat gemaakte kleine moleculen
De auteurs creëerden een nieuwe reeks verwante moleculen rondom een gemeenschappelijk chemisch skelet dat aminopyrimidin-4-yl-1H-pyrazool wordt genoemd. Beginnend met eenvoudige bouwstenen hebben ze deze onderdelen stap voor stap aan elkaar gekoppeld en vervolgens één deel van de structuur aangepast om negen uiteindelijke kandidaten te produceren. Elk molecuul werd zorgvuldig gecontroleerd met standaard analytische methoden om te bevestigen dat structuur en zuiverheid overeenkwamen met wat bedoeld was. Deze modulaire aanpak stelde het team in staat te onderzoeken hoe subtiele veranderingen in vorm en flexibiliteit de manier beïnvloeden waarop deze verbindingen met SYK interageren.
Observeren hoe de verbindingen hun doel vastgrijpen
Voordat ze naar de laboratoriumbank gingen, gebruikten de onderzoekers computersimulaties om te zien hoe stevig elk molecuul zich aan SYK zou kunnen hechten. Dockingberekeningen schatten in hoe goed de verbindingen in het bindingsvak van het enzym passen, waarbij één kandidaat, aangeduid als 44, bijzonder veelbelovend bleek. Meer gedetailleerde moleculaire dynamicasimulaties, waarin het eiwit–geneesmiddelcomplex gedurende honderden nanoseconden werd gevolgd, toonden aan dat 44 een bijzonder stabiele samenwerking met SYK vormt. Het eiwit bleef compact, sleutelcontacten bleven behouden, en het systeem kwam in één lage-energietoestand met veel sterke waterstofbruggen terecht, vooral met aminozuren zoals tryptofaan en serine die helpen het molecuul te omkaderen.
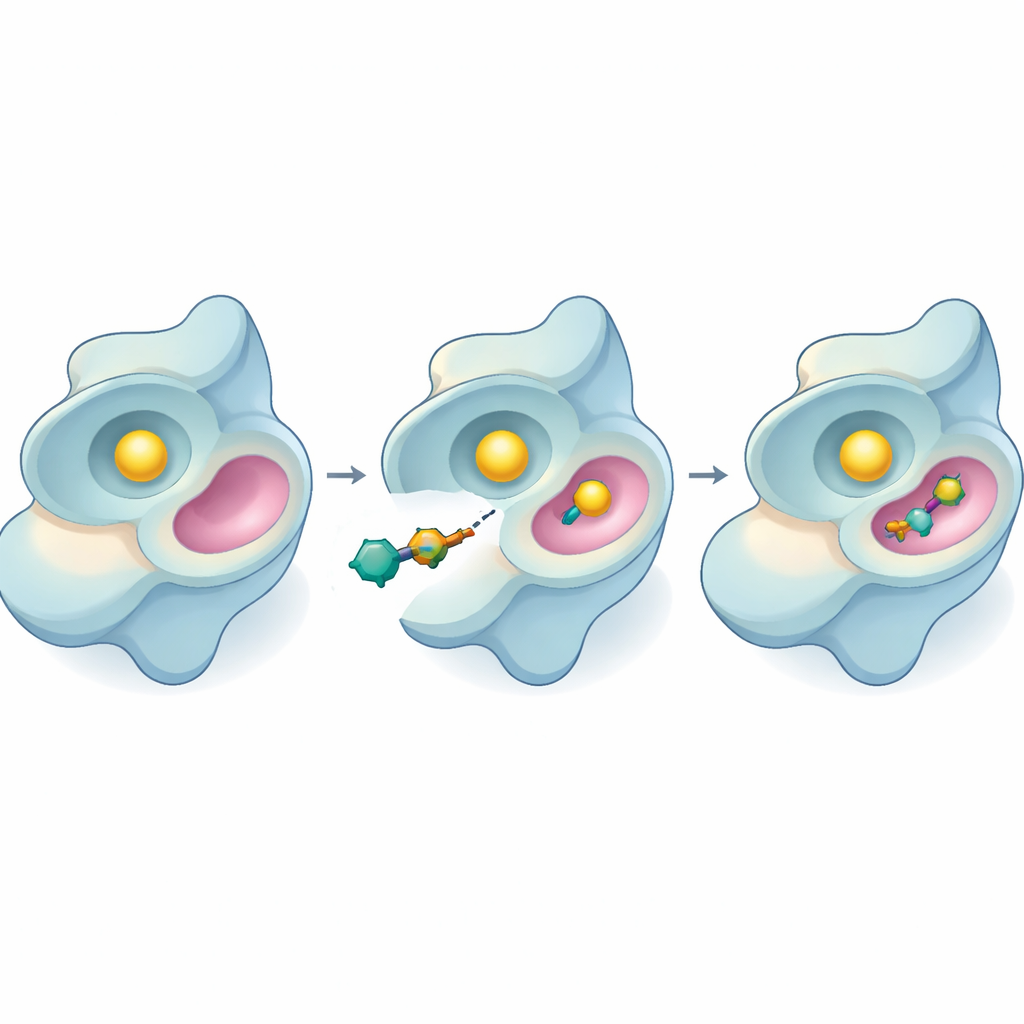
De nieuwe remmers op de proef stellen
Het team ging vervolgens over naar laboratoriumexperimenten met een lichtgebaseerde assay die meet hoe actief SYK zijn brandstofmolecuul, ATP, verbruikt. Verschillende van de nieuwe verbindingen vertraagden het enzym, maar 44 stak er opnieuw bovenuit. Het remde SYK bij zeer lage concentraties en werd effectiever naarmate het langer aan het enzym bleef. Door de hoeveelheid aanwezig substraat te variëren, konden de onderzoekers afleiden hoe 44 werkt: in plaats van direct te concurreren met ATP op de hoofdactieve plaats, lijkt het te binden aan een andere, allosterische plaats en het gedrag van het enzym van afstand te veranderen. Dit is belangrijk omdat allosterische remmers hun effect vaak behouden, ook wanneer ATP-niveaus hoog zijn of wanneer mutaties de primaire plaats veranderen.
Wat dit kan betekenen voor toekomstige behandelingen
Samen genomen schetsen de computermodellen en laboratoriummetingen een consistent beeld: molecuul 44 bindt sterk aan SYK, houdt het enzym in een stabiele, minder flexibele toestand en schakelt zijn activiteit uit via een indirect, niet-competitief mechanisme. Voor niet-specialisten betekent dit dat de onderzoekers een fijn afgestemde chemische sleutel hebben geïdentificeerd die past op een slot dat cruciaal is voor veel immuungedreven ziekten, zonder simpelweg de hoofdopening te blokkeren. Hoewel er nog veel werk aan de winkel is—vooral tests in cellen, dieren en bredere panels van verwante enzymen—biedt dit skelet een veelbelovend startpunt voor toekomstige geneesmiddelen gericht op het temmen van schadelijke ontsteking en het vertragen van bepaalde kankers door SYK te richten.
Bronvermelding: Rajasheker, K.V., Pallavi, M.S., Singh, P. et al. Chemical synthesis of novel aminopyrimidin-4-yl-1H-pyrazole derivatives as spleen tyrosine kinase (SYK) inhibitors. Sci Rep 16, 8323 (2026). https://doi.org/10.1038/s41598-026-38719-w
Trefwoorden: spleen tyrosine kinase, kinaseremmers, kankertherapieën, auto-immuunziekte, allosterische geneesmiddelen