Clear Sky Science · nl
Validatie van chemoresistentiefenotypes bij pleuraal mesothelioom in 2D-, 3D- en in vivo-modellen
Waarom sommige kankers chemotherapie van zich afschudden
Voor mensen bij wie pleuraal mesothelioom is vastgesteld—een kanker die in verband wordt gebracht met asbestblootstelling—is chemotherapie vaak de belangrijkste behandelingsoptie. Toch reageren veel tumoren nauwelijks, of ze krimpen aanvankelijk en komen dan snel weer terug. Deze studie stelt een schijnbaar eenvoudige vraag met grote gevolgen: zijn de laboratoriummodellen die onderzoekers gebruiken om medicijnen te testen realistisch genoeg om te voorspellen wat daadwerkelijk in het lichaam van een patiënt gebeurt?
Van platte cellagen naar kleine tumorbolletjes
De meeste kankermedicijnen worden eerst getest op cellen die als platte lagen op plastic schalen groeien. Deze tweedimensionale (2D) kweekmodellen zijn praktisch, maar lijken niet op echte tumoren, die driedimensionale (3D) massa’s zijn van dicht opeengepakte cellen omgeven door een complex netwerk van bloedvaten, ondersteunende eiwitten en immuuncellen. De onderzoekers bouwden een 3D "sferoïde"-model van mesothelioom, waarbij kankercellen samenklonteren tot compacte mini-tumoren. Ze vergeleken hoe mesothelioomcellen van alle belangrijke subtypes—epithelioid, biphasic en het zeer agressieve sarcomatoid—reageerden op standaardchemotherapie wanneer ze werden gekweekt als platte 2D-lagen of als 3D-sferoïden.
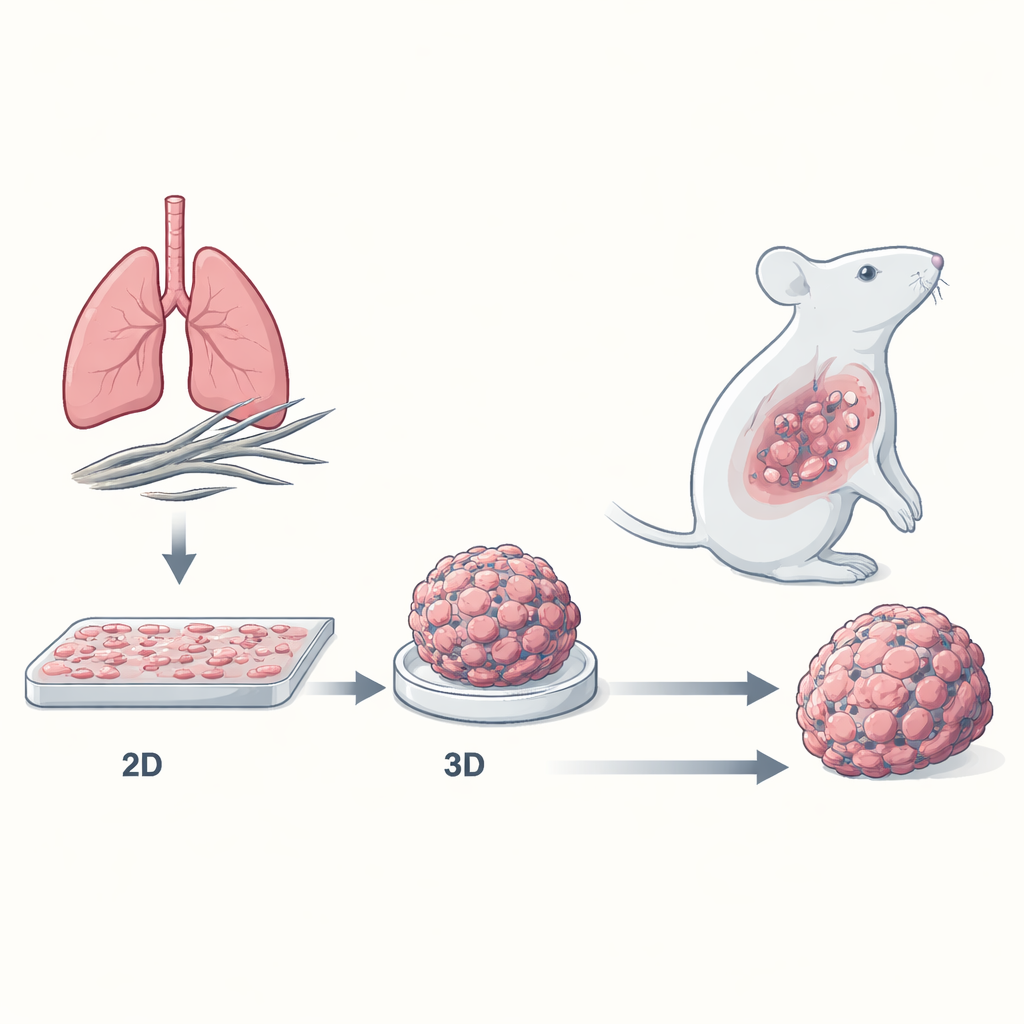
3D mini-tumoren zijn veel moeilijker te doden
Bij blootstelling aan de veelgebruikte combinatie cisplatine–pemetrexed raakten mesothelioomcellen gekweekt als 2D-lagen gemakkelijk beschadigd: hun groei vertraagde, velen kwamen vast te zitten in de "S-fase" van de celcyclus, en grote aantallen ondergingen geprogrammeerde celdood (apoptose). In contrast krimpten 3D-sferoïden nauwelijks en waren veel hogere medicijndoses nodig om vergelijkbare effecten te bereiken. Het sarcomatoïde subtype, dat bij patiënten bekendstaat als het moeilijkst te behandelen, was ook het meest geneesmiddelresistent in het 3D-model—een weerspiegeling van het klinische gedrag in de praktijk. Gedetailleerde metingen lieten zien dat 2D-cellen na behandeling hun levensvatbaarheid verloren en richting celdood gingen, terwijl cellen in sferoïden grotendeels in leven bleven, met slechts bescheiden toename van vroege apoptose.
Een stillere stofwisseling en overlevingsbevorderende signalen
Het team onderzocht hoe het energieverbruik verschilde tussen de twee modellen met behulp van een metabolische "stress-test." Chemotherapie duwde 2D-cellen van een actieve, energiehongerige toestand naar een stillere modus, met scherpe dalingen in mitochondriale zuurstofconsumptie—bewijs dat de behandeling hun interne energiecentrales verstoorde. Daarentegen leefden 3D-sferoïden al in een laag-energie, zuurstofarme toestand die nauwelijks veranderde door behandeling, vergelijkbaar met de gestreste, hypoxische omstandigheden in echte tumoren. De onderzoekers maten ook kleine regulerende moleculen genaamd microRNA’s en vonden subtypespecifieke patronen die aan medicijnresistentie gekoppeld waren. Vooral niet-epithelioïde sferoïden verhoogden microRNA’s die eerder geassocieerd werden met slechte prognose en verminderde celdood in andere kankers. In tumoren die in muizen uit 3D-sferoïden groeiden, werden eiwitten die betrokken zijn bij krachtige overlevingsroutes—PI3K/AKT en VEGF/Notch—opgevoerd, wat de kankercellen verder beschermde tegen celdood.
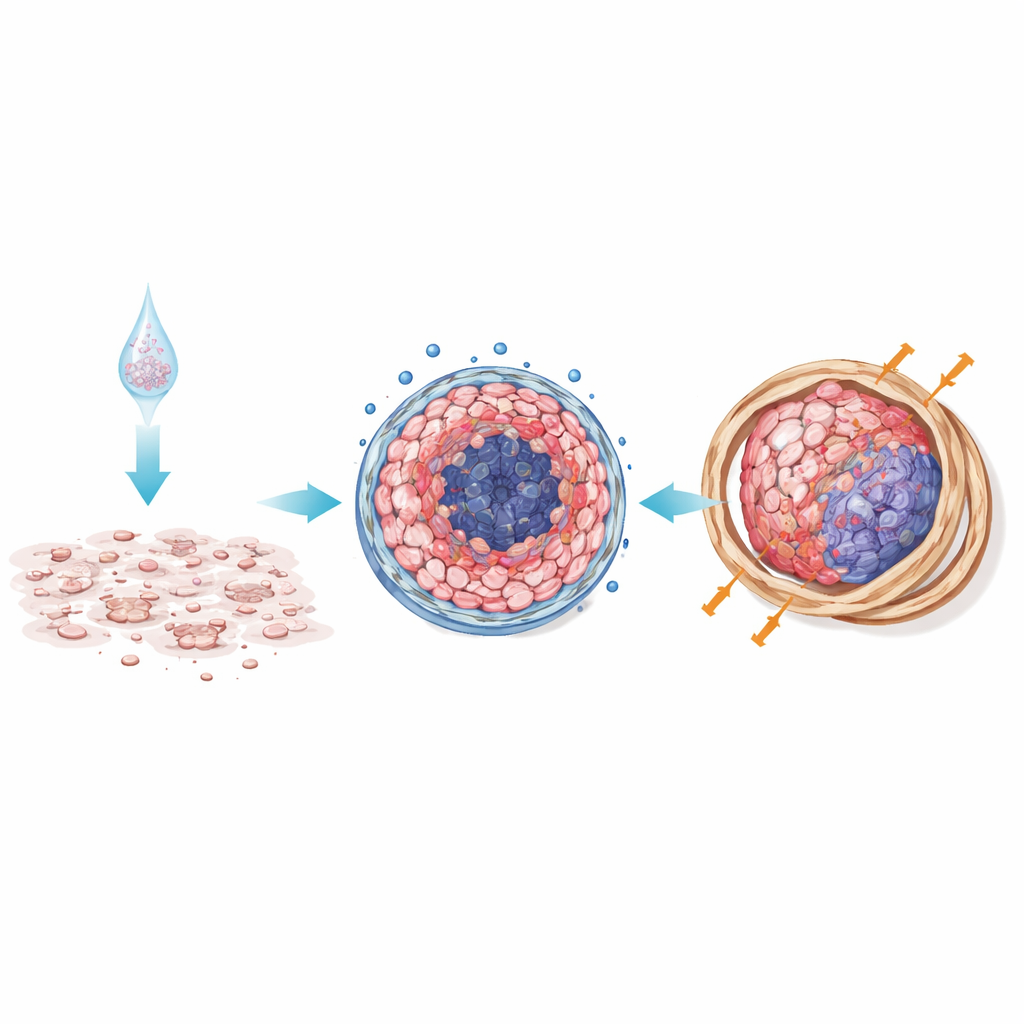
Muizen-tumoren bevestigen wat de schaal voorspelt
Om te zien of deze verschillen in levende organismen van betekenis waren, implanteren de wetenschappers mesothelioomcellen in muizen, ofwel als losse cellen (nabootsend 2D-kweek) of als voorafgevormde 3D-sferoïden. Tumoren die als sferoïden begonnen, groeiden groter en reageerden minder op chemotherapie dan die welke als losse cellen begonnen. Onder de microscoop toonden uit 3D afgeleide tumoren dichte banden van collageen en vezelig weefsel, met meer georganiseerde celnesten en minder dood weefsel. Deze fibrotische mantel werkt waarschijnlijk als een fysieke en biochemische barrière, beperkt de penetratie van medicijnen en versterkt overlevingssignalen—omstandigheden die sterk lijken op hardnekkige menselijke tumoren.
Wat dit betekent voor toekomstige behandeling
Voor leken is de kernboodschap dat de manier waarop we kankercellen in het laboratorium laten groeien de realiteit van medicijntesten kan maken of breken. Kleine 3D-tumorsferoïden reproduceren belangrijke kenmerken van mesothelioom die platte cellagen missen: zuurstofarme kernen, gestreste maar moeilijk te doden cellen, beschermend littekenachtig weefsel en activatie van overlevingsroutes die celdood blokkeren. Omdat deze 3D-modellen veel meer lijken op echte tumoren bij patiënten en in muizen, bieden ze een sterker platform voor het ontdekken van geneesmiddelen en voor het testen van combinaties die zowel de kankercellen als hun beschermende omgeving aanpakken. Op de lange termijn kan het gebruik van zulke realistische modellen onderzoekers helpen behandelingen te identificeren die een grotere kans van slagen hebben in de kliniek, niet alleen in het laboratorium.
Bronvermelding: Shi, H., Selvamani, S.P., Zelei, R. et al. Validation of chemoresistance phenotypes in pleural mesothelioma across 2D, 3D, and in vivo models. Sci Rep 16, 8396 (2026). https://doi.org/10.1038/s41598-026-38692-4
Trefwoorden: pleuraal mesothelioom, chemotherapie resistentie, 3D tumorsferoïden, tumormicro-omgeving, kanker medicijntestmodellen