Clear Sky Science · nl
Studie naar de differentiële expressie van disulfidptosis‑gerelateerde genen en hun associatie met immuunregulatie bij patiënten met diabetische retinopathie
Waarom deze oogziekte ons allemaal aangaat
Nu diabetes wereldwijd vaker voorkomt, is een van de meest gevreesde complicaties diabetische retinopathie — een aandoening die het lichtgevoelige weefsel achter in het oog beschadigt en kan leiden tot onomkeerbaar verlies van gezichtsvermogen. Artsen hebben nog altijd moeite te voorspellen welke patiënten hun zicht zullen verliezen en hoe ze dat het beste kunnen voorkomen. Deze studie onderzoekt een recent beschreven vorm van celdood, disulfidptosis genoemd, en vraagt of aan deze aandoening gerelateerde genen in het bloed vroegtijdige schade in het oog kunnen signaleren en nieuwe manieren kunnen onthullen om gezichtsverlies te voorkomen.
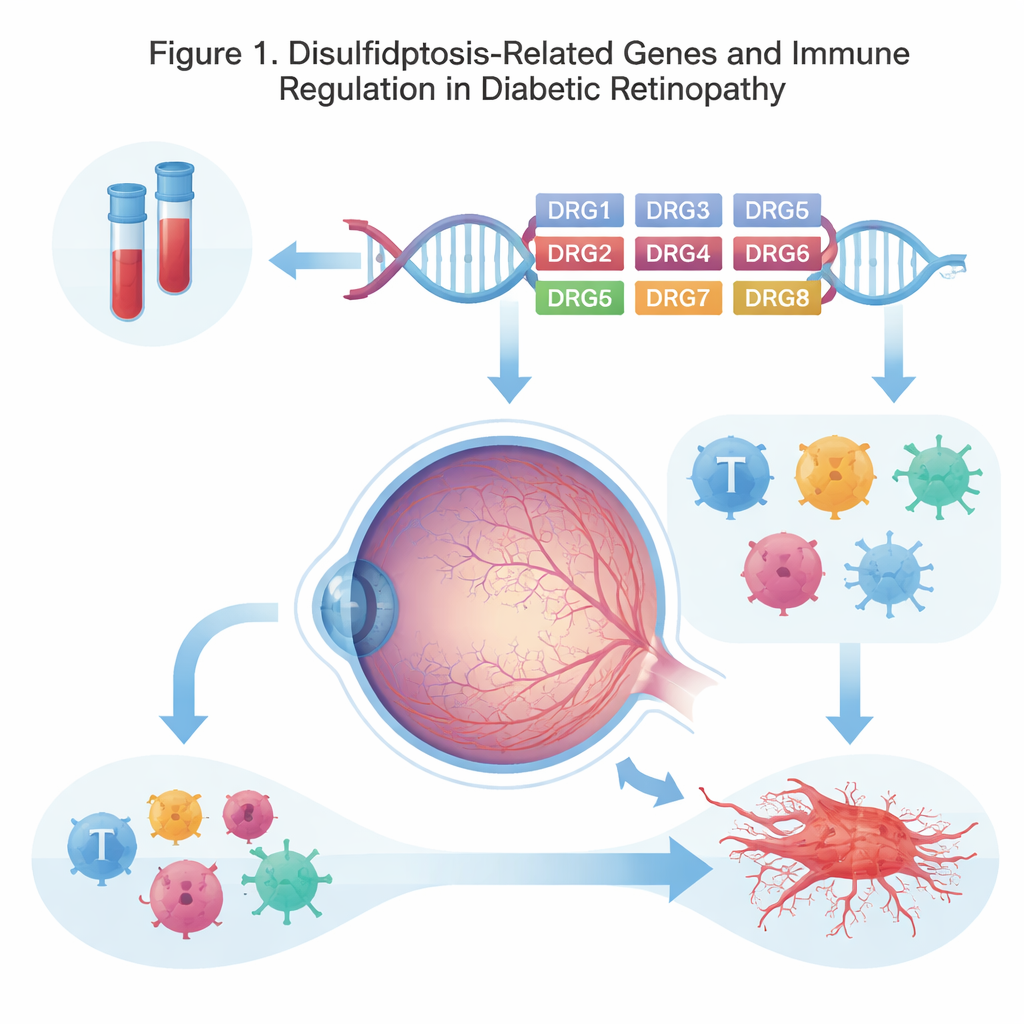
Een nieuw soort celtak
Onze cellen repareren en recyclen zichzelf voortdurend, en veel ziekten ontstaan wanneer deze ingebouwde doodsprogramma’s ontsporen. Onderzoekers beschreven recent disulfidptosis, een proces waarbij bepaalde chemische bindingen binnen structurele eiwitten abnormaal ophopen, het interne geraamte van de cel destabiliseren en tot instorten leiden. Omdat diabetische retinopathie samenhangt met langdurig hoge bloedsuikers, oxidatieve stress en kwetsbare bloedvaten in het netvlies, vermoedden de auteurs dat disulfidptosis‑gerelateerde genen betrokken kunnen zijn bij de sluipende schade die mensen hun gezichtsvermogen kost.
Op zoek naar waarschuwingssignalen in het bloed
Het team keek in een grote openbare databank met bloedmonsters van mensen met en zonder diabetische retinopathie. Ze richtten zich op 16 genen die eerder aan disulfidptosis waren gekoppeld en vergeleken hoe sterk deze genen waren aangeschakeld bij patiënten met oogziekte versus gezonde vrijwilligers. Acht genen vielen op als consequent verschillend, waarbij verschillende genen iets hogere activiteit vertoonden en twee lagere activiteit bij aangedane patiënten. De onderzoekers verzamelden vervolgens verse bloedmonsters van hun eigen ziekenhuispatiënten en bevestigden dat dezelfde genen, met name twee genaamd FLNB en GYS1, hetzelfde op‑ of neerwaartse patroon vertoonden. Hoewel elk gen slechts bescheiden veranderde, waren de afwijkingen over veel mensen heen consistent genoeg om betekenisvol te zijn.
Hoe bloedcellen en bloedplaatjes het oog kunnen beschadigen
Vervolgens onderzochten de wetenschappers wat deze genen mogelijk doen. Met standaard bioinformatica‑methoden vonden ze dat de veranderde genen waren verrijkt in routes die verband houden met bloedstolling, plaatjesactivatie en het behoud van normale circulatie. Deze processen staan centraal bij diabetische retinopathie, waarbij kleine haarvaten in het netvlies dichtslibben, lekken en vervolgens fragiele nieuwe vaatjes vormen. Een andere groep paden, waaronder Rap1‑ en MAPK‑signaalroutes, reguleert bekend hoe stevig vaatwandcellen aan elkaar hechten en hoe ze reageren op ontstekingsstress. De studie suggereert dat subtiele verschuivingen in disulfidptosis‑gerelateerde genen bloedplaatjes en vaatwandcellen richting schadelijk gedrag kunnen duwen, wat na verloop van tijd bijdraagt aan geblokkeerde of verzwakte retinaalvaten.
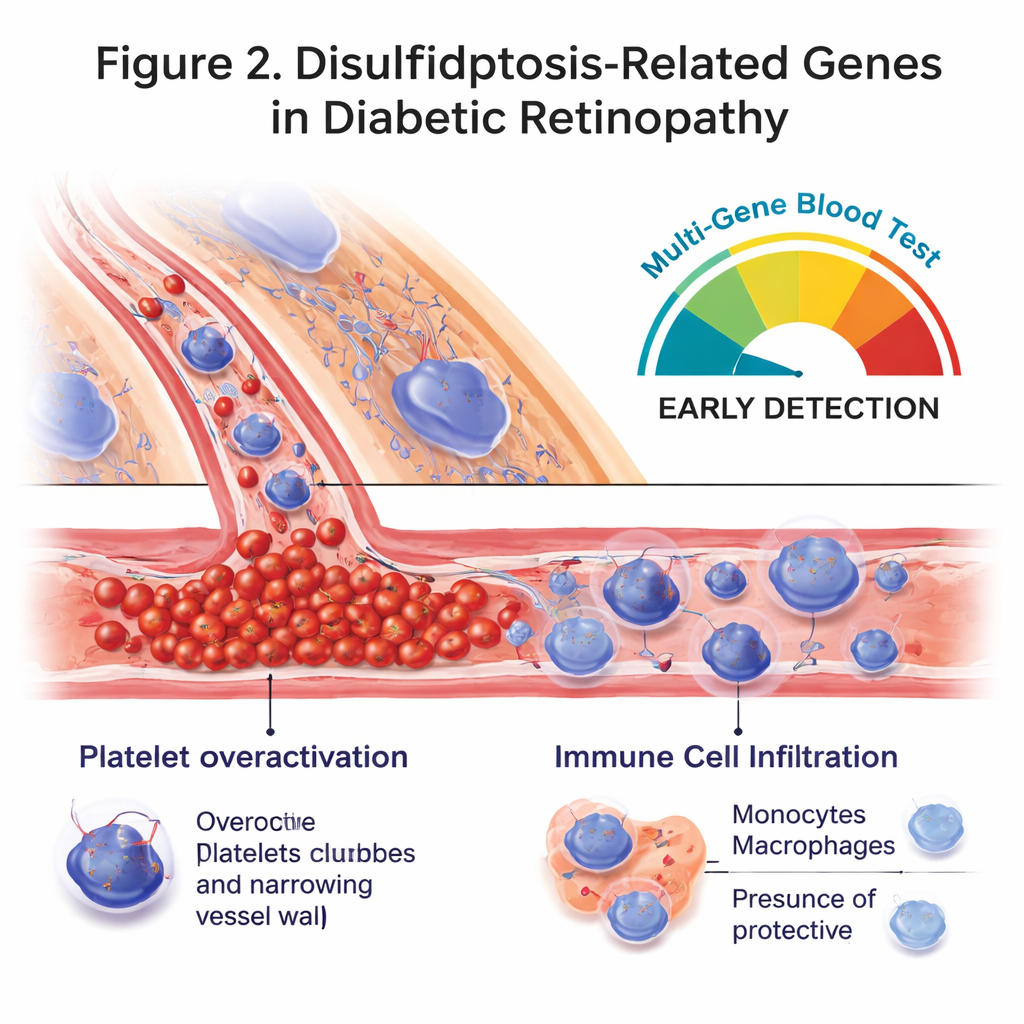
Immuuncellen en een op bloed gebaseerd risico‑score
De auteurs onderzochten ook immuuncelpatronen in dezelfde bloedmonsters met behulp van computationele methoden. Mensen met diabetische retinopathie hadden meer circulerende monocyten en vroege macrofagen — cellen die ontsteking kunnen versterken — en minder geactiveerde geheugen‑T‑cellen, die doorgaans helpen een gebalanceerde immuunrespons te coördineren. Verschillende van de disulfidptosis‑gerelateerde genen waren matig gekoppeld aan deze immuunverschuivingen, wat suggereert dat ze mede kunnen sturen hoe het immuunsysteem zich gedraagt bij diabetes. Voortbouwend op deze verbanden combineerde het team alle acht sleutelgenen in één risico‑score met een statistisch model. Deze multi‑genen “handtekening” onderscheidde patiënten met oogziekte redelijk nauwkeurig van gezonde controles, beter dan elk individueel gen alleen, en biedt een potentieel raamwerk voor een toekomstige bloedtest.
Wat dit voor mensen met diabetes zou kunnen betekenen
Vooralsnog is het werk vooral een proof of concept. Het model is gebouwd op één openbare dataset en een relatief kleine ziekenhuisgroep, en de studie toonde niet direct disulfidptosis aan in oogweefsel. Toch is het de eerste die deze nieuwe celdoodroute koppelt aan diabetische retinopathie en een set bloedgebaseerde genen voorstelt die samenhangen met zowel vaatbeschadiging als immuundisbalans. Als deze patronen worden bevestigd in grotere en gevarieerdere patiëntengroepen, zouden ze deel kunnen uitmaken van een goedkope bloedtest om personen met een hoog risico op gezichtsverlies te identificeren terwijl hun ogen nog gezond lijken, wat de deur opent naar eerdere monitoring en meer gepersonaliseerde preventiestrategieën.
Bronvermelding: Hao, Y., Zhang, XX., Wang, XY. et al. Study on the differential expression of disulfidptosis-related genes and their association with immune regulation in patients with diabetic retinopathy. Sci Rep 16, 7654 (2026). https://doi.org/10.1038/s41598-026-38671-9
Trefwoorden: diabetische retinopathie, disulfidptosis, biomarkers, immuuncellen, genrisicomodel