Clear Sky Science · nl
ConvAHKG: Actie-gebaseerde hybride kennisgraaf met een dubbelkanaals convolutionele aanpak voor geneesmiddelherbestemming
Nieuwe toepassingen vinden voor bestaande medicijnen
Het op de markt brengen van een volledig nieuw geneesmiddel kan meer dan een decennium duren en miljarden dollars kosten, en veel kandidaten stranden onderweg. Deze studie onderzoekt een slimmer kortere weg: het gebruik van data en kunstmatige intelligentie om nieuwe ziekten te ontdekken die bestaande, reeds goedgekeurde geneesmiddelen mogelijk veilig kunnen behandelen. De auteurs introduceren een raamwerk, ConvAHKG genoemd, dat allerlei soorten biomedische informatie verweeft tot één samenhangende kaart en vervolgens een moderne neurale netwerk gebruikt om veelbelovende geneesmiddel–ziekte-combinaties te signaleren — wat een snellere, goedkopere route naar nieuwe therapieën kan bieden.
Een rijke kaart van hoe geneesmiddelen en ziekten elkaar beïnvloeden
Centrraal in dit werk staat een “hybride kennisgraaf”, een gigantische kaart die geneesmiddelen, ziekten, eiwitten, bijwerkingen, chemische structuren en biologische routes met elkaar verbindt. In plaats van alleen eenvoudige ja/nee-koppelingen op te slaan (bijvoorbeeld “geneesmiddel A behandelt ziekte B”), legt de kaart vast hoe een geneesmiddel op een eiwit inwerkt — of het het activeert, remt of eraan bindt — en hoe eiwitten bij ziekten betrokken zijn, bijvoorbeeld als biomerkers of door veranderingen in activiteit. De graaf bevat meer dan 11.000 entiteiten en 59 typen relaties, inclusief gedetailleerde informatie over geneesmiddelclassificaties, bijwerkingen, eiwit–eiwitcontacten en chemische substructuren. Door deze veelheid aan contextlagen vast te leggen, kan de graaf meer van de daadwerkelijke biologische complexiteit achter behandeleffecten en bijwerkingen weerspiegelen. 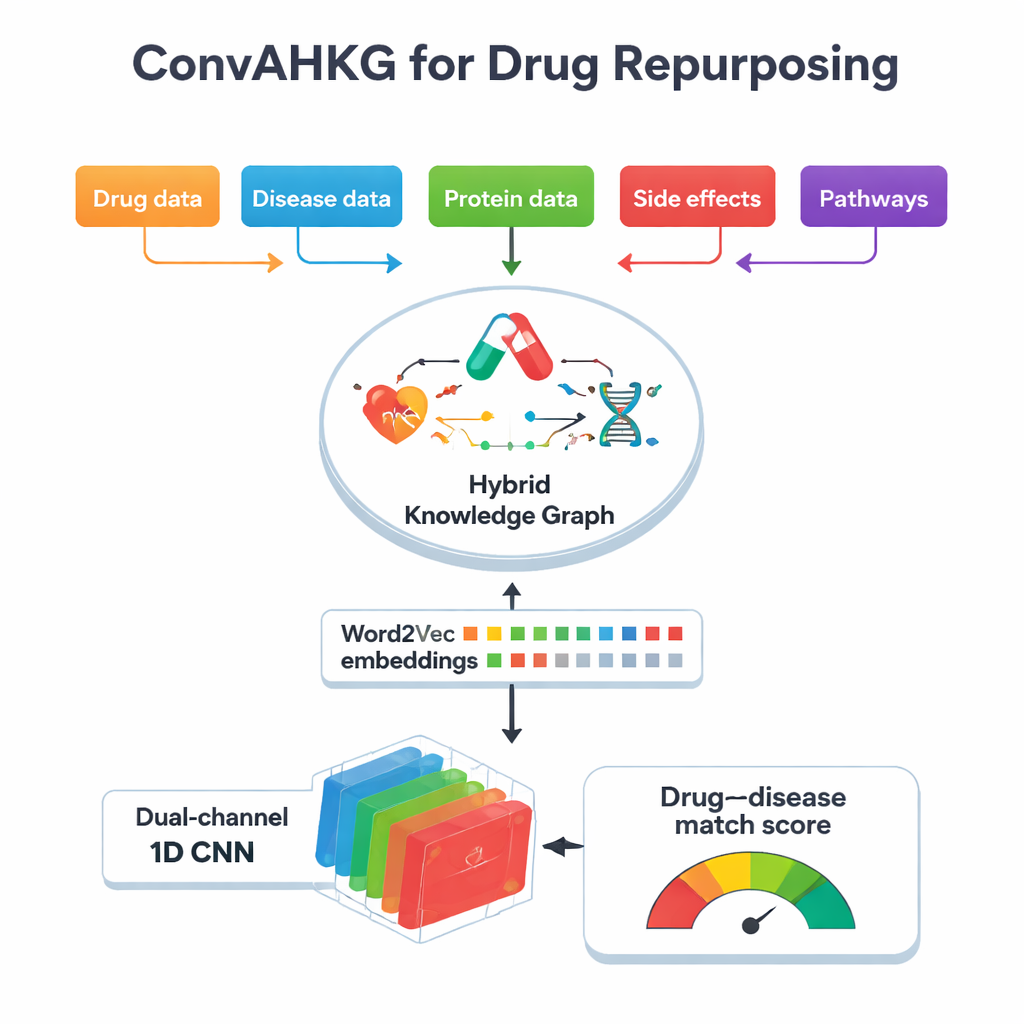
Het de computer de taal van de biologie leren
Om deze complexe kaart bruikbaar te maken voor machine learning zet het team elke verbinding in de graaf om in een eenvoudige drieledige “zin”: een head (zoals een ziekte), een relation (zoals biomarker) en een tail (zoals een eiwit). Ze passen vervolgens Word2Vec toe, een methode oorspronkelijk ontwikkeld voor natuurlijke taalverwerking, om numerieke “embeddings” te leren voor elk geneesmiddel, elke ziekte en elk eiwit. Items die vaak samen in deze zinnen voorkomen, komen dicht bij elkaar te liggen in deze wiskundige ruimte, vergelijkbaar met woorden met vergelijkbare betekenissen in tekst. Deze aanpak is veel eenvoudiger en sneller dan veel graf-specifieke embedding-technieken, en legt toch subtiele patronen vast. In tests tegen meerdere populaire knowledge-graph embedding-methoden evenaarde of overtrof Word2Vec hun voorspellende kracht terwijl het veel minder rekentijd gebruikte.
Een dubbel neurale route voor ja/nee-behandelbeslissingen
Zodra elk geneesmiddel en elke ziekte is vertaald naar een numerieke vector, voert ConvAHKG ze in een dubbelkanaals eendimensionaal convolutioneel neuraal netwerk. Het ene kanaal verwerkt de geneesmiddelvector en het andere kanaal verwerkt de ziektevector met een reeks convolutionele filters die lokale patronen en bredere motieven detecteren, geïnspireerd door ontwerpen uit beeldherkenning zoals InceptionNet en AlexNet. Na deze afzonderlijke verwerking worden de twee stromen samengevoegd en door meerdere volledig verbonden lagen geleid die één enkele kanswaarde produceren: vormt dit geneesmiddel–ziekte-paar een waarschijnlijk effectieve behandeling, of eerder een schadelijke bijwerking? Om om te gaan met het feit dat bekende positieve paren veel zeldzamer zijn dan negatieve, introduceren de auteurs een gewogen verliesfunctie die het missen van echte behandelingen zwaarder bestraft, waardoor de prestaties op deze moeilijk te vinden gevallen verbeteren. 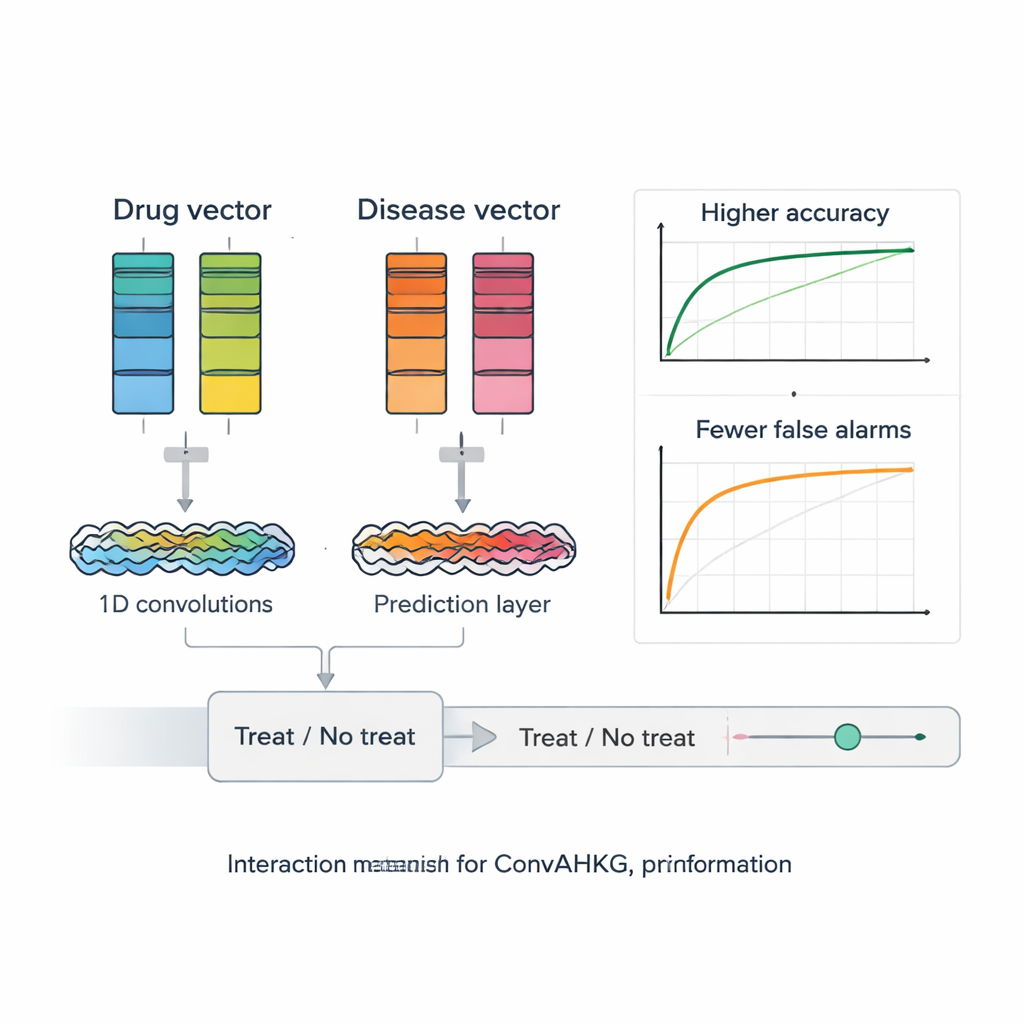
Beter dan bestaande methoden en het vinden van kandidaat-middelen tegen kanker
De onderzoekers testen hun raamwerk grondig tegen meerdere state-of-the-art tools voor geneesmiddelherbestemming die matrixfactorisatie, grafneuronale netwerken en diepe auto-encoders gebruiken. ConvAHKG behaalt een area under the ROC curve van 0,9836 en een area under the precision–recall curve van 0,9686, waarmee het alle concurrerende benaderingen op dezelfde benchmark-dataset overtreft. Ze passen het model vervolgens toe op niet-kleincellig longcarcinoom, de meest voorkomende en dodelijkste vorm van longkanker wereldwijd. ConvAHKG belicht meerdere geneesmiddelen die eerder niet als behandeling voor deze ziekte waren aangemerkt, waaronder het antilichaam trastuzumab, dat het HER2-eiwit target en al ondersteunend klinisch bewijs heeft bij longkanker, evenals andere biologische middelen en zelfs het klassieke antibioticum benzylpenicilline. Docking-simulaties suggereren dat benzylpenicilline sterk kan binden aan DNA en aan topoisomerase II alpha, een enzym dat vaak verhoogd is in deze tumoren, wat wijst op een mogelijk anticancereel mechanisme dat nu laboratoriumonderzoek rechtvaardigt.
Waarom dit belangrijk is voor patiënten
Simpel gezegd fungeert ConvAHKG als een zeer geïnformeerde matchmaker tussen bestaande geneesmiddelen en ziekten, gebruikmakend van een gedetailleerde kaart van biologische acties en een krachtig patroonherkenningssysteem om te voorspellen welke oude medicijnen in nieuwe contexten kunnen werken. Door veiligheid-geteste geneesmiddelen te behandelen als herbruikbare bouwstenen in plaats van als single-purpose hulpmiddelen, kan dit raamwerk de ontdekking van therapieën voor aandoeningen zoals longkanker versnellen, vooral waar conventionele geneesmiddelontwikkeling te traag of te kostbaar is. Hoewel de voorspellingen nog zorgvuldige experimentele en klinische validatie vereisen, toont de studie aan dat het combineren van rijke biologische kennis met moderne AI de zoekruimte drastisch kan verkleinen en veelbelovende, mogelijk levensreddende behandelingen sneller binnen bereik kan brengen.
Bronvermelding: Khodadadi AghGhaleh, M., Abedian, R., Zarghami, R. et al. ConvAHKG: Action-based hybrid knowledge graph with a dual-channel convolutional approach for drug repurposing. Sci Rep 16, 7592 (2026). https://doi.org/10.1038/s41598-026-38656-8
Trefwoorden: geneesmiddelherbestemming, kennisgraaf, deep learning, longkanker, geneesmiddelontdekking