Clear Sky Science · nl
Photo-geïnduceerde protonoverdracht in verschillend gestructureerd water: een EPR-benadering om een klassiek probleem op te lossen
Waarom de verborgen reizen van protonen ertoe doen
Elke keer dat u ademt, denkt, of zonlicht omzet in bruikbare energie in een zonnecel, bewegen kleine positief geladen deeltjes, protonen. Hoe deze protonen door water reizen is een eeuwenoud raadsel, voor het eerst geformuleerd door Theodor Grotthuss in 1806. Deze nieuwe studie gebruikt een slimme combinatie van licht en magnetische metingen om protonen te volgen in water met verschillende structuren — van zoute en drukke oplossingen tot ijzige, glasachtige mengsels en zelfs binnen een membraanprotein. Het werk biedt een frisse manier om klassieke ideeën over protonbeweging te testen en om omgevingen te onderzoeken die met andere methoden moeilijk te bestuderen zijn.
Een nieuwe manier om protonen te zien bewegen
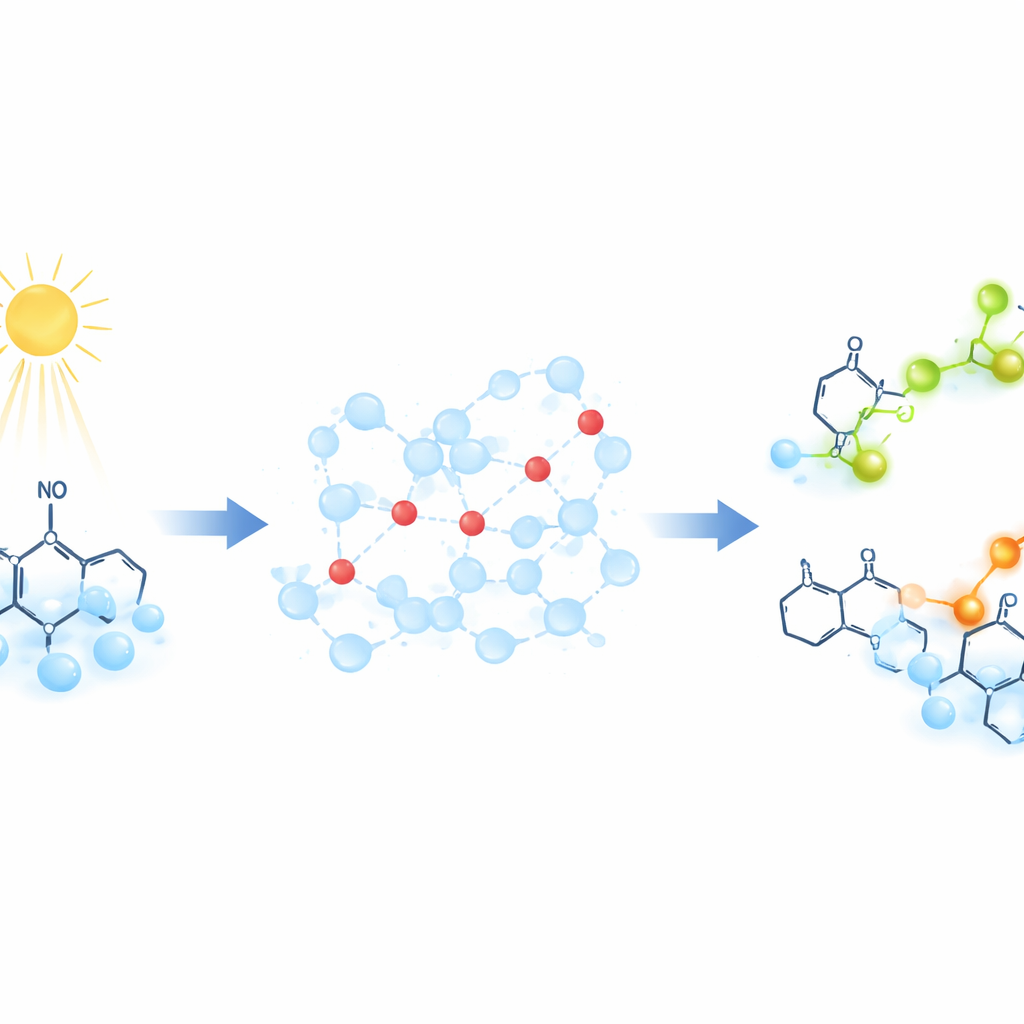
In plaats van protonen direct te volgen, gebruiken de onderzoekers speciale “probe”-moleculen die hun magnetische signatuur veranderen wanneer ze een proton opnemen. Deze probes zijn stabiele organische radicalen waarvan de ongepaarde elektron een goed gedefinieerd signaal in elektronparamagnetische resonantie (EPR) geeft — een techniek die detecteert hoe ongepaarde elektronen reageren op een magnetisch veld. Om protonbeweging op commando te starten, belicht het team een verbinding genaamd 2-nitrobenzaldehyde. Deze lichtgestuurde reactie geeft in minder dan een miljardste van een seconde een uitbarsting van protonen vrij en verlaagt plotseling de pH van de oplossing. Terwijl protonen zich door het water verspreiden en aan de probes binden, verschuift het EPR-signaal in de tijd, waardoor de wetenschappers kunnen volgen hoe snel protonoverdracht plaatsvindt.
Hoe de omgeving van water de stroom vertraagt of versnelt
Water komt zelden alleen voor; het is meestal omgeven door opgeloste zouten of andere moleculen die het netwerk van waterstofbruggen subtiel herschikken. Het team onderzocht hoe dergelijke toevoegingen protonbeweging beïnvloeden door zuiver water te vergelijken met oplossingen die kaliumchloride, ureum of guanidiniumchloride bevatten, allemaal in hoge concentraties. Door de EPR-veranderingen aan eenvoudige kinetische modellen te passen, bepaalden ze schijnbare snelheden voor protonoverdracht. Ze vonden dat in 6 molair guanidiniumchloride protonoverdracht ongeveer 40 keer langzamer was dan in zuiver water, terwijl 8 molair ureum slechts een bescheiden vertraging veroorzaakte en kaliumchloride tussentijdse effecten gaf. Omdat de snelheid waarmee protonen met de probes reageren wordt beperkt door hun beweging door het waterstofbrugnetwerk, wijzen deze verschillen op aanzienlijke veranderingen in hoe water rondom de toegevoegde ionen en moleculen is gestructureerd.
Protonbeweging in glasachtig ijs en binnen eiwitten
De methode is niet beperkt tot gewoon vloeibaar water. De auteurs bestudeerden ook een water–glycerolmengsel afgekoeld tot 160 kelvin, waar het een star glas vormt. Vrije diffusie van moleculen is in wezen bevroren, maar het EPR-signaal liet nog steeds zien dat de probes na lichtblootstelling worden gepotheerd. Dit suggereert dat protonoverdracht kan doorgaan zonder klassieke diffusie, mogelijk via kwantumtunneling langs een keten van waterstofbruggen, wat aansluit bij moderne verfijningen van het Grotthuss-idee. Om de biologische relevantie te onderzoeken, hechtten de onderzoekers een pH-gevoelig radicaal aan een specifieke plaats op het membraanprotein bacteriorhodopsine, op de grens tussen het eiwit en het omgevende water. Toen zij protonvrijgave met licht startten, observeerden ze een tijdsafhankelijke EPR-respons van deze gelabelde plaats, waarmee werd aangetoond dat hun benadering protonlevering naar een gedefinieerde positie op een eiwitoppervlak kan volgen.
Structuur, water en protonenroutes met elkaar verbinden
Om beter te begrijpen waarom de eiwitgebonden probe zich zeer vergelijkbaar gedroeg met een in bulkwater, voerden de onderzoekers computersimulaties uit van bacteriorhodopsine in een membraan en van een klein peptide in oplossing. Ze berekenden hoe watermoleculen de nitroxylgroep van het spinlabel omringen en vonden vrijwel identieke lokale hydratatiepatronen in beide gevallen, met slechts milde afscherming door de membraanomgeving. Dit betekent dat, althans voor de bestudeerde plaats, protonen toegang hebben via een waterlaag die sterk lijkt op gewoon vloeibaar water. De auteurs laten ook zien dat hun probes kunnen worden gebruikt in tijdsgeëigende EPR-experimenten, wat de deur opent om zowel proton- als elektronenbeweging tegelijkertijd te volgen in reacties waarin die twee sterk gekoppeld zijn.
Wat dit werk ons in eenvoudige bewoordingen vertelt
In wezen verandert deze studie licht in een scherp startschot voor protonbeweging en gebruikt vervolgens gevoelige magnetische probes om te zien hoe snel die protonen verschillende doelen bereiken. Door eenvoudige zoutoplossingen, dichte denaturanten, glasachtige mengsels en een membraanprotein te vergelijken, tonen de onderzoekers aan dat protonstroom sterk wordt bepaald door hoe watermoleculen zijn gerangschikt en door de omringende omgeving. Hun aanpak ondersteunt niet alleen het idee dat protonen hoppen langs netwerken van waterstofbruggen, maar laat ook zien dat dit hoppen kan voortduren zelfs wanneer normale moleculaire beweging vrijwel bevroren is. Deze nieuwe gereedschapsset kan wetenschappers helpen uit te zoeken hoe protonen bewegen in enzymen, energiewisselsystemen en nieuwe materialen, en brengt ons dichter bij het beheersen van deze kleine maar krachtige ladingsdragers.
Bronvermelding: Barbon, A., Savitsky, A., Grigoriev, I. et al. Photoinduced proton transfer in differently structured water: an EPR approach to solving a classic problem. Sci Rep 16, 7983 (2026). https://doi.org/10.1038/s41598-026-38650-0
Trefwoorden: protonoverdracht, waterstructuur, elektronparamagnetische resonantie, waterstofbrugnetwerk, bacteriorhodopsine