Clear Sky Science · nl
PLOD2 bevordert proliferatie, migratie en invasie van colorectale kankercellen via het PI3K‑AKT‑GSK3β‑signaleringspad
Waarom de omgeving rond een tumor ertoe doet
Colorectale kanker is een van de meest voorkomende vormen van kanker wereldwijd, en veel mensen krijgen pas een diagnose nadat de ziekte al gevorderd is. Deze studie kijkt verder dan de kankercellen zelf en onderzoekt hun omgevende “buurt” van ondersteunend weefsel. De onderzoekers richten zich op een weinig bekend enzym genaamd PLOD2 en tonen aan hoe het colorectale tumoren helpt groeien en verspreiden door zowel de weefselomgeving als belangrijke groeisignalen binnen de cellen te veranderen.
Een verborgen bouwer in het geraamte van de tumor
Onze organen worden ondersteund door een netwerk van eiwitten dat bekendstaat als de extracellulaire matrix, waarbij collageen het belangrijkste structurele bestanddeel is. PLOD2 is een enzym dat collageen chemisch wijzigt en helpt bij het vormen van sterke dwarsverbindingen en stijve vezels. Het team analyseerde grote genetische en proteïnedatabanken en onderzocht vervolgens weefselmonsters van 75 patiënten. Ze vonden dat PLOD2‑niveaus veel hoger waren in colorectaal kankergewebe dan in aangrenzend normaal weefsel. Hoge PLOD2 hing samen met meer gevorderde tumoren, uitzaaiing naar lymfeklieren en zenuwinvasie, en patiënten wiens tumoren meer PLOD2 bevatten, hadden over het algemeen een kortere overleving. Deze bevindingen maken PLOD2 tot een sterke kandidaat als merker voor agressieve ziekte.
Hoe PLOD2 kankercellen agressiever maakt
Om verder te gaan dan correlaties in patiëntmonsters, manipuleerden de onderzoekers colorectale kankercellijnen in het laboratorium. In het ene celtype verhoogden ze de PLOD2‑productie; in een ander schakelden ze het uit. Cellen met extra PLOD2 groeiden sneller, vormden meer kolonies en sloten kunstmatige “wonden” in kweekschalen sneller, wat een verbeterde beweeglijkheid aantoont. Ze migreerden ook gemakkelijker door poreuze membranen en drongen makkelijker door een gel die weefselbarrières nabootst dan controlecellen. Wanneer PLOD2 werd uitgeschakeld, verminderden al deze eigenschappen. Samen tonen deze experimenten aan dat PLOD2 actief de groei, migratie en invasie van kankercellen aanstuurt, in plaats van slechts een bijverschijnsel te zijn.
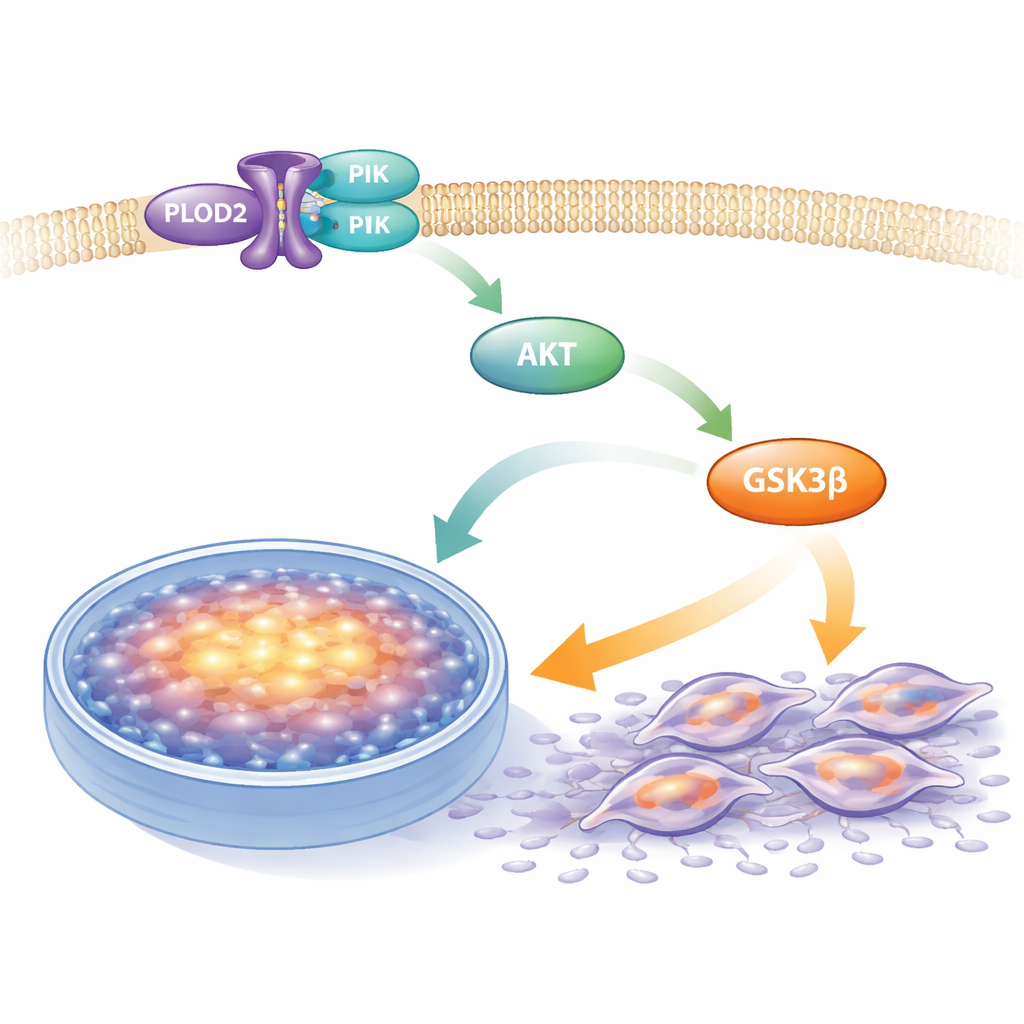
Een kankerversterende signaalketen inschakelen
In kankercellen worden veel processen geregeld door onderling verbonden signaalketens. Een centrale keten, algemeen bekend als het PI3K–AKT–GSK3β‑pad, helpt cellen te overleven, zich te delen en hun metabolisme aan te passen. Met data‑mining en biochemische tests ontdekten de onderzoekers dat PLOD2 nauw verbonden is met dit pad. Ze toonden aan dat PLOD2 fysiek bindt aan PI3K, het “starter”‑enzym in de keten. Wanneer PLOD2‑niveaus hoog waren, namen de geactiveerde (gefosforyleerde) vormen van PI3K, AKT en GSK3β toe, hoewel de totale hoeveelheid van elk eiwit gelijk bleef. Wanneer PLOD2 werd verminderd, daalde de activatie van dit pad, wat suggereert dat PLOD2 fungeert als een schakelaar die dit groeien‑en‑motiliteitssysteem inschakelt.
Het pad testen met chemische middelen
Om te bevestigen dat de schadelijke effecten van PLOD2 afhankelijk zijn van deze signaalketen, gebruikte het team geneesmiddelen die PI3K ofwel blokkeren ofwel stimuleren. In cellen die te veel PLOD2 producen, dempte een PI3K‑remmer de activatie van AKT en GSK3β en vertraagde de celgroei, beweging en invasie. In cellen waarin PLOD2 was uitgeschakeld, herstelde een PI3K‑activator de padactiviteit en herstelde gedeeltelijk het vermogen van de cellen om te prolifereren en te migreren. Hoewel het herstel niet volledig was — wat aangeeft dat PLOD2 mogelijk ook andere routes beïnvloedt — ondersteunen deze experimenten sterk het idee dat PLOD2 maligniteit vooral bevordert door in te voeden op de PI3K–AKT–GSK3β‑signaleringsas.
Wat dit betekent voor patiënten
Voor niet‑specialisten valt deze moleculaire informatie terug te brengen tot een eenvoudige kern: PLOD2 helpt colorectale kankercellen hun omgeving verharden en herstructureren terwijl het ook het gaspedaal indrukt van belangrijke interne groeicircuits. Door die dubbele werking maakt het tumoren vatbaarder voor agressieve groei en verspreiding. De studie suggereert dat het meten van PLOD2 kan helpen hoogrisicopatiënten te identificeren en dat geneesmiddelen die gericht zijn op PLOD2 zelf — of op de signaalketen die het activeert — mogelijk ooit deel kunnen uitmaken van meer gerichte behandelingen voor colorectale kanker. Meer werk in diermodellen en grotere patiëntengroepen is nodig, maar PLOD2 tekent zich nu af als een veelbelovende nieuwe aangrijpingsfactor bij een hardnekkige ziekte.
Bronvermelding: Fang, H., Zheng, J., Ren, S. et al. PLOD2 promotes proliferation, migration and invasion of colorectal cancer cells via PI3K-AKT-GSK3β signaling pathway. Sci Rep 16, 8118 (2026). https://doi.org/10.1038/s41598-026-38593-6
Trefwoorden: colorectale kanker, PLOD2, tumormicro‑omgeving, PI3K AKT signalering, kankermetastase