Clear Sky Science · nl
Geactiveerde T-cellen veroorzaken apoptose in A549-longadenocarcinoomcellen via TRPV4-gemedieerde calciuminflux
Waarom dit onderzoek belangrijk is voor longkanker
Longkanker behoort nog steeds tot de dodelijkste vormen van kanker, deels omdat tumoren vaak leren resistent te worden tegen standaardbehandelingen zoals chemotherapie en bestraling. De afgelopen jaren heeft het benutten van het eigen immuunsysteem nieuwe hoop geboden. Deze studie verkent een nieuwe invalshoek: ze laat zien hoe een specifiek type immuuncel, genaamd een geactiveerde T‑cel, longkankercellen kan dwingen tot zelfvernietiging door calciumopname via een moleculaire “poort” genaamd TRPV4 te stimuleren. Inzicht in deze route kan onderzoekers helpen krachtigere en preciezere immunotherapieën te ontwerpen.
Soldaten van het immuunsysteem ontmoeten longtumorcellen
De onderzoekers concentreerden zich op humane longadenocarcinoomcellen bekend als A549‑cellen, een veelgebruikt model voor niet-kleincellige longkanker. Ze koppelden deze kankercellen aan Jurkat T‑cellen, een model voor de killer T‑cellen van het lichaam, die normaal geïnfecteerde of kwaadaardige cellen opsporen en vernietigen. Door de Jurkat‑cellen chemisch te activeren, simuleerde het team de sterk waakzame staat van T‑cellen tijdens een echte immuunreactie. Vervolgens mengden ze geactiveerde of niet-geactiveerde T‑cellen met de longkankercellen in verschillende verhoudingen en volgden ze het verloop gedurende één tot drie dagen, met bijzondere aandacht voor hoeveel kankercellen overleefden en hoeveel geprogrammeerde celdood (apoptose) ondergingen.
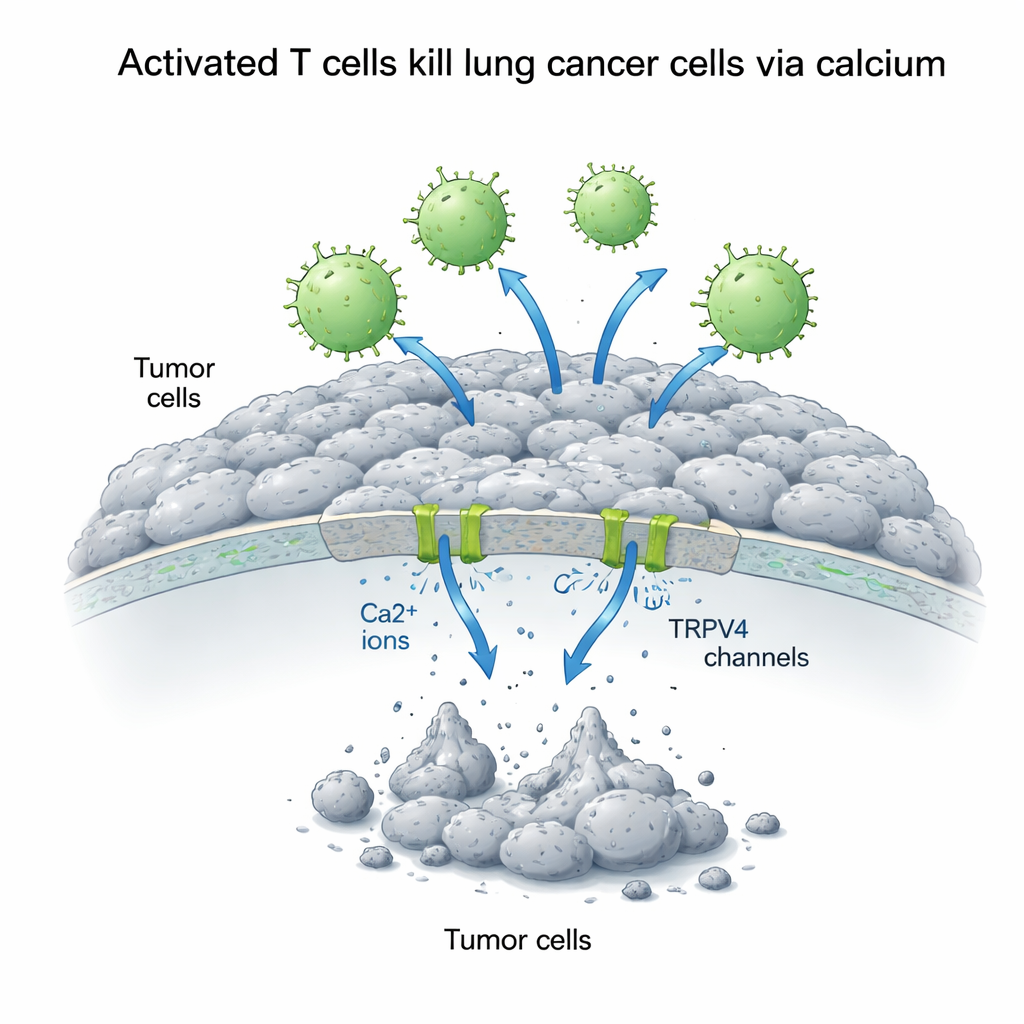
Calcium als een tweesnijdend signaal voor kankercellen
Calcium binnenin cellen functioneert als een veelzijdige signaalschakelaar die afhankelijk van de omstandigheden groei kan bevorderen of juist celdood kan veroorzaken. De wetenschappers verhoogden de hoeveelheid calcium buiten de A549‑cellen en maten hoe dit de interactie tussen T‑cellen en tumorcellen beïnvloedde. Verrassend genoeg bevorderde extra calcium op zichzelf de groei van de longkankercellen, wat suggereert dat calcium onder rustige omstandigheden overlevingsroutes aanwakkert. Maar wanneer geactiveerde T‑cellen aanwezig waren, keerde het beeld om: een hogere extracellulaire calciumconcentratie versterkte de door T‑cellen geïnduceerde celdoding dramatisch. Over 72 uur daalde de overleving van kankercellen tot minder dan een derde van normaal wanneer zowel geactiveerde T‑cellen als extra calcium werden gecombineerd, terwijl niet-geactiveerde T‑cellen weinig effect hadden en bij toevoeging van calcium zelfs de groei konden ondersteunen.
Een calcium “poort” gekoppeld aan stress en celdood
Om te begrijpen hoe de omschakeling van groei naar dood plaatsvindt, richtte het team zich op TRPV4, een eiwitkanaal in het celmembraan dat calcium binnenlaat. Met behulp van proteïneanalyse ontdekten ze dat TRPV4‑niveaus scherp toenamen wanneer A549‑cellen werden blootgesteld aan extra calcium, zowel met als zonder T‑cellen, en dat de niveaus het hoogst waren wanneer calcium en geactiveerde T‑cellen samen voorkwamen. Tegelijkertijd vertoonden de kankercellen duidelijke tekenen van oxidatieve stress: het evenwicht schoof weg van beschermende antioxidanten (lagere totale antioxidantcapaciteit) en in de richting van schadelijke oxidanten (hogere totale oxidantenstatus). Flowcytometrie, een techniek die cellen markeert met fluorescerende kleurstoffen, bevestigde dat geactiveerde T‑cellen zowel vroege als late stadia van apoptose veroorzaakten, vooral wanneer calcium overvloedig aanwezig was. Samen wijzen deze observaties op een reeks gebeurtenissen waarbij TRPV4‑kanalen meer calcium binnenlaten, wat vervolgens chemische stress in de cel veroorzaakt en de cel naar de dood duwt.
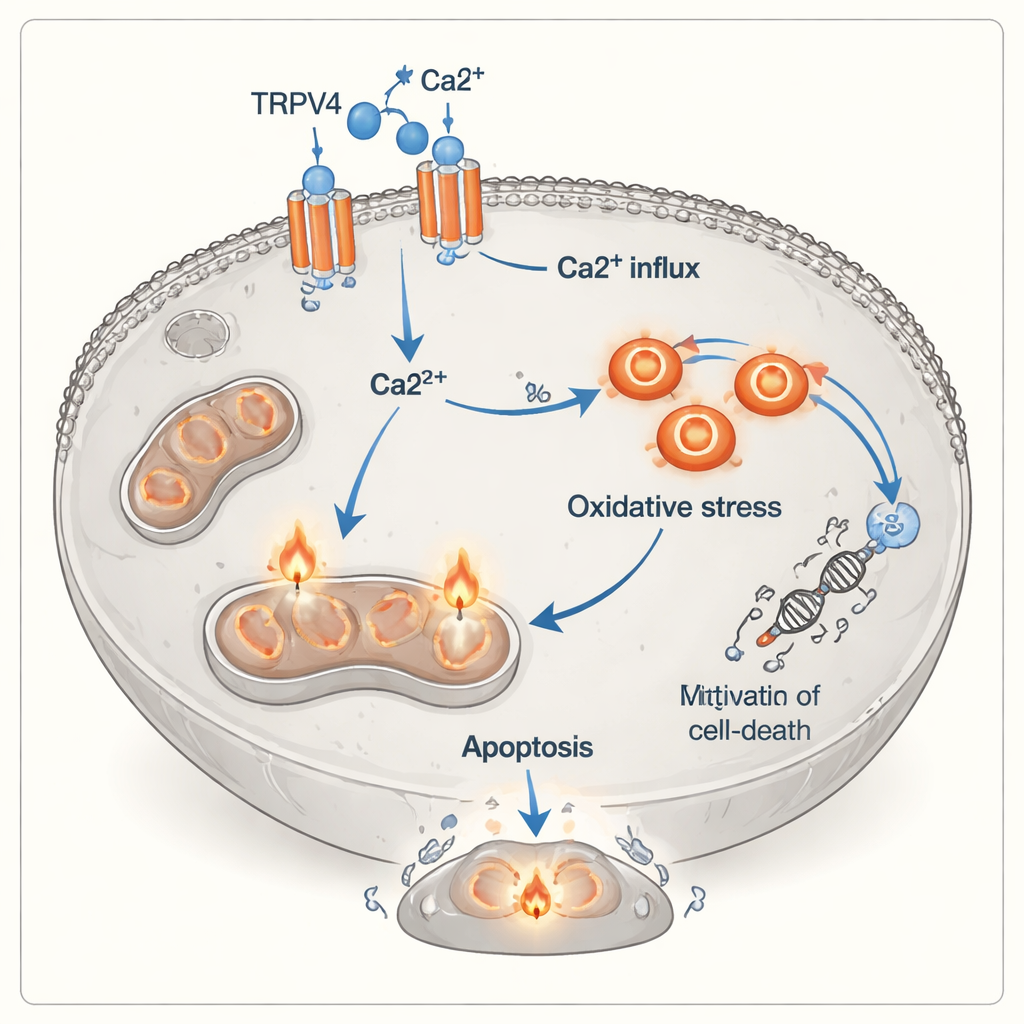
Een nieuwe laag in hoe immuuncellen tumoren doden
Traditioneel vernietigen killer T‑cellen hun doelen door toxische eiwitten vrij te geven of door death‑receptoren op het celoppervlak van de kankercel te activeren. Deze studie suggereert dat er een andere, meer indirecte route bestaat: signalen van geactiveerde T‑cellen — waaronder inflammatoire moleculen en nauw cel‑tot‑cel contact — lijken longkankercellen gevoeliger te maken voor TRPV4 en kwetsbaarder voor calciumoverbelasting en oxidatieve schade. In deze zienswijze fungeert TRPV4 als een sensitiverende schakelaar die calcium, dat anders groeibevorderend is, in een dodelijk signaal verandert. Hoewel de experimenten in kweekschalen zijn uitgevoerd en één kankercellijn gebruiken, benadrukken ze een potentiële brug tussen immuunaanval, ionkanalen en de interne stressmechanismen van tumorcellen.
Wat dit kan betekenen voor toekomstige behandelingen
Voor niet‑specialisten is de conclusie dat het succes van immunotherapie mogelijk niet alleen afhangt van het versterken van T‑cellen, maar ook van het vergemakkelijken van de vernietiging van kankercellen. Door TRPV4 of verwante calciumkanalen te targeten, zouden artsen ooit de capaciteit van T‑cellen kunnen vergroten om longtumoren uit te schakelen of behandelingen kunnen verfijnen om schade aan gezonde weefsels te vermijden. Het werk bevindt zich nog in een vroeg stadium en de auteurs benadrukken de noodzaak van vervolgexperimenten in diermodellen en complexere systemen. Desondanks voegt de ontdekking van een TRPV4–calcium–oxidatieve stress‑as een veelbelovend nieuw doelwit toe aan de gereedschapskist voor het verbeteren van op immuniteit gebaseerde therapieën tegen longkanker.
Bronvermelding: Alavi, F., Kazemi-Lomedasht, F., Eftekhari, Z. et al. Activated T cells induce apoptosis in A549 lung adenocarcinoma cells via TRPV4-mediated calcium influx. Sci Rep 16, 7155 (2026). https://doi.org/10.1038/s41598-026-38589-2
Trefwoorden: immunotherapie bij longkanker, T-cellen, calciumsignalering, TRPV4-kanaal, oxidatieve stress