Clear Sky Science · nl
Mesoporeuze silicium-micropartikels versterken antivirale immuniteit en geheugenantwoorden tegen SARS-CoV-2
Waarom piepkleine siliciumdeeltjes belangrijk zijn voor toekomstige vaccins
Naarmate de wereld vooruitkijkt voorbij de eerste golf van COVID-19-vaccins, zoeken wetenschappers naar manieren om bescherming langer te laten duren en beter te laten werken tegen ernstige ziekte. Deze studie onderzoekt een onverwachte hulp: microscopische, sponsachtige deeltjes van silicium die gemengd kunnen worden met coronavirus-eiwitten. Deze deeltjes werken als een versterker voor het immuunsysteem en zijn bedoeld om sterkere, duurzamere afweer te creëren dan veel huidige vaccinadditieven, terwijl ze veilig en gemakkelijk te produceren blijven.
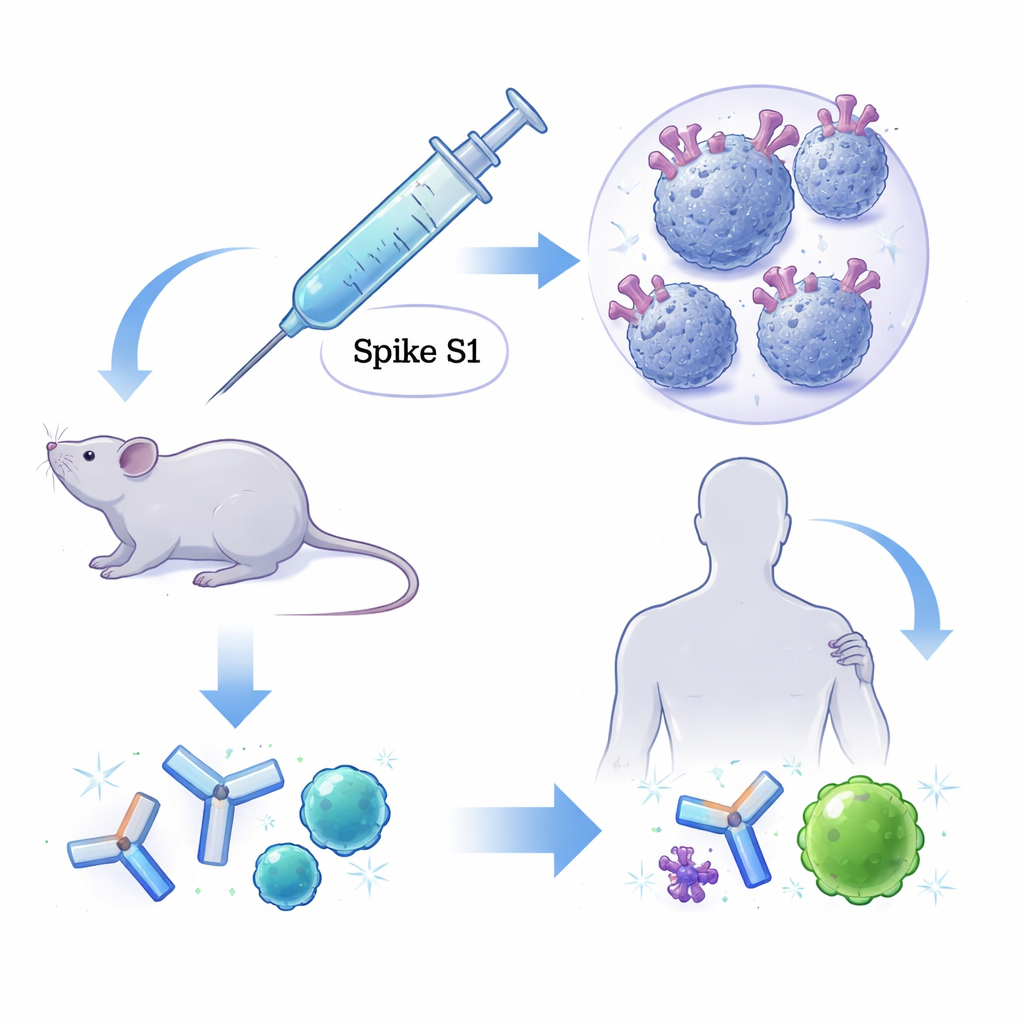
Een beter vaccinhulpje bouwen
De meeste moderne vaccins gebruiken geen hele virussen; in plaats daarvan vertrouwen ze op gezuiverde onderdelen zoals het spike-eiwit van SARS-CoV-2. Op zichzelf kunnen deze onderdelen te zwak zijn om een blijvende afweer op te roepen, dus worden ze gecombineerd met additieven die adjuvantia worden genoemd en die het immuunsysteem alarmeren en trainen. Aluminiumsalzen vervullen deze rol al bijna een eeuw, maar ze bevoordelen meestal slechts één deel van de respons en zijn niet ideaal om sterke antivirale geheugenantwoorden op te wekken. Het team achter dit werk ontwikkelde “mesoporeuze silicium-micropartikels” — kruimelachtige fragmenten van silicium vol met kleine poriën — die geladen kunnen worden met het S1-deel van het spike-eiwit. Hun grootte, hoge oppervlak en langzaam vrijkomende eigenschappen zijn ontworpen om ze aantrekkelijk te maken voor immuuncellen die het lichaam patrouilleren.
Sterkere en langduriger antilichamen in muizen
De onderzoekers vergeleken siliciumgebaseerde vaccinmengsels met standaard op aluminium gebaseerde mengsels in muizen. Gedurende meer dan zes maanden produceerden beide versies vergelijkbare niveaus van antilichamen tegen het spike S1-eiwit, en lieten ze duidelijk betere resultaten zien dan het spike-eiwit alleen. Belangrijk is dat na een late boosterdosis de siliciumformulering een duidelijke stijging veroorzaakte van een bepaald type antilichaam dat gekoppeld is aan antivirale, cel-dodende reacties, en deze antilichamen waren bijzonder goed in het blokkeren van het spike-eiwit om zich aan de menselijke ACE2-receptor te hechten — de eerste stap van infectie. Terwijl de muisantilichamen goed werkten tegen de originele, Beta- en Delta-varianten van het virus, neutraliseerden ze Omicron niet goed, wat weerspiegelt hoe ver het spike-eiwit van die variant is afgedwaald van de oorspronkelijke stam die voor immunisatie werd gebruikt.
Het mobiliseren van de cellulaire verdedigers van het lichaam
Antilichamen vormen slechts een deel van het verhaal; langdurige bescherming tegen virussen hangt ook af van T-cellen die geïnfecteerde cellen kunnen herkennen en vernietigen. Toen de wetenschappers immuuncellen van gevaccineerde muizen onderzochten, ontdekten ze dat muizen die de siliciumgebaseerde formulering kregen meer van het antivirale boodschapperstofje interferon-gamma produceerden, met name van T-cellen die geassocieerd zijn met directe vernietiging van geïnfecteerde cellen. Dit wees op een sterke cellulaire respons die minstens zeven maanden aanhield en duidelijk sterker was dan bij aluminium. In een strenge proef met genetisch gemodificeerde muizen die zeer gevoelig zijn voor SARS-CoV-2, beschermden zowel de silicium- als de aluminiumgebaseerde vaccins de meeste dieren tegen een dodelijke uitdaging, en verminderden ze het virusniveau in longen en hersenen sterk vergeleken met niet-gevaccineerde controles.
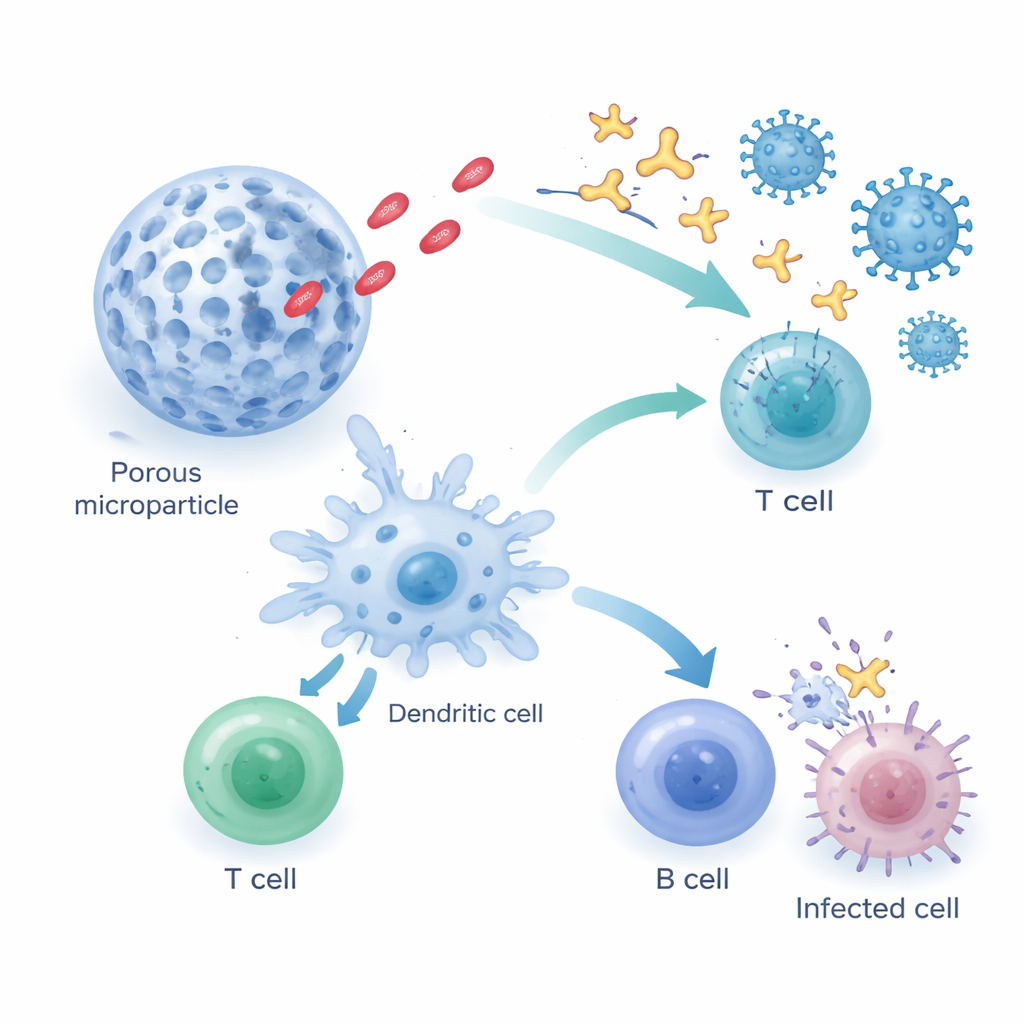
Aanwijzingen van menselijke immuuncellen
Om te onderzoeken of deze deeltjes ook de menselijke immuniteit zouden kunnen helpen, verzamelde het team bloedcellen van vrijwilligers die eerder waren geïnfecteerd met of gevaccineerd tegen SARS-CoV-2. In het laboratorium stelden ze deze cellen bloot aan spike-afgeleide fragmenten, ofwel vrij zwevend of bevestigd aan de siliciumdeeltjes. Wanneer de virale fragmenten door het silicium werden gedragen, schakelden meer T-cellen van gevaccineerde donoren over op de productie van interferon-gamma, vooral wanneer ze werden ondersteund door dendritische cellen — de professionele wachtposten van het immuunsysteem. Deze resultaten suggereren dat de deeltjes kunnen helpen bestaand immunologisch geheugen te heractiveren en mogelijk goed geschikt zijn om reacties te versterken bij mensen die het virus of een eerder vaccin al hebben ontmoet.
Wat dit zou kunnen betekenen voor toekomstige vaccins
Samen genomen schetsen de muis- en menselijke celgegevens mesoporeuze silicium-micropartikels als veelbelovende hulpstoffen voor de volgende generatie vaccins. Ze evenaren aluminiumsalzen wat betreft de algehele antilichaamproductie, overtreffen ze na een vertraagde boost in het genereren van krachtige, antivirale antilichaamtypes, en bieden sterkere ondersteuning voor duurzame T-celresponsen — en dat alles terwijl ze gemaakt zijn van een biologisch afbreekbaar, laag-toxisch materiaal dat op schaal geproduceerd kan worden. Voor een leek is de boodschap dat zorgvuldig ontworpen siliciumkruimels toekomstige vaccins kunnen helpen niet alleen hogere schilden op te werpen tegen virussen zoals SARS-CoV-2, maar ook het immuunsysteem te leren die bedreigingen dieper en langer te onthouden.
Bronvermelding: López-Gómez, A., Real-Arévalo, I., Mayol-Hornero, E. et al. Mesoporous silicon microparticles enhance antiviral immunity and memory responses against SARS-CoV-2. Sci Rep 16, 7355 (2026). https://doi.org/10.1038/s41598-026-38583-8
Trefwoorden: COVID-19-vaccins, vaccin-adjuvantia, siliciummicropartikels, antivirale immuniteit, immunologisch geheugen