Clear Sky Science · nl
Histatin-1 bevordert de expressie van markers geassocieerd met odontoblastische differentiatie in de pulpa en apicale papil
Waarom speeksel je tanden misschien kan redden
Wanneer een tand ernstig beschadigd is door cariës of letsel, proberen tandartsen het te behouden door het zachte binnenweefsel, de pulpa, te beschermen. De droom van toekomstige tandheelkunde is dat de tand zichzelf herstelt en de harde dentinelaag herbouwt in plaats van alleen te vertrouwen op vullingen en kronen. Deze studie onderzoekt of een natuurlijk eiwit in menselijk speeksel, histatin‑1 genaamd, cellen in jonge tanden kan aanzetten om te veranderen in dentine-vormende cellen en zo het herstel van binnenuit kan bevorderen.
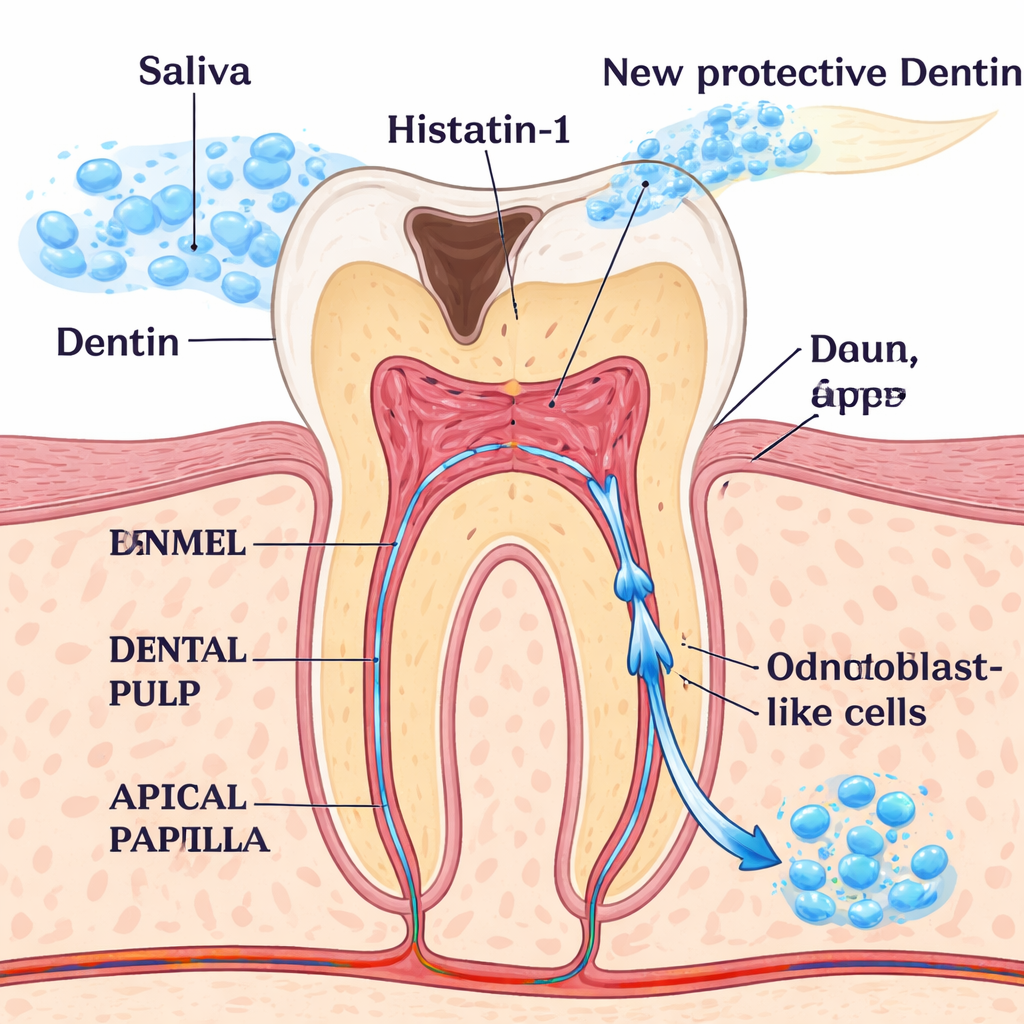
Verborgen reparatieteams in jonge tanden
In elke tand bevatten de tandpulpa en een aangrenzende regio bij de worteltip, de apicale papil, veelzijdige cellen die kunnen rijpen tot verschillende celtypen. Een van de belangrijkste zijn odontoblasten, de gespecialiseerde cellen die dentine opbouwen en onderhouden, het harde beschermende weefsel onder het glazuur. Bij diepe caries of trauma raken odontoblasten beschadigd of gaan ze verloren, en succesvolle regeneratieve behandelingen hangen af van het vervangen van hun functie. Wetenschappers zoeken al lang naar veilige signalen die pulpa- en apicale papilcellen in de richting van een odontoblast‑achtige staat duwen zodat ze de tand van binnenuit kunnen herbouwen.
Een speekseleiwit met verrassende talenten
Histatin‑1 staat vooral bekend als een klein eiwit in speeksel dat tanden beschermt tegen microben en wondgenezing bevordert. Eerder werk toonde aan dat het ook botgerelateerde cellen kan stimuleren om te bewegen, zich te hechten en mineralen af te zetten, wat erop wijst dat het mogelijk breder invloed heeft op de vorming van harde weefsels. De auteurs van deze studie onderzochten of histatin‑1 specifiek pulpa- en apicale papilcellen uit onvolgroeide blijvende tanden kon aanzetten richting een odontoblast‑achtige identiteit, in plaats van slechts een algemene botachtige toestand. Als dat zo is, zou deze uit speeksel afkomstige molecule een natuurlijk hulpmiddel kunnen worden voor gerichte tandheelkundige regeneratie.
Pulpacellen omzetten in dentinebouwers
Om deze gedachte te testen, verkregen de onderzoekers recent verwijderde onvolgroeide kiesjes en splitsten ze het pulpa–apicale papilcomplex van elke tand in tweeën, waarbij de ene helft werd behandeld met histatin‑1 en de andere als controle diende. Na een week onderzochten ze beide weefsels onder de microscoop. Histatin‑1‑behandelde monsters vertoonden meer van twee kenmerkende dentine-eiwitten—DSPP en DMP1—en meer cellen die positief kleurden voor deze markers, vooral in de apicale papil. Toen het team de residentiële mesenchymale cellen isoleerde en in kweek bracht, verhoogde histatin‑1 opnieuw de DSPP-niveaus en nam de activiteit van bèta‑catenine toe, een signaalmolecuul dat bekendstaat om het stimuleren van tandcelrijping. Onder de microscoop kregen behandelde cellen ook vormkenmerken die gezien worden bij ontwikkelende odontoblasten: meer primaire cilieën—kleine antenneachtige uitstulpingen—en een meer gefocusseerd, gepolariseerd Golgi‑apparaat, wat suggereert dat de cellen zich voorbereiden om dentinematrix in één richting uit te scheiden.
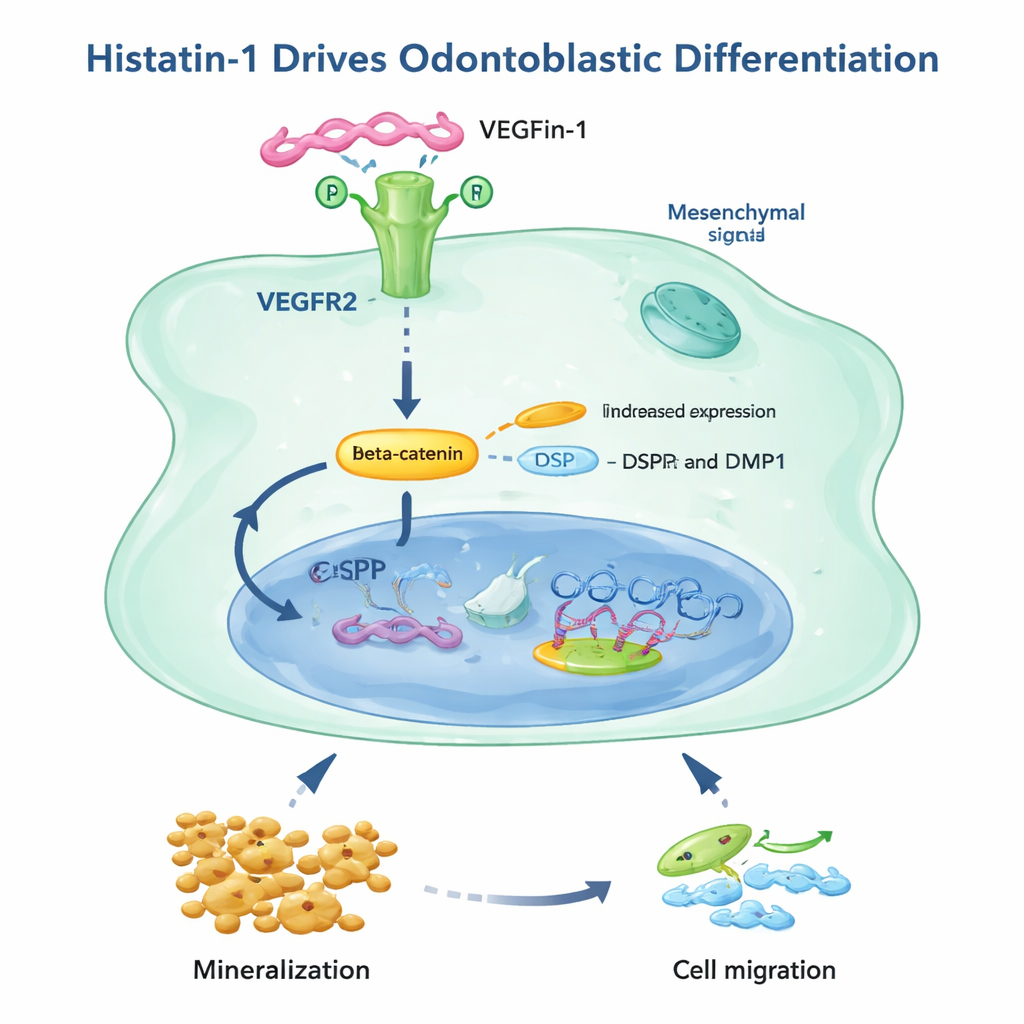
Hoe histatin‑1 het signaal afgeeft
De studie vervolgde met de vraag hoe histatin‑1 zijn boodschap overbrengt. Eerder onderzoek had een receptor op celoppervlakken geïdentificeerd, VEGFR2, die aan histatin‑1 kan binden. Hier bevestigden de onderzoekers dat zowel pulpa- als apicale papilweefsels VEGFR2 tot expressie brengen en dat histatin‑1 de niveaus verhoogt. Het blokkeren van VEGFR2 met een specifiek medicijn, of het gebruik van een gemodificeerde vorm van histatin‑1 die niet langer aan deze receptor kan binden, verminderde sterk het vermogen van histatin‑1 om mineralisatie in deze cellen te stimuleren. Dezelfde receptor bleek ook cruciaal voor histatin‑1‑gedreven celbeweging in apicale papilcellen, hoewel pulpacellen schijnbaar een extra, VEGFR2‑onafhankelijke manier hadden om te migreren. Al met al wijzen de bevindingen op een route waarbij histatin‑1 aan VEGFR2 bindt, bèta‑catenine‑signaal versterkt, odontoblastmarkers inschakelt en zowel mineralisatie als beweging van sleutelcellen voor reparatie bevordert.
Wat dit kan betekenen voor toekomstige tandheelkunde
Voor niet‑specialisten is de kernboodschap dat een natuurlijk bestanddeel van speeksel jonge tandcellen kan instrueren zich als dentinebouwers te gedragen via een gedefinieerde signaalweg. Hoewel dit werk is uitgevoerd in cel- en weefselmonsters en niet bij patiënten, identificeert het histatin‑1 als een veelbelovende, ogenschijnlijk weefselvriendelijke kandidaat voor regeneratieve tandheelkundige therapieën. In de toekomst zouden op maat gemaakte gels, spoelingen of pulp‑capping materialen met histatin‑1 de cellen van de tand kunnen begeleiden om naar beschadigde gebieden te migreren en verloren dentine te herbouwen, wat een meer biologische alternatief biedt voor traditionele restauratieve ingrepen.
Bronvermelding: Silva, P., Garrido, M., Tapia, H.A. et al. Histatin-1 promotes the expression of markers associated with odontoblastic differentiation in the dental pulp and apical papilla. Sci Rep 16, 7360 (2026). https://doi.org/10.1038/s41598-026-38578-5
Trefwoorden: tandheelkundige regeneratie, histatin-1, odontoblasten, tandpulpa stamcellen, reparatie van dentine