Clear Sky Science · nl
Integratieve analyse van het transcriptoom en single-cell sequencing gecombineerd met experimentele validatie identificeert biomarkers geassocieerd met T-cellen en veroudering bij sepsis
Waarom dit onderzoek belangrijk is voor patiënten met ernstige infecties
Sepsis is een levensbedreigende reactie op een infectie die een routineziekte of -verwonding binnen enkele uren in een spoedsituatie kan veranderen. Artsen missen nog steeds een eenvoudige, betrouwbare manier om te herkennen welke patiënten afglijden richting orgaanfalen, en er zijn geen geneesmiddelen ontwikkeld die specifiek gericht zijn op het herstellen van de immuunchaos die sepsis veroorzaakt. Deze studie onderzoekt hoe bepaalde immuuncellen, zogenaamde T-cellen, en de veroudering van deze cellen sepsis kunnen aansturen — en identificeert een kleine set genen die artsen kunnen helpen de aandoening eerder te diagnosticeren en die aanwijzingen geven voor nieuwe behandelingen.
Sepsis: wanneer de verdediging van het lichaam ontspoort
Bij sepsis explodeert het immuunsysteem eerst in een intense ontstekingsreactie en schakelt dan vaak over naar een gevaarlijke uitval. T-cellen, die normaal helpen infecties te verwijderen en zich eerdere infecties te herinneren, worden minder talrijk en minder effectief. Tegelijkertijd vertonen veel immuuncellen tekenen van “senescentie” — een vorm van cellulaire veroudering waarin cellen stoppen met delen maar doorgaan met het afgeven van ontstekingssignalen. De auteurs stelden dat als ze genen konden aanwijzen die zowel met T-cellen als met senescentie samenhangen, ze nieuwe biomarkers konden ontdekken die onthullen wie sepsis ontwikkelt en waarom sommige patiënten sneller verslechteren dan anderen.
Het bloed onderzoeken op het niveau van individuele cellen
Het team combineerde meerdere datalagen uit bloedmonsters van mensen met en zonder sepsis. Ze gebruikten eerst bulk-transcriptoomgegevens (een weergave van welke genen aan staan) om bijna 10.000 genen te vinden die hun activiteit veranderden bij sepsis. Vervolgens onderzochten ze met single-cell RNA-sequencing tienduizenden individuele bloedcellen om meer dan 1.300 genen te identificeren die specifiek veranderd waren in T-cellen. Door deze sets te overlappen met een samengestelde lijst van 866 genen die bekendstaan om betrokken te zijn bij cellulaire veroudering, beperkten ze de selectie tot 45 kandidaten die op het kruispunt van sepsis, T-cellen en senescentie lagen. 
Vier belangrijke genetische bakenpunten gevonden
Om deze lijst verder te filteren pasten de onderzoekers twee machine-learningtechnieken toe die zoeken naar de meest informatieve kenmerken in complexe data. Deze benaderingen convergeerden naar zes veelbelovende genen, en toen het team twee onafhankelijke patiëntdatasets controleerde, staken vier daarvan consequent met kop en schouders boven de rest uit: PATZ1, SIN3B, BLK en MTHFD2. In openbare gegevens waren PATZ1, SIN3B en BLK verlaagd bij sepsis, terwijl MTHFD2 verhoogd was. In een kleine reeks klinische monsters getest met een gevoelige methode genaamd RT-qPCR, waren de eerste drie genen opnieuw duidelijk lager in het bloed van sepsispatiënten, terwijl MTHFD2 geen duidelijk verschil liet zien — wat suggereert dat de rol ervan mogelijk meer te maken heeft met eiwitfunctie dan met de hoeveelheid die wordt geproduceerd.
Hoe deze genen verband houden met immuunbalans en mogelijke geneesmiddelen
Verdere analyses verbonden elk gen met bredere biologische routes. PATZ1 werd gekoppeld aan DNA-replicatie en T-celreceptor-signalisering, processen die essentieel zijn voor T-cellen om zich te vermenigvuldigen en op infecties te reageren. SIN3B werd geassocieerd met een lipiden-gebaseerd signaleringssysteem dat invloed heeft op celdood en ontsteking. BLK, beter bekend uit auto-immuunziekten, hing samen met bloedcelontwikkeling en darmafweer, inclusief de productie van IgA-antilichamen die de intestinale barrière beschermen. MTHFD2 werd gekoppeld aan machinerie voor eiwitsynthese en -afbraak, centraal voor hoe immuuncellen hun metabolisme bij stress aanpassen. Toen het team patronen van immuuncel-infiltratie in bloed onderzocht, ging een hogere PATZ1-expressie gepaard met meer CD8-T-cellen en minder neutrofielen, een balans die mogelijk betere infectiebeheersing bevordert. Met behulp van deze vier genen bouwden de onderzoekers een kunstmatig neuraal netwerk — een eenvoudig AI-model — dat sepsis onderscheidde van niet-sepsisgevallen in twee externe datasets met bijna perfecte nauwkeurigheid. Ze gebruikten ook een geneesmiddel–gen database en moleculaire docking-simulaties om verschillende bestaande verbindingen voor te stellen, waaronder het antibioticum latamoxef en de moleculen emetine en dihydroergotamine, als kandidaten die sterk aan deze doelen binden. 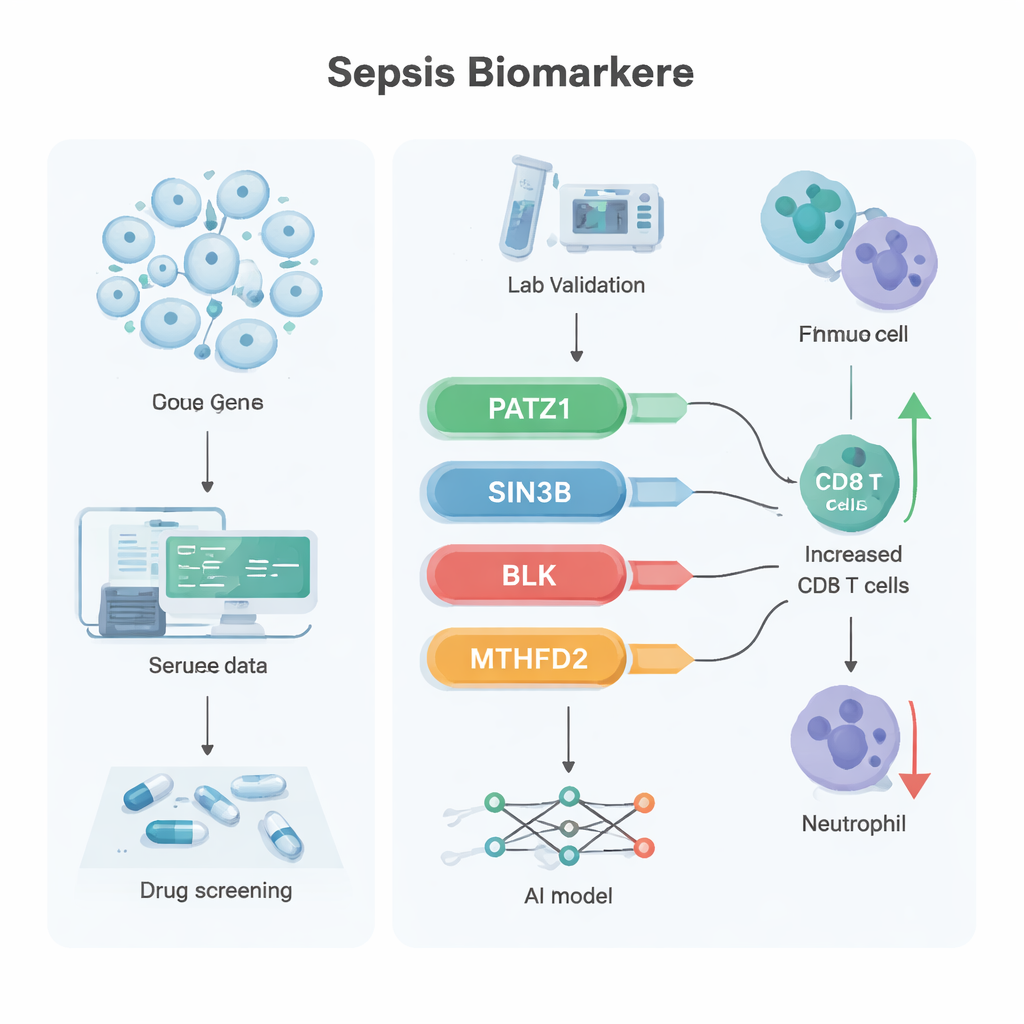
Wat dit kan betekenen voor toekomstige zorg
Voor een leek is de belangrijkste conclusie dat deze studie vier genen identificeert die fungeren als waarschuwingsbakens op T-cellen die fout gaan en vroegtijdig verouderen tijdens sepsis. Samen vormen deze genen een potentiële bloedtestpanel die artsen mogelijk op termijn kan helpen sepsis eerder en nauwkeuriger te diagnosticeren dan de huidige instrumenten. Ze geven ook aanwijzingen over hoe het energiegebruik en de reparatiemechanismen van het immuunsysteem falen, wat nieuwe invalshoeken biedt voor geneesmiddelen die gericht zijn op het herstellen van gezonde T-celfunctie in plaats van alleen het onderdrukken van ontsteking. Hoewel grotere studies en laboratoriumexperimenten nodig zijn voordat een van deze bevindingen de kliniek bereikt, effent dit werk een veelbelovende weg naar meer precieze, op biologie gebaseerde diagnose en behandeling van sepsis.
Bronvermelding: Yang, K., Hu, Y., Ma, C. et al. Integrative analysis of transcriptome and single-cell sequencing combined with experimental validation identifies biomarkers associated with T cell and senescence in sepsis. Sci Rep 16, 7109 (2026). https://doi.org/10.1038/s41598-026-38559-8
Trefwoorden: sepsis biomarkers, T-cellen, immuunsenescentie, single-cell sequencing, immunometabolisme