Clear Sky Science · nl
Vergelijking en combinatie van xevinapant met ATR- en PARP-remming voor de radiosensitisatie van HPV-negatieve HNSCC-cellen
Waarom het versterken van bestraling ertoe doet
Radiotherapie is een hoeksteen van de behandeling van kanker in mond en keel, maar veel tumoren zijn ertegen resistent, waardoor artsen hoge doses moeten inzetten die gezond weefsel kunnen beschadigen. Deze studie stelt een praktische vraag met grote implicaties voor patiënten: van verschillende moderne kankergeneesmiddelen die zijn ontworpen om kankercellen gevoeliger te maken, welke werken daadwerkelijk het beste in combinatie met bestraling tegen hardnekkige, HPV‑negatieve hoofd‑ en halskankers gekweekt in het laboratorium?
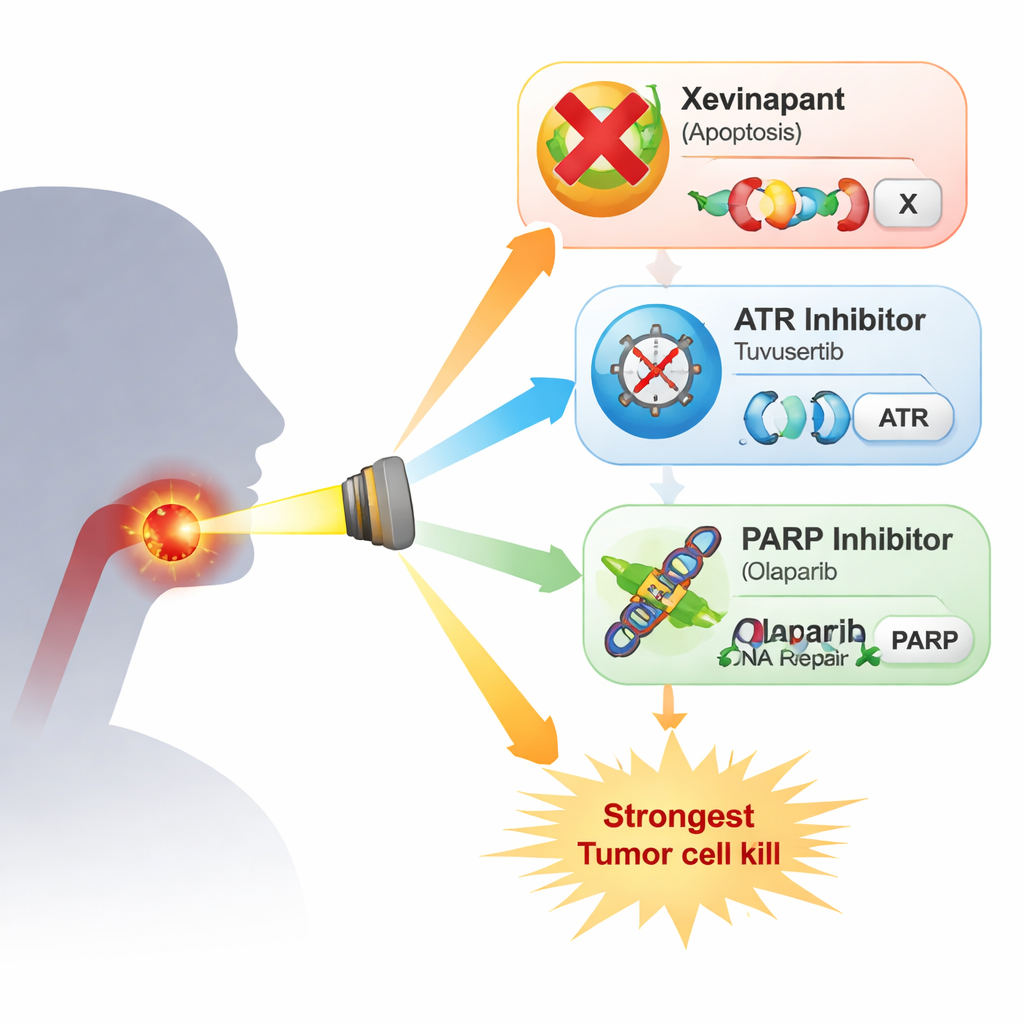
Huidige behandeling en de beperkingen ervan
Mensen met lokaal gevorderd plaveiselcelcarcinoom van hoofd en hals worden vaak behandeld met een combinatie van bestraling en het chemotherapeuticum cisplatin, of met chirurgie gevolgd door bestraling. Hoewel deze aanpak de ziekte kan beheersen, laat ze vaak patiënten achter met ernstige blijvende bijwerkingen zoals slikproblemen, een droge mond, gehoorproblemen en nierschade. Veel oudere of medisch kwetsbare patiënten kunnen helemaal geen cisplatin verdragen. Dat heeft geleid tot grote belangstelling voor “radiosensitizers” – middelen die tumorcellen makkelijker te doden maken met bestraling, zodat de behandeling effectiever of mogelijk minder belastend kan zijn.
Een veelbelovend middel dat struikelde
Een van die middelen, xevinapant, werd aanvankelijk geprezen als een doorbraak. Het bootst een natuurlijk eiwit genaamd SMAC na en blokkeert moleculen die kankercellen helpen het geprogrammeerde celdoodpad te omzeilen. In eerder werk verbeterde het toevoegen van xevinapant aan standaard chemoradiatie de uitkomsten in een fase‑2 klinische studie voor hoofd‑ en halskanker, wat de hoop wekte dat het een nieuwe standaard zou kunnen worden. Maar een veel grotere fase‑3 studie, TrilynX, werd voortijdig stopgezet toen tussentijdse gegevens niet alleen een gebrek aan voordeel, maar zelfs slechtere overleving en meer bijwerkingen in de xevinapant‑groep lieten zien. Die onverwachte mislukking maakte het dringend noodzakelijk om opnieuw te beoordelen hoe goed xevinapant de bestraling daadwerkelijk ondersteunt, en om het te vergelijken met andere, nieuwere strategieën.
Drie strategieën onderling vergeleken
De onderzoekers bestudeerden vier bestraling‑resistente HPV‑negatieve hoofd‑ en halskankercellijnen. Ze vergeleken xevinapant met twee middelen die de DNA‑schade‑reactie van de cel aanpakken: de ATR-remmer tuvusertib en de PARP‑remmer olaparib, beide gebruikt op doses vergelijkbaar met wat in patiënten haalbaar is. ATR en PARP zijn sleutelspelers die cellen helpen de celcyclus te pauzeren en DNA te herstellen na schade zoals die door röntgenstralen wordt veroorzaakt. In eenvoudige groeiproeven vertraagde elk middel alleen de celdeling slechts bescheiden, en de patronen verschilden tussen de cellijnen. In combinatie met bestraling, in de strengste test—tellen hoeveel enkele cellen nog in staat zijn uit te groeien tot kolonies—verscherpte het beeld: xevinapant gaf in meerdere lijnen slechts een milde of geen extra bestralingswerking, terwijl zowel tuvusertib als olaparib de bestraling consequent dodelijker maakten. Het sterkste effect werd gezien bij het combineren van ATR‑ en PARP‑remming, wat vooral diepe dalingen in kolonievorming opleverde in drie van de vier cellijnen.
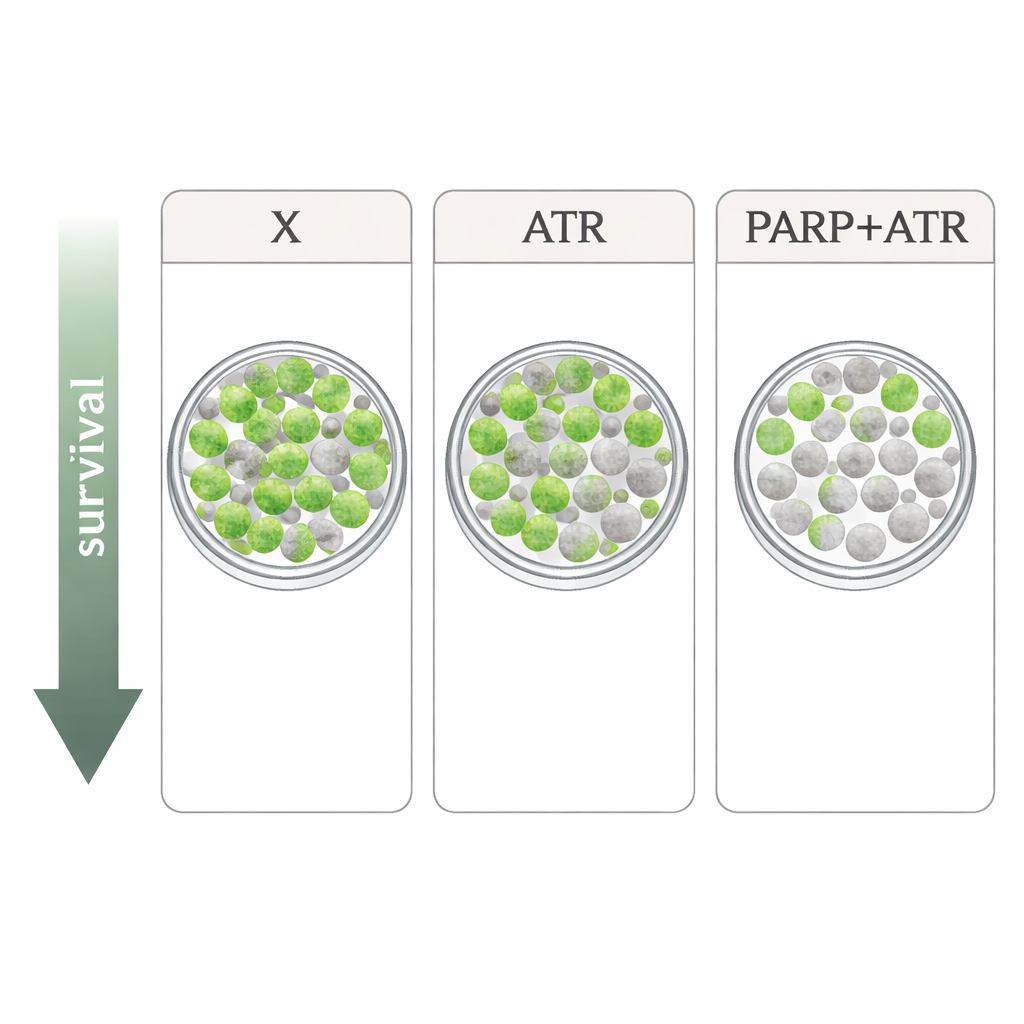
Celsterftesignalen vertellen niet het hele verhaal
Aangezien xevinapant bedoeld is om celdood te induceren, maten de onderzoekers ook hoeveel cellen apoptotisch werden of lysatie vertoonden na behandeling, met en zonder bestraling. Deze markers van celdood namen in sommige situaties duidelijk toe—vooral in één cellijn genaamd HSC4 en wanneer middelen werden gecombineerd—maar ze correleerden niet betrouwbaar met hoe goed bestraling op de lange termijn de overleving onderdrukte. Met andere woorden, de kortetermijnmetingen van celdood waren slechte voorspellers van echte radiosensitisatie. Deze discrepantie benadrukt een belangrijke les voor geneesmiddelenontwikkeling: alleen assays die cellen lang genoeg volgen om te zien of ze zich kunnen hergroeperen—zoals kolonievormingstests—kunnen correct beoordelen of een radiosensitizer effectief is.
Wat dit betekent voor toekomstige behandelingen
Uit deze laboratoriumexperimenten blijkt dat xevinapant enige capaciteit heeft om bestraling te versterken in HPV‑negatieve hoofd‑ en halskankercellen, maar de impact was zwakker en minder consistent dan benaderingen die rechtstreeks het DNA‑schade‑beheer via ATR en PARP verstoren. Het combineren van ATR‑ en PARP‑remmers gaf het krachtigste effect, wat suggereert dat zorgvuldig gedoseerde combinaties van deze middelen met radiotherapie een veelbelovender pad kunnen bieden dan het verder najagen van xevinapant, althans voor dit kankertype. Het vertalen van deze bevindingen naar de kliniek zal niet eenvoudig zijn, omdat dergelijke middelen ook stress kunnen veroorzaken in normale, sneldelende weefsels en in vroege klinische proeven al dosisverlagingen nodig maakten. Toch wijzen de resultaten clinici en onderzoekers in de richting van DNA‑herstel‑gerichte strategieën als overtuigendere kandidaten om radiotherapie zowel effectiever als mogelijk veiliger te maken voor patiënten die geen standaardchemotherapie kunnen krijgen.
Bronvermelding: Roehrle, J., Perugachi-Heinsohn, A., Gatzemeier, F. et al. Comparing and combining xevinapant with ATR and PARP inhibition for the radiosensitization of HPV-negative HNSCC cells. Sci Rep 16, 5882 (2026). https://doi.org/10.1038/s41598-026-38550-3
Trefwoorden: hoofd- en halskanker, radiotherapie, DNA-herstelremmers, xevinapant, radiosensitisatie