Clear Sky Science · nl
Nieuwe histologische observatiemethode met verstrooid licht van niet-gekleurde collageensecties
Waarom het bekijken van onzichtbare vezels ertoe doet
Onze huid, pezen en veel organen worden bijeengehouden door collageen, een taai, touwachtig eiwit. Wanneer deze collageenvezels beschadigd raken of herschikt worden, ontstaan littekens en verstijft weefsel — een proces dat bekendstaat als fibrose en ten grondslag ligt aan veel voorkomende aandoeningen, van levercirrose tot hartfalen en huidveroudering. Toch hebben artsen en onderzoekers nog steeds moeite om de fijne details van hoe collageen verandert tijdens ziekte te zien, omdat bestaande beeldvormingstools traag, duur of afhankelijk van ingewikkelde kleuringen zijn. Deze studie introduceert een nieuwe manier om collageen in gewone laboratoriemonsters te bekijken met alleen licht en slimme beeldverwerking, wat gedetailleerde vezelanalyse veel toegankelijker zou kunnen maken.
Een nieuwe manier om te zien met verstrooid licht
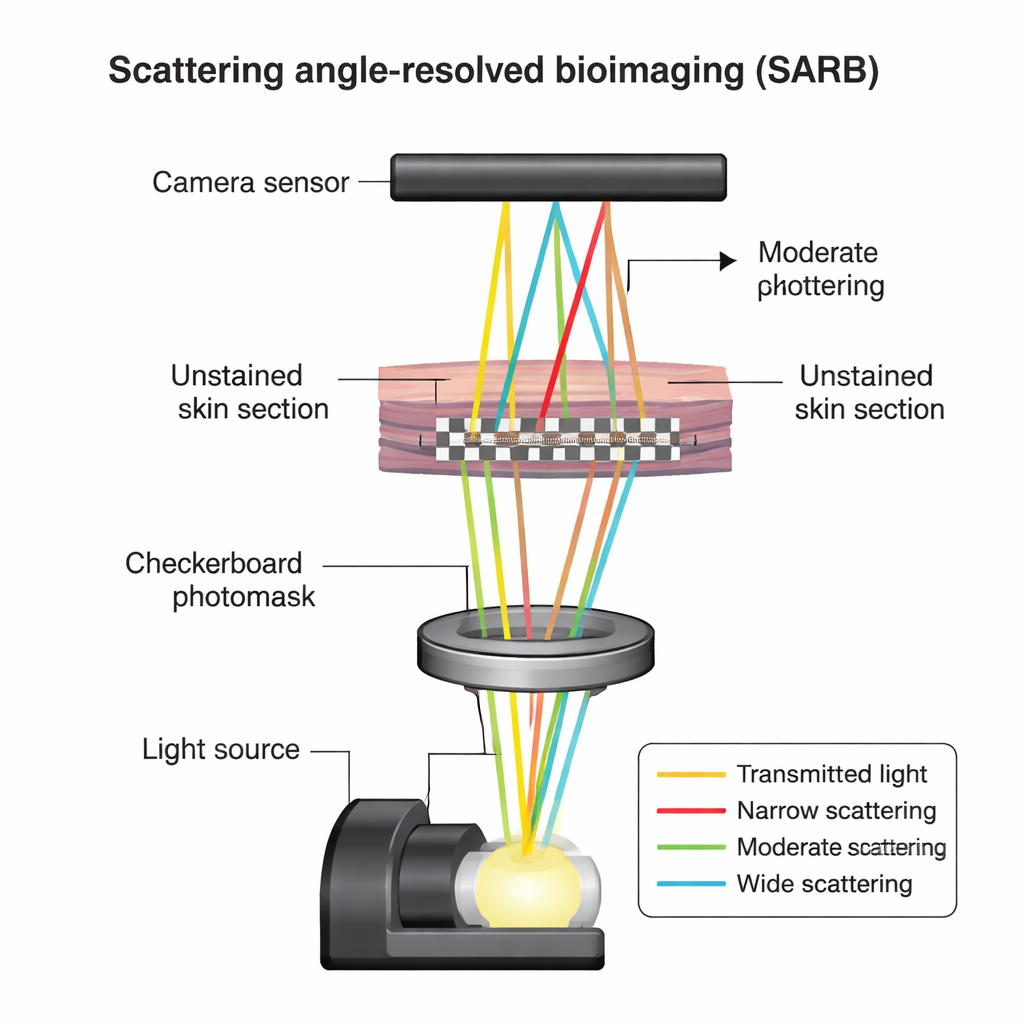
De onderzoekers richtten zich op standaard pathologiestalen: dunne plakjes muizenhuid die gefixeerd en in paraffine ingebed waren, precies zoals weefsels die dagelijks in ziekenhuizen worden onderzocht. In plaats van deze secties chemisch te kleuren, lieten ze ze onaangeroerd en gebruikten een techniek genaamd scattering angle-resolved bioimaging, of SARB. Simpel gezegd: wanneer licht door weefsel gaat, gaat een deel van het licht recht door, terwijl een ander deel in verschillende richtingen wordt verstrooid afhankelijk van de kleine structuren die het tegenkomt. SARB schijnt een fijn geordend dambordpatroon van licht door het weefsel in een gewone microscoop en, door dit patroon te verschuiven en te analyseren hoe het beeld verandert, haalt het wiskundig licht uit elkaar dat onder verschillende hoeken is verstrooid. Dit verandert een gewone microscoop in een instrument dat subtiele structurele verschillen kan "lezen" zonder kleurstoffen.
Gewone secties omzetten in rijke structurele kaarten
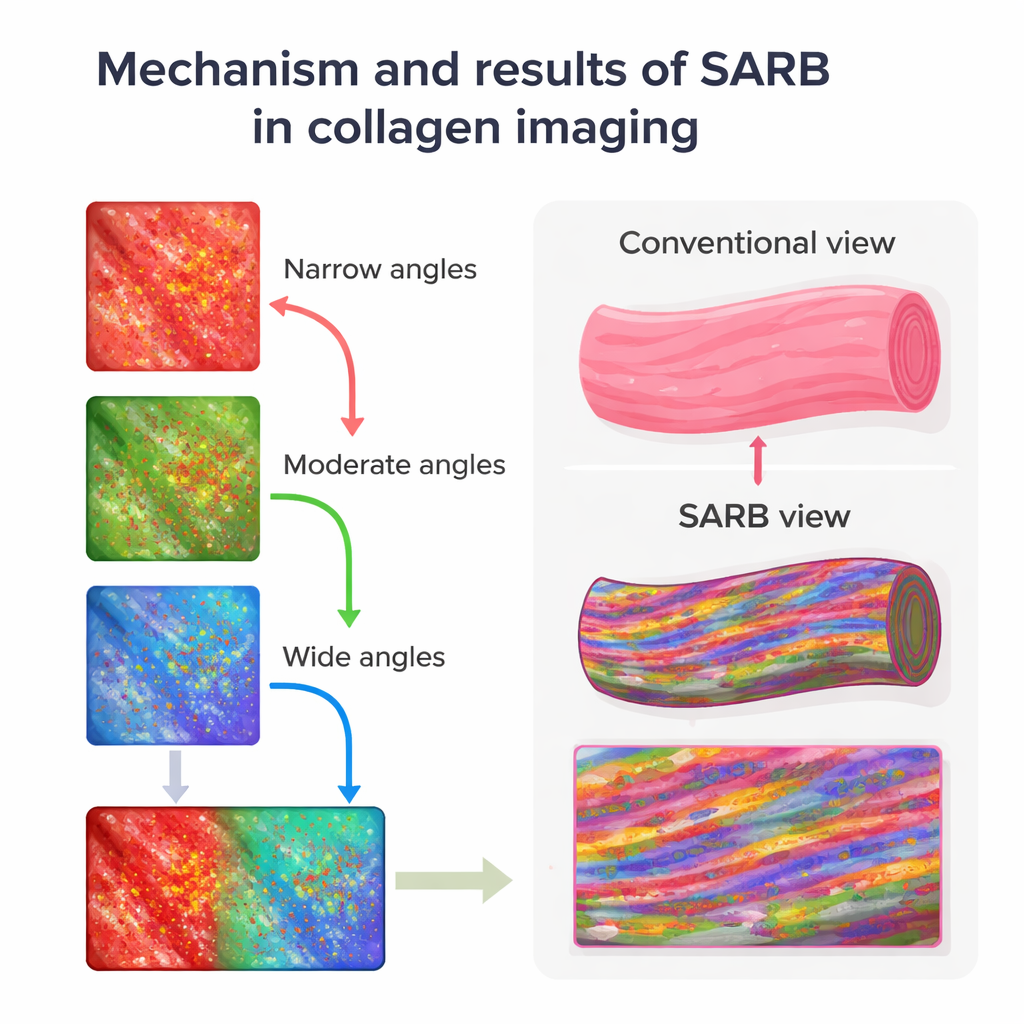
Door SARB toe te passen op 4 micrometer dikke plakjes muizenhuid kon het team duidelijk de belangrijkste huidlagen en haarzakjes zien, maar het echte voordeel zat in de collageenbundels in de dermis. Door beelden op te splitsen in componenten die worden gedomineerd door smal, matig en wijd verstrooid licht, en deze vervolgens toe te wijzen aan de rode, groene en blauwe kleurkanalen, creëerden ze samengestelde weergaven waarbij verschillen in verstrooiing als duidelijke kleuren naar voren kwamen. Collageenbundels die er bij standaard hematoxyline-eosine (H&E)-kleuring uniform bleekroze uitzagen, toonden in SARB-beelden interne strepen en vlekjes, wat duidde op fijnere substructuren die conventionele lichtmicroscopie normaal verbergt.
Vergelijking met elektronenmicroscopie
Om te testen of deze kleurrijke verstrooiingspatronen daadwerkelijk de echte vezelarchitectuur weerspiegelden, werden dezelfde weefselsecties later onderzocht met scanning- en transmissie-elektronenmicroscopie, die individuele collageenfibrillen kunnen resolven. SARB had twee belangrijke interne patronen binnen collageenbundels onthuld: lineaire strepen en puntachtige vlekken. Elektronenmicroscopie toonde aan dat de gestreepte SARB-regio’s overeenkwamen met collageenfibrillen die in de lengterichting zichtbaar waren, terwijl de gevlekte regio’s overeenkwamen met fibrillen in dwarsdoorsnede. Met andere woorden: hoewel SARB geen individuele fibrillen kan zien, kan het wel hun algemene oriëntatie en organisatie binnen een bundel rapporteren. Dit legt een cruciale verbinding tussen het verstrooiingssignaal en de werkelijke microstructuur en valideert SARB als meer dan een esthetische kleurmethode.
Zien hoe collageen veroudert en losser wordt
Het team vroeg zich vervolgens af of SARB bekende veranderingen in collageen door veroudering kon detecteren. Vergelijking van huid van jonge en oude muizen toonde dat conventionele Picrosirius-roodkleuring onder gepolariseerd licht vooral een verschuiving in collagentypes liet zien — van het ene type naar het andere — maar beperkte inzichten bood in hoe vezels waren gerangschikt. SARB daarentegen toonde dat verouderde huid grotere ruimtes tussen collageenbundels had en minder interne verstrooiingssignalen, wat wijst op lossere of meer gedesorganiseerde fibrillen. Elektronenmicroscopie ondersteunde deze indruk en liet onregelmatiger vezels zien bij oudere dieren. Door SARB-beelden om te zetten in zwart-witkaarten en het aandeel sterk verstrooiende gebieden te meten, vonden de onderzoekers dat oudere muizen een significant lagere verhouding van "hoog-verstrooiend gebied" hadden, wat een eenvoudige metriek opleverde die structureel verval volgde.
Van laboratoriumcuriositeit tot praktisch instrument
Aangezien SARB is gebouwd op een gewone transmissielichtmicroscoop met een toegevoegde gepatternte filter en camera, zou het in principe in veel laboratoria kunnen worden ingezet die al met paraffine-ingebedde weefsels werken. Het vermijdt tijdrovende kleuringen, vermindert variabiliteit tussen laboratoria en levert zowel visuele als kwantitatieve uitkomsten van collageenorganisatie. Hoewel meer werk nodig is om specifieke verstrooiingssignaturen te relateren aan exacte vezeldikte, dichtheid en 3D-arrangement, toont deze studie dat verstrooid licht van niet-gekleurde secties kan dienen als een gevoelige, labelvrije marker voor de staat van collageen. In de toekomst zou SARB kunnen helpen bij het screenen van antifibrotische of anti-verouderingsbehandelingen, het monitoren van wondgenezing en mogelijk het signaleren van vroege weefselveranderingen bij kankers — allemaal door nieuwe structurele informatie te halen uit de glaasjes die pathologen al gebruiken.
Bronvermelding: Otaki, M., Shimano, M., Asano, Y. et al. Novel histological observation method using the scattered light of unstained collagen sections. Sci Rep 16, 7574 (2026). https://doi.org/10.1038/s41598-026-38504-9
Trefwoorden: collageenbeeldvorming, fibrose, huidveroudering, lichtverstrooiing, microscopie