Clear Sky Science · nl
Gerichte remming van HDAC8 met niet-hydroxamaat [1,2,4]triazolo[4,3-a] quinoline verbindingen
Nieuwe hoop voor een kinderoncologische aandoening
Neuroblastoom is een agressieve kinderlijkende kanker die ontstaat uit zenuwcellen en vaak moeilijk te behandelen is zodra deze is uitgezaaid. Deze studie onderzoekt een nieuwe manier om neuroblastoomcellen te vertragen of te doden door een belangrijke cellulaire schakelaar, HDAC8, uit te schakelen. Door een nieuwe familie van geneesmiddelachtige moleculen te ontwerpen die zeer selectief op deze schakelaar werken, streven de onderzoekers ernaar behandelingen te ontwikkelen die zowel effectiever tegen tumoren zijn als milder voor de rest van het lichaam.
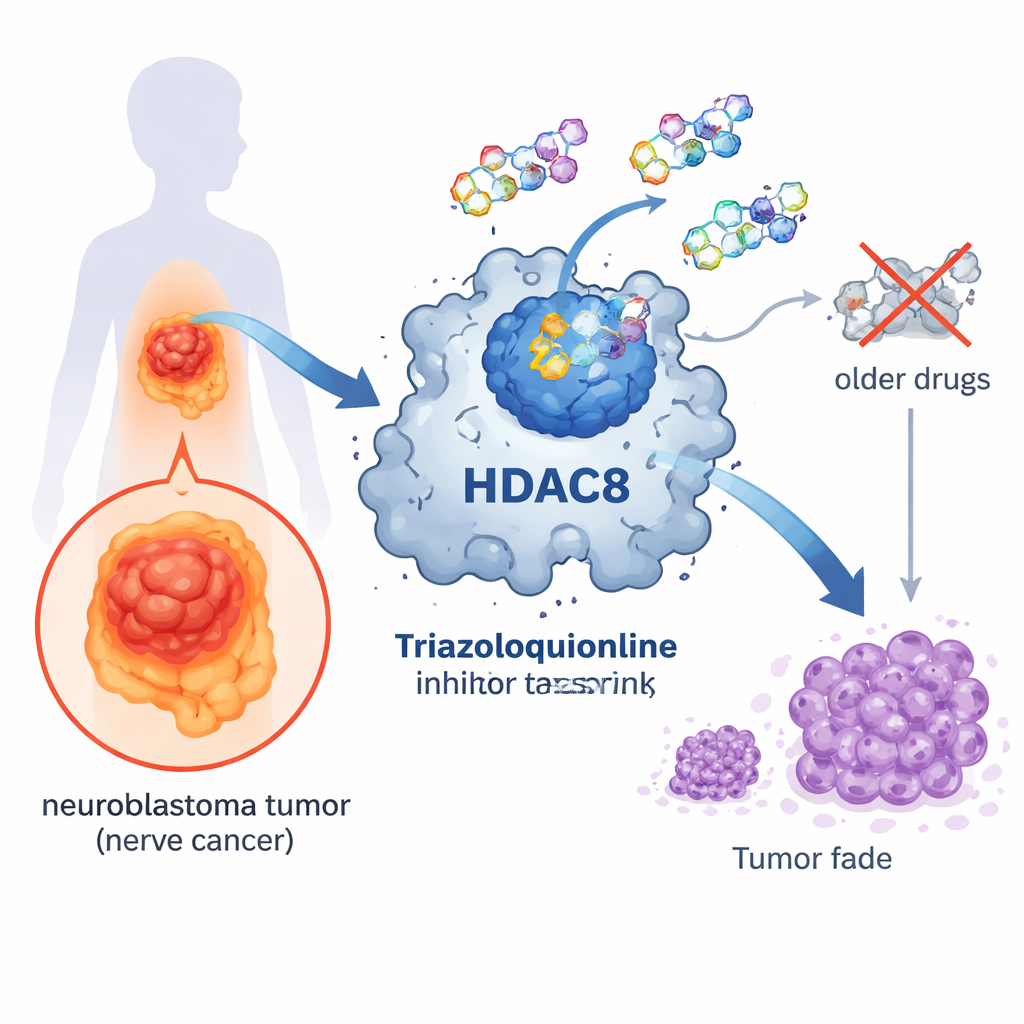
Een moleculaire schakel in het hart van kanker
Binnen onze cellen worden genen voortdurend aan- en uitgezet. Een belangrijk regelsysteem berust op kleine chemische labels, acetylgroepen, die zich hechten aan eiwitten die met DNA geassocieerd zijn. Enzymen die histon deacetylasen (HDACs) worden genoemd verwijderen deze labels, waardoor de verpakking van DNA strakker wordt en de genactiviteit doorgaans afneemt. HDAC8 is een lid van deze enzymfamilie en is in verband gebracht met verschillende vormen van kanker, waaronder neuroblastoom. Wanneer HDAC8 overactief is, kunnen kankercellen gemakkelijker groeien, overleven en uitzaaien, waardoor het een aantrekkelijk doelwit is voor nieuwe geneesmiddelen.
Beperkingen van oudere HDAC-geneesmiddelen
Verschillende HDAC-remmende geneesmiddelen zijn al goedgekeurd voor sommige bloedkankers, maar ze hebben de neiging meerdere HDAC-typen tegelijk te remmen. De meeste van deze medicijnen gebruiken een hydroxamaat-chemische groep om een metaalion in het actieve centrum van het enzym vast te grijpen. Hoewel effectief, bindt deze groep metalen zo sterk dat dit tot bijwerkingen kan leiden en de precisie waarmee het middel onderscheid maakt tussen verschillende HDACs beperkt. Daardoor kunnen patiënten toxiciteit ervaren en worden gezonde cellen samen met kankercellen beschadigd. Onderzoekers zoeken daarom naar alternatieve chemische ontwerpen die de kankervoordelen behouden en tegelijkertijd onbedoelde schade verminderen.
Ontwerpen van een nieuwe klasse gerichte remmers
In dit werk ontwierp en synthetiseerde het team 21 nieuwe verbindingen gebouwd rond een triazoloquinoline-scaffold, verbonden via een flexibele linker met een "+alpha-amino amide"-gebied dat het zinkatoom in het actieve centrum van HDAC8 kan binden. Met computerondersteund ontwerp kozen ze deze architectuur om in een smalle "acetaatafvoerkanaal" te passen die uniek is voor HDAC8, een structureel kenmerk dat helpt hoge specificiteit te bereiken. Gedetailleerde dockingstudies en moleculaire dynamicasimulaties toonden aan dat verschillende van de nieuwe moleculen — met name die aangeduid als 9m en 9r — stabiele, langdurige interacties vormen in het HDAC8-pocket en even sterk of sterker binden dan een bekende referentie-remmer. Belangrijk is dat biochemische tests bevestigden dat de beste verbindingen HDAC8 sterk blokkeren terwijl andere leden van de HDAC-familie grotendeels ongemoeid worden gelaten.
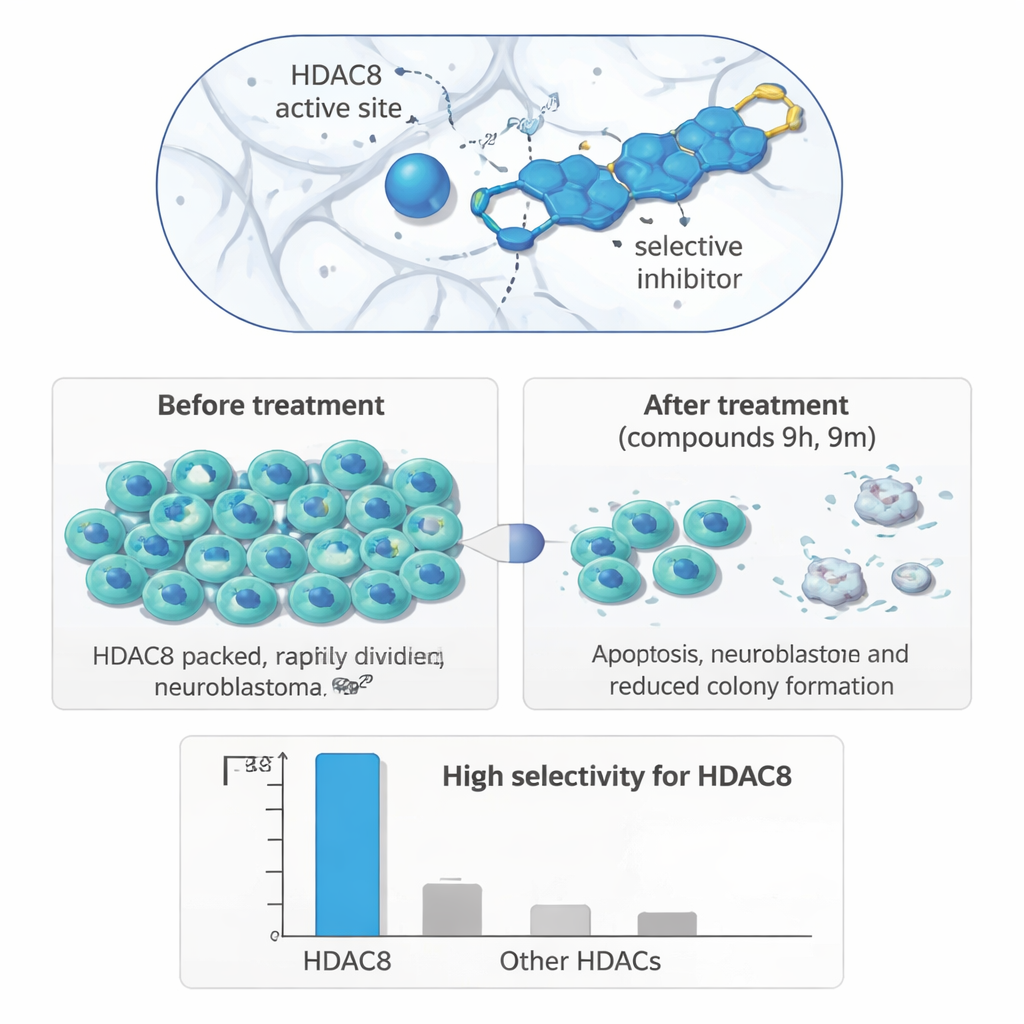
Van reageerbuis naar tumorcellen
Om te onderzoeken of deze precieze enzymtargeting zich vertaalt in bruikbare biologische effecten, testten de onderzoekers hun verbindingen op een paneel van menselijke cellijnen. In neuroblastoomcellen (IMR-32) staken twee moleculen, 9h en 9m, duidelijk boven de rest uit: ze verminderden celgroei bij micromolaire concentraties en deden dit sterker in neuroblastoom dan in borstkanker- of darmkankercellen, of in niet-kankercellen uit de nier. Langdurige kolonievormingsexperimenten toonden aan dat behandelde neuroblastoomcellen veel van hun vermogen om na medicijnblootstelling opnieuw te groeien verloren. In een wound-healing-assay, die bijhoudt hoe snel cellen migreren om een kras in een cellaag te sluiten, vertraagden beide verbindingen de beweging van neuroblastoomcellen, wat duidt op een verminderde metastatische potentie.
Onderzoeken hoe de verbindingen kankercellen doden
Flowcytometriestudies toonden aan dat 9h en 9m geprogrammeerde celdood (apoptose) in neuroblastoomcellen opwekken en een ophoping van cellen veroorzaken in een fase van de celcyclus die geassocieerd wordt met DNA-schade of celdood (Sub‑G1). Om te bevestigen dat deze effecten werkelijk voortkomen uit HDAC8-blokkade, mat het team de acetylatiestatus van een eiwit genaamd SMC3, een bekende HDAC8-doelwit die betrokken is bij het bijeenhouden van zusterchromosomen tijdens celdeling. Wanneer HDAC8 wordt geremd, hoopt geacetyleerd SMC3 zich op. Na behandeling met 9h of 9m stegen de niveaus van geacetyleerd SMC3 sterk, terwijl het totale SMC3-eiwit ongewijzigd bleef — overtuigend bewijs dat deze verbindingen HDAC8 rechtstreeks in levende cellen treffen en diens normale functie in chromosoomcontrole verstoren.
Wat dit kan betekenen voor toekomstige behandelingen
Samengevoegd schetsen de chemie, computermodeling, enzymtests en celgebaseerde experimenten een consistent beeld: de nieuw ontwikkelde triazoloquinoline-verbindingen zijn krachtige, zeer selectieve remmers van HDAC8 die de groei en verspreiding van neuroblastoomcellen kunnen beperken terwijl andere HDAC-enzymen gespaard blijven. Omdat ze de conventionele hydroxamaatgroep vermijden, kunnen ze een veiliger pad bieden om HDAC8 als therapeutisch doel te benutten. Hoewel er nog veel werk te doen is — vooral dierstudies en uiteindelijke klinische proeven — legt dit onderzoek een solide basis voor de ontwikkeling van preciezere geneesmiddelen tegen kinderlijkende neuroblastoom en mogelijk andere HDAC8-gedreven aandoeningen.
Bronvermelding: Bandaru, N.V.M.R., Fathima, A., Sengar, S. et al. Targeted HDAC8 inhibition with non-hydroxamate [1,2,4]triazolo[4,3-a] quinoline compounds. Sci Rep 16, 7472 (2026). https://doi.org/10.1038/s41598-026-38490-y
Trefwoorden: HDAC8-remmers, neuroblastoom, epigenetische therapie, triazoloquinoline, gerichte kankergeneesmiddelen