Clear Sky Science · nl
Een interpreteerbaar machine learning‑model dat routinematige klinische gegevens gebruikt voor vroege terugkeer‑voorspelling bij hepatocellulair carcinoom
Waarom dit belangrijk is voor patiënten en families
Voor mensen die een operatie ondergaan om leverkanker te verwijderen, is een van de meest urgente vragen: “Komt de kanker binnenkort terug?” Tegenwoordig kunnen artsen slechts ruwe schattingen geven, vaak gebaseerd op brede stadia‑systemen die veel verschillende patiënten als gelijk behandelen. Deze studie presenteert een nieuwe manier om informatie die ziekenhuizen al verzamelen—routinematige bloedtesten en scanresultaten—te combineren met interpreteerbare kunstmatige intelligentie om elke patiënt een duidelijker, meer gepersonaliseerd beeld te geven van het kortetermijnrisico dat de kanker terugkeert.
Een veelvoorkomende kanker met een hardnekkige terugkeersnelheid
Hepatocellulair carcinoom is het meest voorkomende type primaire leverkanker en een belangrijke oorzaak van kankersterfte wereldwijd. Zelfs wanneer chirurgen zichtbare tumoren volledig verwijderen, ziet meer dan 70% van de patiënten de ziekte binnen vijf jaar terugkeren. Vroege terugkeer—ongeveer binnen twee jaar na de operatie—is bijzonder zorgwekkend, omdat dit meestal wijst op agressieve kankercellen die zich al binnen de lever hebben verspreid en de overleving sterk verslechteren. Bestaande klinische stadia‑systemen, zoals TNM of Barcelona Clinic Liver Cancer (BCLC), kunnen patiënten wel grofweg in categorieën indelen maar slagen er vaak niet in om precies aan te geven wie daadwerkelijk een hoog risico op vroege terugkeer loopt.
Dagelijkse testresultaten omzetten in een risicoscore
De onderzoekers gebruikten gegevens van 1.120 patiënten die tussen 2014 en 2024 ogenschijnlijk curatieve leveroperaties ondergingen in twee grote ziekenhuizen in China. Ze concentreerden zich alleen op informatie die voor de operatie beschikbaar was: leeftijd en geslacht, beeldvormingskenmerken zoals de grootste tumordiameter en of er meerdere tumoren waren, en een breed scala aan standaardlaboratoriumtesten die in de dagen voorafgaand aan de operatie werden uitgevoerd. Hieruit selecteerden ze negen sleutelvoorspellers die verband hielden met de kans op terugkeer. In plaats van zich te baseren op één wiskundige formule, combineerden ze drie verschillende machine learning‑benaderingen en namen het gemiddelde van hun uitkomsten als één risicoscore tussen 0 en 1. Patiënten werden vervolgens ingedeeld in lage, matige en hoge risicocategorieën op basis van deze score. 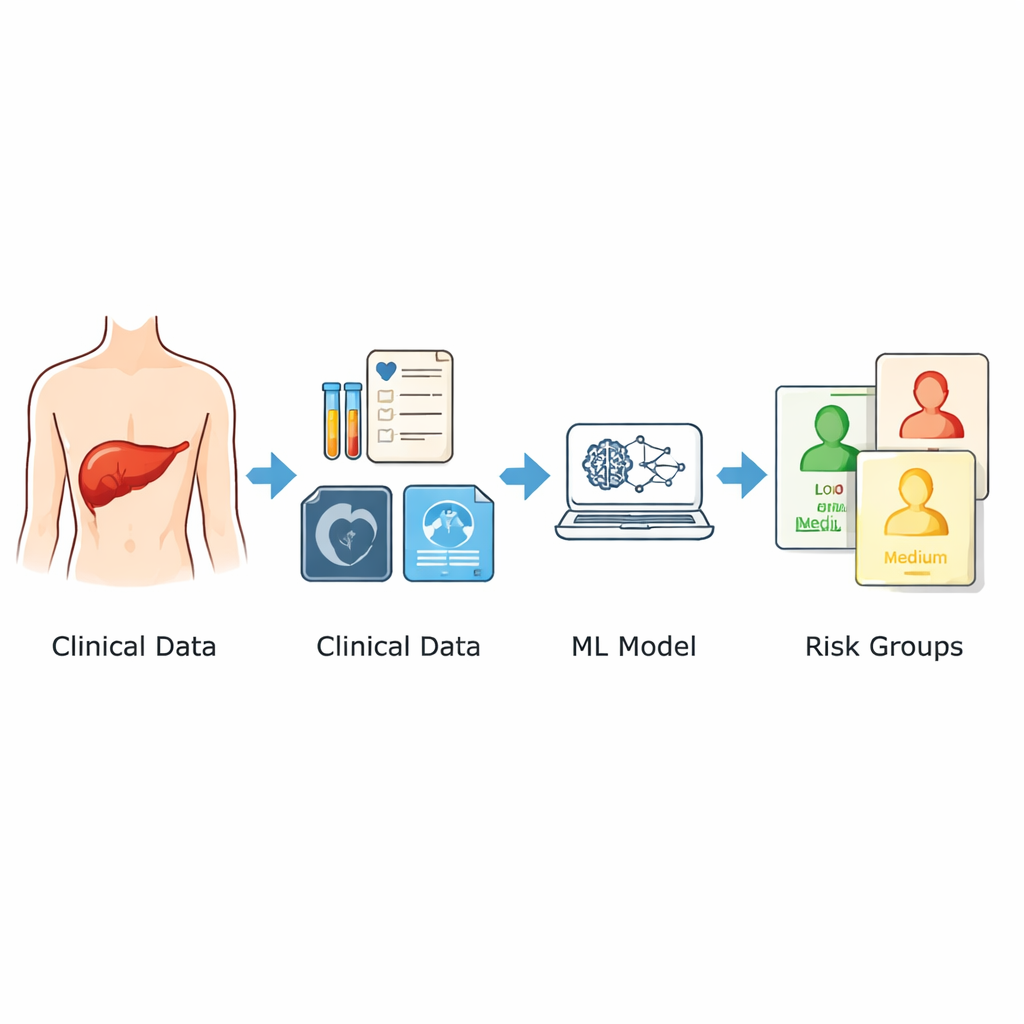
Beter dan standaard stadia‑systemen
Om te testen hoe goed het model werkte, evalueerde het team het eerst in een “hold‑out” groep patiënten uit het oorspronkelijke ziekenhuis en daarna in een onafhankelijke groep uit het tweede ziekenhuis. In beide settings was het nieuwe model duidelijk beter dan traditionele stadia‑systemen in het onderscheiden wie kanker‑vrij zou blijven en wie binnen 24 maanden zou terugkeren. In de interne testgroep was de nauwkeurigheid in de tijd, gemeten met een standaardstatistiek genaamd de area under the curve, ongeveer 0,76, vergeleken met ongeveer 0,55 tot 0,64 voor gebruikelijke stadia‑methoden. Mensen in de hoge‑risicogroep hadden de slechtste terugkeer‑vrije overleving, degenen in de matige‑risicogroep zagen hun kans op terugkeer met ongeveer 60% afnemen, en degenen in de lage‑risicogroep hadden ongeveer 90% minder risico dan de hoge‑risicogroep. Deze sterke verschillen bleven ook in het externe ziekenhuis zichtbaar en waren grotendeels consistent over de meeste subgroepen, zoals jongere en oudere patiënten, mannen en vrouwen, en patiënten met grote of kleine tumoren.
De zwarte doos van kunstmatige intelligentie openen
Een frequente kritiek op machine learning in de geneeskunde is dat het opereert als een zwarte doos: het voorspelt mogelijk goed, maar zelfs specialisten kunnen niet zien waarom. Om dit aan te pakken, pasten de auteurs een methode toe genaamd SHapley Additive exPlanations, of SHAP, die elke voorspelling uitsplitst in bijdragen van individuele invoervariabelen. De analyse toonde aan dat tumorgrootte de sterkste enkele factor was die het hogere risico dreef in alle drie de algoritmen, gevolgd door kenmerken zoals het aantal tumoren en bloedgebaseerde indicatoren van leverfunctie en ontsteking. Interessant genoeg leek het chloridegehalte in het bloed het risico in de tegengestelde richting te beïnvloeden en fungeerde het als een beschermende factor in deze dataset. Voor individuele patiënten kan het model eenvoudige balkachtige grafieken genereren die bijvoorbeeld laten zien hoe een grote tumordiameter en ongunstige bloedwaarden de risicoscore omhoog drijven, terwijl betere leverfunctie die omlaag haalt. 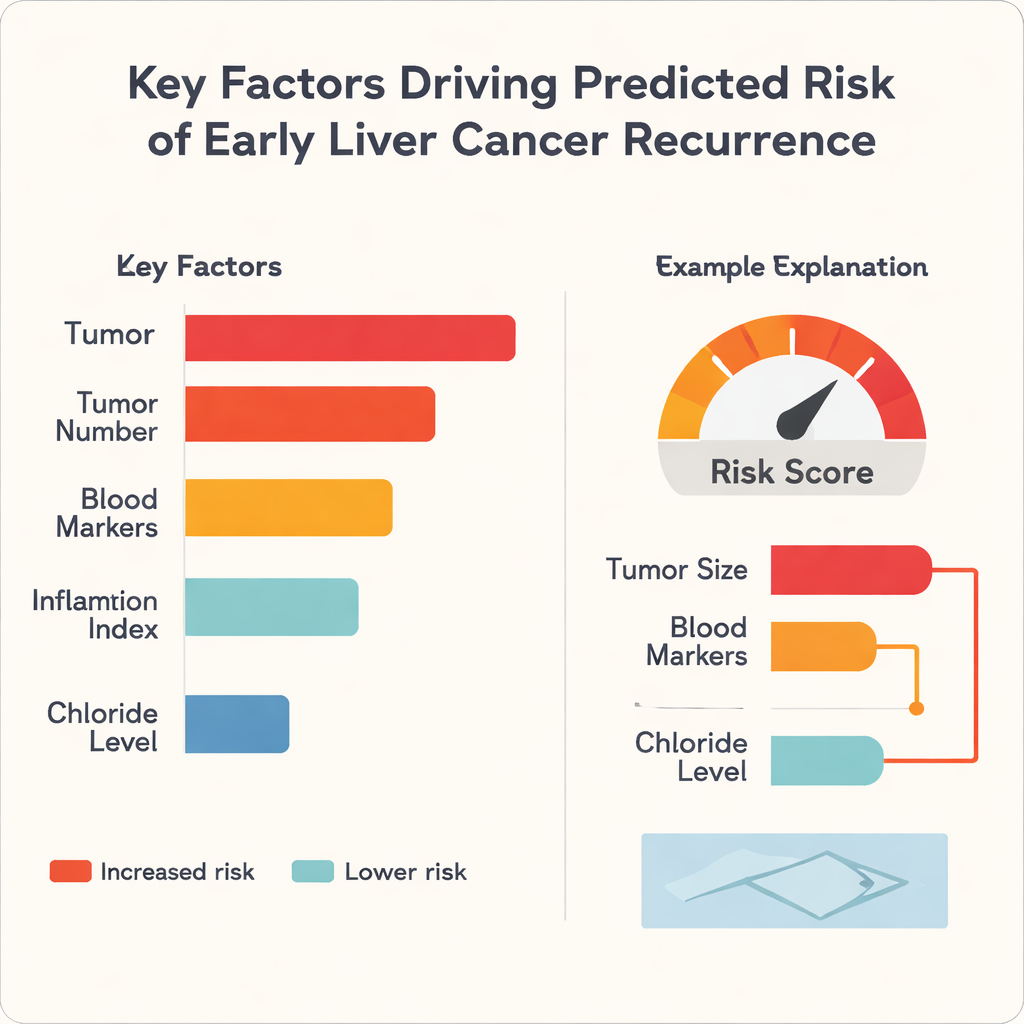
Wat dit in de kliniek zou kunnen betekenen
Aangezien het model werkt met gegevens die ziekenhuizen al verzamelen en geen speciale scans of dure genetische tests vereist, zou het in veel verschillende zorgomgevingen kunnen worden ingezet, ook in settings met beperkte middelen. Voor de operatie zouden artsen het kunnen gebruiken om mensen te identificeren die intensievere opvolgschema’s nodig hebben of mogelijk baat hebben bij aanvullende behandelingen na de operatie, terwijl echte laag‑risicopatiënten worden gespaard van onnodige onderzoeken en onrust. De auteurs wijzen erop dat hun studie retrospectief is en afkomstig uit een specifieke patiëntenpopulatie, dus zijn toekomstige prospectieve proeven in meer diverse omgevingen nog nodig. Niettemin laat hun werk zien hoe transparante, verklaarbare AI vertrouwde laboratoriumwaarden en scanbevindingen kan omzetten in betekenisvolle, geïndividualiseerde voorspellingen die gedeelde besluitvorming tussen patiënten en hun zorgteams kunnen ondersteunen.
Bronvermelding: Guo, DF., Wen, Q., Zhang, X. et al. An interpretable machine learning model using routine clinical data for early recurrence prediction in hepatocellular carcinoma. Sci Rep 16, 7520 (2026). https://doi.org/10.1038/s41598-026-38484-w
Trefwoorden: terugkeer van leverkanker, machine learning‑model, klinische risicovoorspelling, interpreteerbare AI, hepatocellulair carcinoom