Clear Sky Science · nl
GluN2A-gemedieerde stromen en calciumsignaal in door menselijke iPSC afgeleide neuronen
Waarom kleine in het lab gekweekte hersencellen ertoe doen
Wetenschappers wenden zich steeds vaker tot in het laboratorium gekweekte menselijke hersencellen om te bestuderen hoe onze hersenen zich ontwikkelen en om te onderzoeken wat er misgaat bij aandoeningen zoals autisme, epilepsie en de ziekte van Alzheimer. Deze studie stelt een eenvoudige maar cruciale vraag: groeien deze in het lab gemaakte neuronen op en verbinden ze zich op manieren die echt lijken op de menselijke hersenen, vooral in hoe ze omgaan met een belangrijke chemische boodschapper genaamd glutamaat? Het antwoord laat zien hoe men realistischere “mini-hersen” modellen kan opbouwen en wijst op nieuwe manieren om hersengezondheid en -ziekten te onderzoeken.
Neuronen bouwen uit gereprogrammeerde cellen
De onderzoekers begonnen met menselijke geïnduceerde pluripotente stamcellen—gewone cellen die zijn “gereprogrammeerd” naar een stamceltoestand. Vanuit daar stuurden ze de cellen richting neurale voorlopercellen en uiteindelijk naar netwerken van neuronen en ondersteunende astrocyten, waarmee ze de zich ontwikkelende menselijke cortex nabootsten. Ze vergeleken twee veelgebruikte kweekrecepten, ofwel cultuurcondities. Eén, BrainPhys-medium genoemd, is ontworpen om actieve, elektrisch reagerende neuronen te bevorderen en levert doorgaans meer astrocyten op. De andere, een meer traditioneel onderhoudsmedium voor neuronen, geeft de voorkeur aan neuronen met minder astrocyten. Gedurende zestig dagen volgde het team hoe deze culturen veranderden in uiterlijk, genexpressie en celtypen, en ontdekte dat in BrainPhys gekweekte culturen complexere neuronale vormen en een neuron-naar-astrocyt verhouding ontwikkelden die dichter bij die van het echte menselijke brein lag.
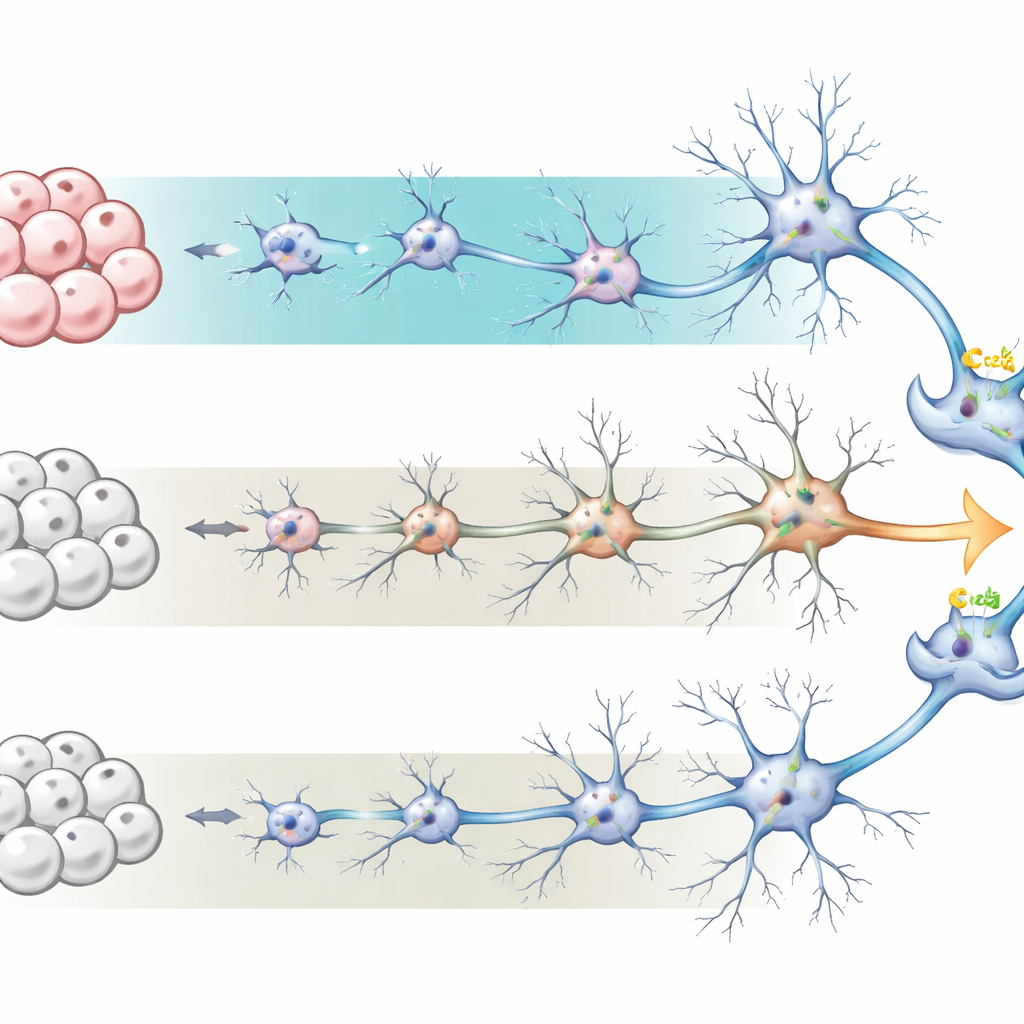
Signaleren dat de cellen volwassen worden
Om te zien hoe “rijp” de neuronen waren, mat het team de globale genexpressie met RNA-sequencing op dag 60. Cellen gekweekt in BrainPhys toonden bijna tweeduizend genen met afwijkende expressieniveaus vergeleken met het standaardmedium, waarvan veel gekoppeld aan neuronale differentiatie, synapsvorming en elektrische activiteit. Genen geassocieerd met astrocytfunctie en ontsteking waren ook hoger, wat de grotere astrocytenpopulatie weerspiegelt. Gezamenlijk suggereren deze patronen dat de BrainPhys-culturen beter latere stadia van hersenontwikkeling nabootsen, met fijnere communicatiepunten tussen neuronen en een ondersteunende omgeving die meer lijkt op levend weefsel.
Belangrijke schakelaars in chemische communicatie
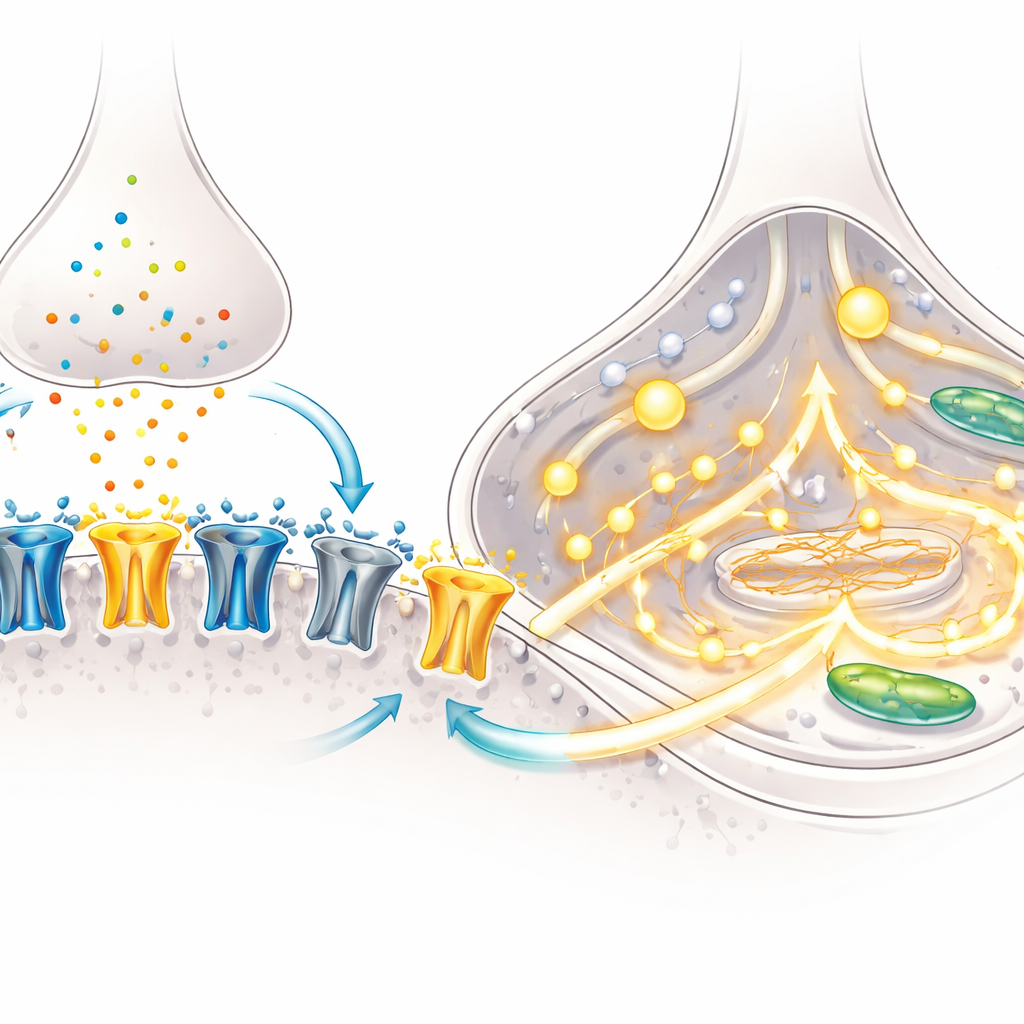
Een kenmerk van hersenrijping is een verschuiving in de samenstelling van NMDA-receptoren—moleculaire poorten op neuronen die opengaan als reactie op glutamaat en helpen bij het vormen van leergerelateerde verbindingen. Vroeg in de ontwikkeling domineert een subunit genaamd GluN2B; later neemt GluN2A het over, wat bepaalt hoe lang en hoe sterk de receptoren open blijven. Met behulp van microscopie toonde het team aan dat er in de loop van de tijd meer NMDA-receptoren naar synapsen verhuisden, de contactpunten tussen neuronen, vooral in BrainPhys-culturen. Gerichte genmetingen toonden een daling van de “vroege” GluN2B-subunit en een stijging van de “latere” GluN2A-subunit, wat aangeeft dat de neuronen deze klassieke ontwikkelingsschakel ondergingen.
Stromen en calcium binnen de cellen volgen
Functionele tests bevestigden dat deze moleculaire veranderingen er toe deden. Met fijngepunte elektroden registreerden de onderzoekers elektrische stromen die werden opgewekt door NMDA, een stof die selectief NMDA-receptoren activeert. Neuronen uit beide kweekmethoden toonden robuuste stromen, maar het blokkeren van de GluN2A-subunit verminderde deze stromen ongeveer met de helft, wat aantoont dat GluN2A nu een belangrijke rol speelt in het signaaltransport. Het team volgde daarna calcium, een belangrijke interne boodschapper, met behulp van een fluorescerende kleurstof. Bij blootstelling aan NMDA vertoonde een veel groter aandeel van de in BrainPhys gekweekte neuronen sterke calciumpieken, en de omvang van het signaal was groter. Genanalyse suggereerde waarom: BrainPhys-culturen upreguleerden meerdere componenten van calciumkanalen en vrijmakingsroutes, waardoor de cellen beter in staat waren NMDA-receptoractivatie om te zetten in brede, gecoördineerde calciumsignalen.
Wat dit betekent voor het bestuderen van hersenaandoeningen
Samen laten deze bevindingen zien dat uit menselijke stamcellen afgeleide neuronen binnen slechts twee maanden een functioneel rijpe staat kunnen bereiken, vooral wanneer ze worden gekweekt onder condities die actieve netwerken en een realistische mix van neuronen en astrocyten bevorderen. In deze staat domineert de “volwassen-achtige” GluN2A-subunit NMDA-receptorstromen en levert ze een sterke bijdrage aan calcium‑signaaltransductie, vergelijkbaar met wat wordt gezien in het ontwikkelende menselijke brein. Voor niet‑specialisten is de conclusie dat onderzoekers nu een trouwere laboratoriummodel hebben van hoe menselijke exciterende neuronen volwassen worden, zich onderling verbinden en reageren op glutamaat. Dit maakt het mogelijk te onderzoeken hoe subtiele genetische veranderingen of ziekteprocessen deze fijn afgestelde schakelaars verstoren, en opent een venster naar aandoeningen variërend van epilepsie tot de ziekte van Alzheimer en helpt bij het ontwerpen en testen van toekomstige therapieën.
Bronvermelding: Escamilla, S., Avilés-Granados, C., Peralta, F.A. et al. GluN2A-mediated currents and calcium signal in human iPSC-derived neurons. Sci Rep 16, 9736 (2026). https://doi.org/10.1038/s41598-026-38482-y
Trefwoorden: NMDA-receptoren, stamcelneuronen, hersenontwikkeling, calciumsignaal, synaptische rijping