Clear Sky Science · nl
De dubbele G9a-remmer en histamine H3-receptorantagonist A-366 verbetert repetitief en sociaal gedrag en vermindert neuro-inflammatie bij BTBR T + tf/J-muizen
Waarom deze muizenstudie ertoe doet voor autisme
Gezinnen die leven met een autismespectrumstoornis (ASS) hebben vaak te maken met een lappendeken aan behandelingen die telkens maar een paar symptomen verlichten. Deze studie onderzoekt een nieuw experimenteel samengesteld middel, A-366 genaamd, dat is ontwikkeld om tegelijkertijd op twee zeer verschillende biologische systemen in te werken. In een veelgebruikt muismodel voor autismachtig gedrag verlaagde A-366 repetitieve handelingen, verbeterde het sociale interactie en dempte het ontstekingsreacties in de hersenen, wat wijst op een toekomst waarin één medicijn mogelijk meerdere kernkenmerken van ASS tegelijk aanpakt.
Een aandoening met veel bewegende onderdelen
ASS is geen enkele ziekte met één enkele oorzaak. Het omvat moeilijkheden met sociale communicatie, repetitief gedrag en vaak andere uitdagingen zoals angst of aandachtsproblemen. Achter deze uiterlijke tekenen schuilt een kluwen van veranderingen in hersenchemie en genregulatie. Huidige medicijnen, zoals het antipsychoticum aripiprazol, richten zich voornamelijk op boodschappersystemen in de hersenen zoals dopamine en serotonine, en zijn alleen goedgekeurd voor bijbehorende symptomen zoals prikkelbaarheid. Tegelijkertijd heeft onderzoek aangetoond dat de manier waarop DNA in hersencellen wordt verpakt en chemisch gemarkeerd — epigenetica — ook verandert bij ASS, net als de activiteit van het eigen immuunsysteem en ontstekingsreacties in de hersenen. Deze verschillende lagen suggereren dat een aanpak die telkens maar één doelwit aanpakt te krap kan zijn.
Beide gen-schakelaars en hersenboodschappers raken
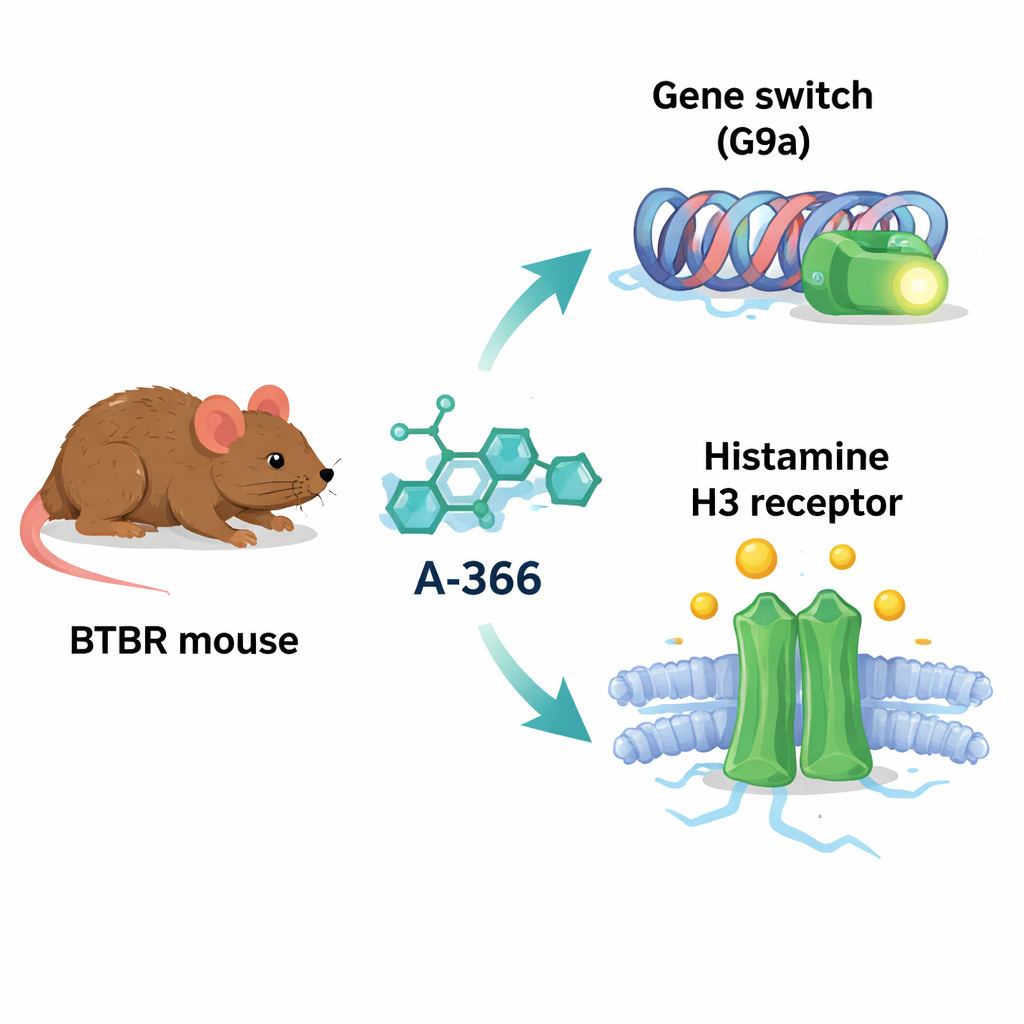
A-366 werd oorspronkelijk ontwikkeld om een eiwit genaamd G9a te blokkeren, een enzym dat chemische labels aan histon-eiwitten toevoegt en genen doorgaans minder actief maakt. Bij meerdere hersenaandoeningen is de activiteit van G9a en de bijbehorende markeringen verhoogd, wat mogelijk genen kan stilleggen die belangrijk zijn voor leren, geheugen en gezonde hersenbekabeling. Intrigerend genoeg lijkt de chemische structuur van A-366 ook op die van middelen die de histamine H3-receptor blokkeren, een schakelaar die de afgifte van histamine en andere neurotransmitters reguleert en die in verband is gebracht met aandacht, waakzaamheid en sociaal gedrag. Vanwege deze overlap vermoedden de auteurs dat A-366 als een “dubbelwerkend middel” zou kunnen fungeren: het verlichten van schadelijke genstillegging via G9a-remming en tegelijkertijd het bevorderen van histaminesignaal door H3-receptoren te blokkeren.
A-366 op de proef gesteld bij autismelikende muizen
Het team werkte met BTBR T+tf/J-muizen, een stam die van nature lage sociabiliteit, sterk repetitief poets- en graafgedrag en verhoogde hersenontsteking vertoont — kenmerken die sleutelaspecten van ASS weerspiegelen. Mannelijke BTBR-muizen kregen drie weken lang dagelijkse injecties met A-366 in drie verschillende doseringen, en hun gedrag werd vergeleken met typische C57-muizen en met BTBR-muizen behandeld met ofwel pitolisant (een standaard H3-receptorblokker) of aripiprazol. In meerdere taken verminderde A-366 dosisafhankelijk repetitief graven, versnipperen en zelfpoetsen en verbeterde het de prestaties in een Y-doolhoftest voor ruimtelijk werkgeheugen. In een sociaal test met drie kamers herstelde A-366 niet alleen de voorkeur van de muizen om tijd met een andere muis door te brengen boven een lege kooi, maar bracht het bij de hoogste dosis de sociale scores op het niveau van typische muizen en overtrof het de effecten van pitolisant en aripiprazol.
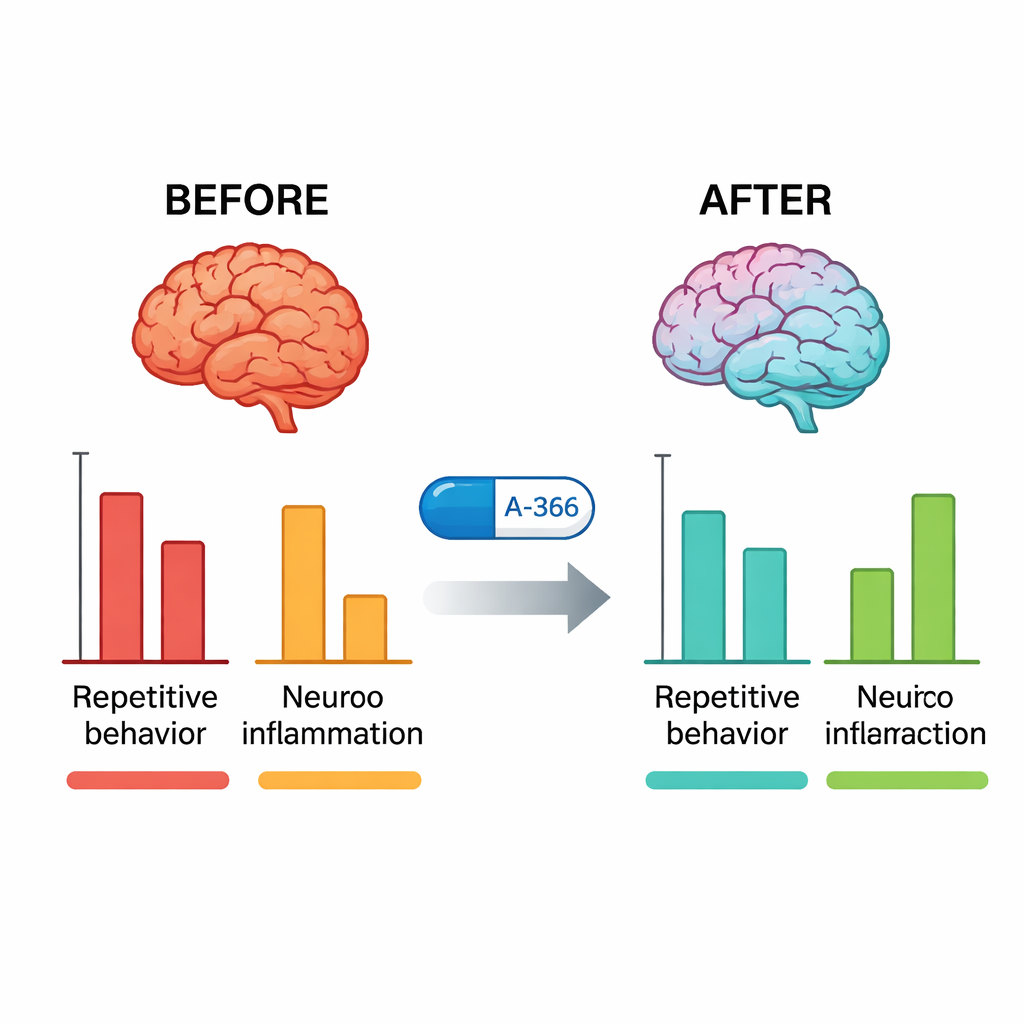
Ontstekingen dempen en de doelwitten bevestigen
Na de gedragsproeven onderzochten de onderzoekers de hersenen van de muizen. Bij onbehandelde BTBR-muizen was de activiteit van G9a in de hippocampus en het cerebellum opvallend hoger dan bij typische muizen. Behandeling met A-366 verminderde deze activiteit sterk terug richting normaal, terwijl pitolisant op zichzelf dat niet deed, wat bevestigt dat A-366 daadwerkelijk zijn epigenetische doelwit raakt. Tegelijkertijd waren sleutelontstekingsmoleculen — TNF-α, IL-6 en IL-1β — sterk verhoogd in BTBR-muizen en werden zij significant verlaagd door A-366, meer dan door aripiprazol. Toen de wetenschappers bovenop A-366 een middel toevoegden dat H3-receptoren activeert (RAMH), werd het gedrags- en anti-inflammatoire voordeel slechts gedeeltelijk teruggedraaid, en bleef de daling in G9a-activiteit bestaan. Dit patroon ondersteunt een gecombineerd mechanisme: duurzame epigenetische verlichting door G9a-remming plus een histaminegemedieerde bijdrage via H3-receptorblokkade.
Wat dit zou kunnen betekenen voor toekomstige behandelingen
Voor niet-specialisten suggereren deze bevindingen dat het mogelijk is medicijnen te ontwerpen die zowel aan de “software” als aan het “berichtenstelsel” van de hersenen tegelijk werken. In dit muismodel van autismachtig gedrag verlichtte A-366 repetitieve handelingen, verbeterde het sociale betrokkenheid en verminderde het tekenen van chronische hersenontsteking door tegelijkertijd schadelijke genuitschakelingen te versoepelen en histaminesignalering aan te passen. A-366 zelf werd ontwikkeld voor andere ziekten en zou optimalisatie en uitgebreide veiligheidstests nodig hebben voordat het bij mensen zou kunnen worden gebruikt. Toch biedt het een blauwdruk voor een nieuwe klasse van middelen met meerdere doelwitten gericht op de complexe biologie van ASS, waarbij het aanpakken van slechts één pad tegelijk tot nu toe beperkte verlichting heeft geboden.
Bronvermelding: Hajar, M., Jayaprakash, P., Stark, H. et al. The dual G9a inhibitor and histamine H3 receptor antagonist A-366 improves repetitive and social behaviors and attenuates neuroinflammation in BTBR T + tf/J mice. Sci Rep 16, 7105 (2026). https://doi.org/10.1038/s41598-026-38481-z
Trefwoorden: autismespectrumstoornis, epigenetische therapie, histamine H3-receptor, neuro-inflammatie, muismodel