Clear Sky Science · nl
aFGF herstelt door hoge glucose veroorzaakte verouderde fibroblasten en verbetert wondgenezing bij diabetes door regulatie van de SIRT1/STAT3-route
Waarom langzaam helende wonden belangrijk zijn
Voor veel mensen met diabetes kan een kleine snijwond aan de voet of het been uitgroeien tot een hardnekkige zweer die maanden aanhoudt, soms leidend tot infectie of zelfs amputatie. Deze chronische zweren zijn niet alleen een oppervlakkig probleem: de huidcellen die het beschadigde weefsel moeten herstellen, worden vaak voortijdig oud en functioneren niet goed meer. Deze studie onderzoekt een veelbelovende manier om sommige van die cellen te “verjongen” met een van nature voorkomend reparatiesignaal, met als doel diabetische wonden sneller en vollediger te laten sluiten.
Cellen die te vroeg verouderen
Gezonde huid is afhankelijk van fibroblasten—ondersteunende cellen die in de diepere huidlagen leven—om zich te vermenigvuldigen, naar een wond te migreren en een nieuw raamwerk voor weefselopbouw neer te leggen. Bij diabetes duwt langdurig hoge bloedsuiker en suurgeschadigde moleculen deze fibroblasten in een toestand die cellulair verouderen of senescentie wordt genoemd. Senescente fibroblasten delen zich niet goed meer, produceren minder van de structurele eiwitten die voor herstel nodig zijn, en scheiden in plaats daarvan een mengsel van ontstekingsbevorderende factoren uit die aanhoudende ontsteking aanwakkeren. De auteurs tonen aan dat bij diabetische ratten de huid rondom een wond meer van deze verouderde fibroblasten bevat en minder van de behulpzame matrixeiwitten, wat samenhangt met veel langzamere genezing.
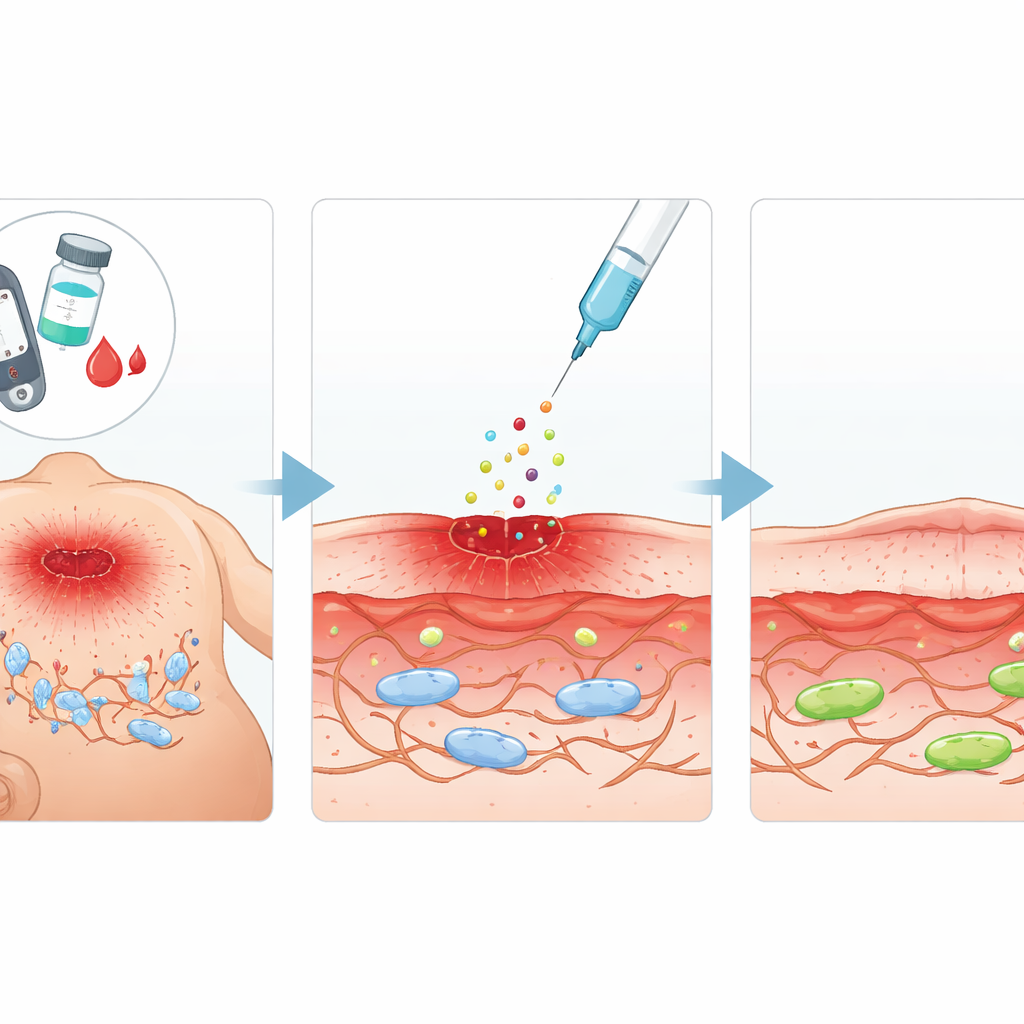
Een veelbelovend reparatiesignaal
Het team concentreerde zich op zuur aFGF (acidic fibroblast growth factor), een van nature voorkomend eiwit dat bekendstaat om het stimuleren van celgroei en weefselherstel. Ze vroegen zich af of aFGF niet alleen de activiteit van fibroblasten kon versterken, maar ook verouderingsachtige veranderingen veroorzaakt door hoge suikerniveaus kon terugdraaien. Bij diabetische ratten maakten ze gestandaardiseerde huidwonden en injecteerden aFGF rond het beschadigde gebied om de paar dagen. Vergeleken met onbehandelde diabetische dieren toonden aFGF-behandelde ratten snellere krimp van het wondoppervlak, betere herbouwing van het onderliggende weefsel en lagere niveaus van merkers die cellulair verouderen aangeven. In parallelle laboratoriumexperimenten met een muizen-fibroblastlijn die werd blootgesteld aan zeer hoge glucoseconcentraties, herstelde aFGF het vermogen van de cellen om te delen en te migreren—twee gedragingen die essentieel zijn voor het sluiten van een wond.
Het kalmeren van oxidatieve stress in de cellen
Hoge bloedsuiker doet meer dan cellen van extra brandstof voorzien: het stimuleert ook de overproductie van reactieve zuurstofsoorten, instabiele moleculen die eiwitten, vetten en DNA beschadigen. Deze oxidatieve stress is een belangrijke trigger voor fibroblasten om senescent te worden. De onderzoekers maten verschillende standaardindicatoren van deze stress in hun celmodel, waaronder schadelijke bijproducten en de activiteit van de eigen antioxidantenzymen van de cel. Onder hoge glucose vertoonden fibroblasten meer schade en zwakkere antioxidatieve verdediging. Toen aFGF werd toegevoegd, verschoof het evenwicht: schadelijke merkers daalden en beschermende enzymen werden actiever. Dit suggereert dat aFGF helpt een gezonder intern milieu te herstellen, waardoor de kans kleiner wordt dat fibroblasten in een permanent verouderde toestand belanden.
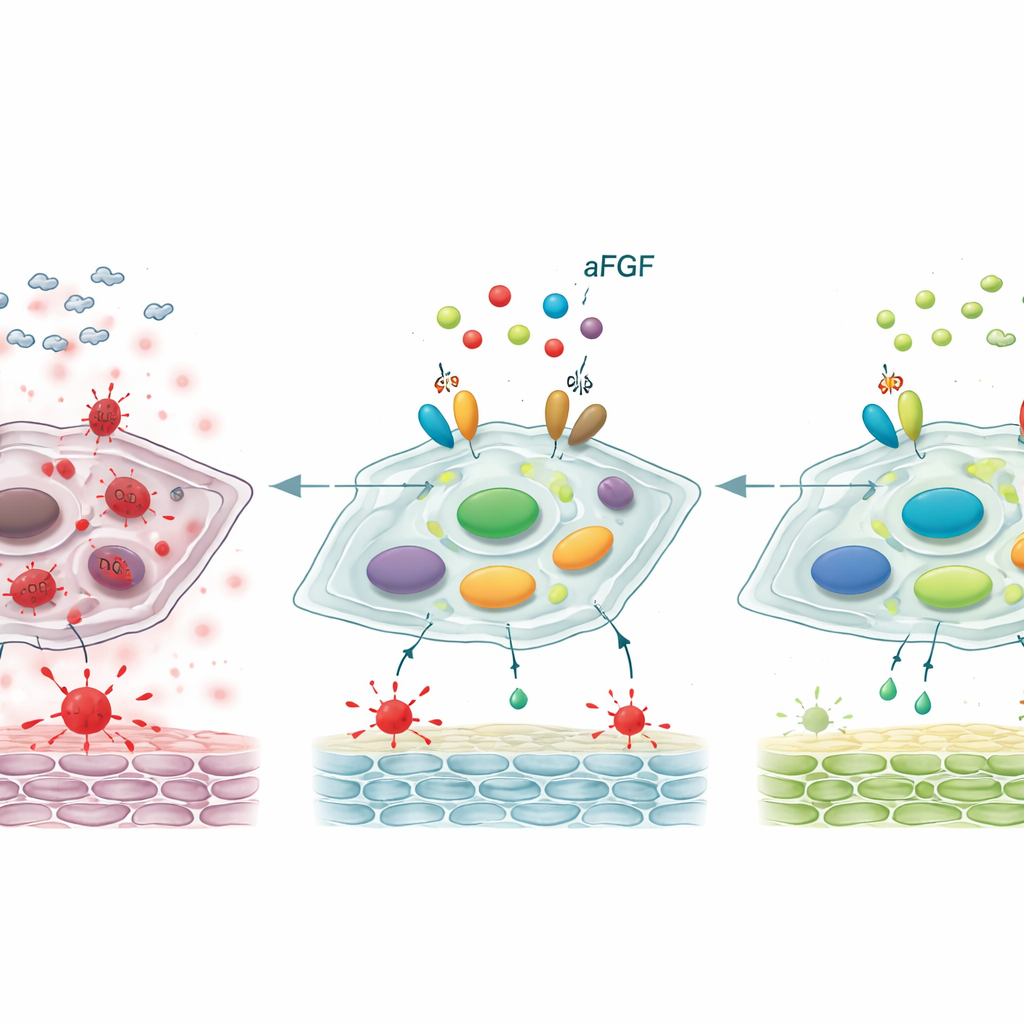
Het resetten van een belangrijke regelschakelaar
Dieper gravend onderzochten de wetenschappers een moleculair controlesysteem met twee eiwitten, SIRT1 en STAT3, die samen beïnvloeden of fibroblasten jong blijven of senescent worden. In diabetische wonden en in cellen behandeld met hoge glucose waren de niveaus van SIRT1, een beschermer geassocieerd met stressbestendigheid, verlaagd, terwijl de geactiveerde vorm van STAT3—een aanjager van veroudering en inflammatoir gedrag—increased was. Behandeling met aFGF keerde dit patroon om: SIRT1 steeg en geactiveerd STAT3 daalde. Toen het team SIRT1 blokkeerde met een specifieke remmer, verloor aFGF grotendeels zijn vermogen om oxidatieve stress te verminderen, verouderingsmerkers te dempen en wondsluiting bij ratten te versnellen. Dit wijst erop dat aFGF’s gunstige effecten sterk afhangen van het heractiveren van SIRT1, dat op zijn beurt STAT3 en het schadelijke verouderingsprogramma dat het aanstuurt, in toom houdt.
Wat dit voor patiënten zou kunnen betekenen
Samengenomen suggereren de bevindingen dat aFGF meer doet dan alleen cellen aanzetten tot groei. Het lijkt overbelaste fibroblasten in diabetische wonden te redden van een destructieve verouderingscyclus, oxidatieve stress te verlichten en een belangrijke moleculaire schakel te resetten zodat deze cellen opnieuw kunnen bijdragen aan weefselherstel. Hoewel het werk uitgevoerd is in ratten en gekweekte cellen, en echte diabetische wonden nog complexer zijn dan de gebruikte modellen, wijzen de resultaten op aFGF als een veelbelovende kandidaat voor toekomstige behandelingen. Als vergelijkbare voordelen bij mensen worden bevestigd, zou zorgvuldig gerichte aFGF-therapie op termijn chronische diabetische ulcera sneller kunnen laten genezen, waardoor pijn, infectierisico en de kans op ernstige complicaties verminderen.
Bronvermelding: Wang, X., Lu, M., Jia, S. et al. aFGF rescues high glucose-induced senescent fibroblasts and improves diabetic wound healing by regulating SIRT1/STAT3 pathway. Sci Rep 16, 7856 (2026). https://doi.org/10.1038/s41598-026-38480-0
Trefwoorden: genezing van diabetische wonden, veroudering van fibroblasten, oxidatieve stress, groeifactortherapie, SIRT1 STAT3-route