Clear Sky Science · nl
In silico-ontdekking van een multi-targetremmer uit natuurlijke verbindingen voor therapie bij de ziekte van Huntington
Een nieuw perspectief op een verwoestende hersenaandoening
De ziekte van Huntington is een zeldzame maar verwoestende hersenaandoening die mensen geleidelijk berooft van beweging, denkvermogen en onafhankelijkheid. De huidige medicijnen kunnen enkele symptomen verlichten, maar ze stoppen of keren de ziekte niet om. Deze studie onderzoekt een nieuwe, door computers aangedreven manier om naar behandelingen te zoeken: men zoekt naar één natuurlijke verbinding die tegelijk meerdere kwetsbare punten in het ziekteproces kan aanpakken — een benadering die effectiever kan zijn dan geneesmiddelen die zich op slechts één doelwit richten.
Waarom Huntington zo moeilijk te behandelen is
De ziekte van Huntington wordt veroorzaakt door een fout gen dat leidt tot de geleidelijke afbraak van zenuwcellen, meestal beginnend op middelbare leeftijd. In het begin kunnen mensen subtiele stemmingsveranderingen, kleine onwillekeurige bewegingen of lichte problemen met planning en concentratie opmerken. Over 10 tot 12 jaar kan dit verslechteren tot ernstige bewegingsstoornissen, verlies van spraak, dementie en volledige afhankelijkheid van verzorgers. Wetenschappers weten dat er veel processen in hersencellen misgaan bij Huntington — de energievoorziening hapert, schadelijke eiwitten klonteren samen en chemische signalen tussen cellen worden toxisch. Omdat zoveel paden tegelijk verstoord zijn, heeft een ‘één eiwit, één geneesmiddel’-strategie moeite gehad echte doorbraken te leveren.
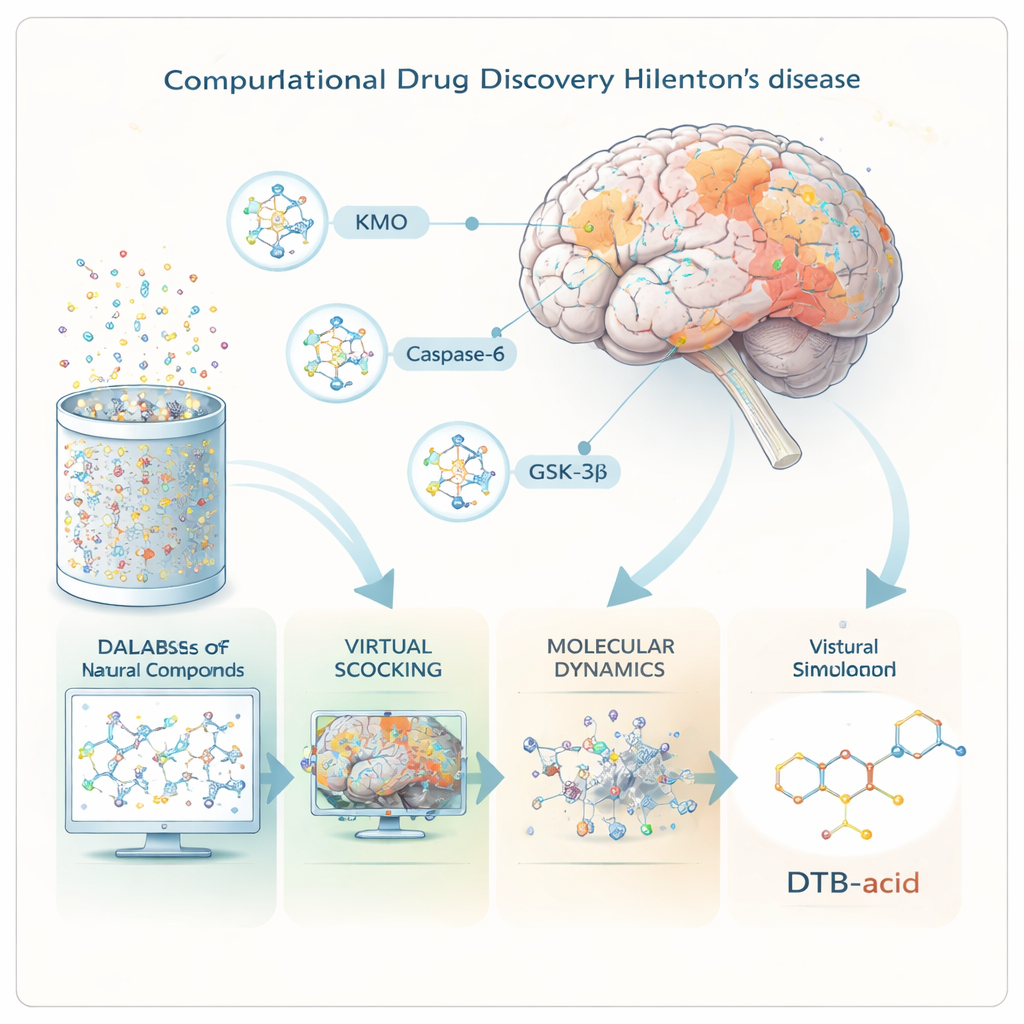
Drie kritieke drukpunten in de hersenen
De onderzoekers richtten zich op drie eiwitten die belangrijke regelpunten vormen bij de ziekte van Huntington. Het eerste, KMO, helpt de afbraak van het aminozuur tryptofaan te sturen naar ofwel toxische of beschermende bijproducten; wanneer dit evenwicht naar toxines kantelt, lijden hersencellen. Het tweede, Caspase‑6, knipt het gemuteerde huntingtine-eiwit in kleinere, zeer toxische fragmenten die vroeg in de ziekte zich ophopen. Het derde, GSK-3β, is een signaalenzym dat gekoppeld is aan abnormale eiwitkluwens en celdood bij verschillende hersenziekten. Door één molecuul te vinden dat de schadelijke activiteit van alle drie tegelijk kan remmen, hoopte het team een therapie te ontwerpen die beter aansluit bij de complexiteit van de ziekte.
De bibliotheek van de natuur screenen met supercomputers
In plaats van chemicaliën in reageerbuizen te mengen, werkten de wetenschappers volledig ‘in silico’ en gebruikten geavanceerde software om te modelleren hoe moleculen zich gedragen. Ze begonnen met meer dan 695.000 natuurlijke verbindingen uit een openbare database en brachten elk in driedimensionale vorm. Krachtige virtuele screeningtools voorspelden vervolgens welke verbindingen waarschijnlijk de bloed‑hersenbarrière zouden passeren, zich als echte geneesmiddelen in het lichaam zouden gedragen en geen grote veiligheidsproblemen zouden veroorzaken. Slechts ongeveer 60.000 slaagden voor deze filters en werden, op de computer, getest op hoe goed ze in de bindingspockets van de drie doelwit‑eiwitten zouden passen.
Een opvallend molecuul: DTB‑zuur
Uit deze enorme zoekactie kwam één molecuul naar voren — DTB‑zuur, een natuurlijk alkaloïde verwant aan matrinisch zuur. Gedetailleerde dockingsstudies toonden aan dat DTB‑zuur sterke, goed geplaatste contacten kon vormen binnen alle drie de eiwitten. Vervolgens voerde het team lange moleculaire dynamicasimulaties uit, die nabootsen hoe atomen zich in water over de tijd bewegen, om te controleren of de verbinding op zijn plek zou blijven in plaats van weg te drijven. Gedurende 100 miljardsten van een seconde gesimuleerde beweging bleven de eiwit‑geneesmiddelcomplexen stabiel. Extra energieberekeningen suggereerden dat de binding aan KMO bijzonder sterk was, terwijl een afzonderlijke analyse van watermoleculen in de bindingsplaatsen aangaf dat interacties met GSK‑3β ook thermodynamisch gunstig waren.
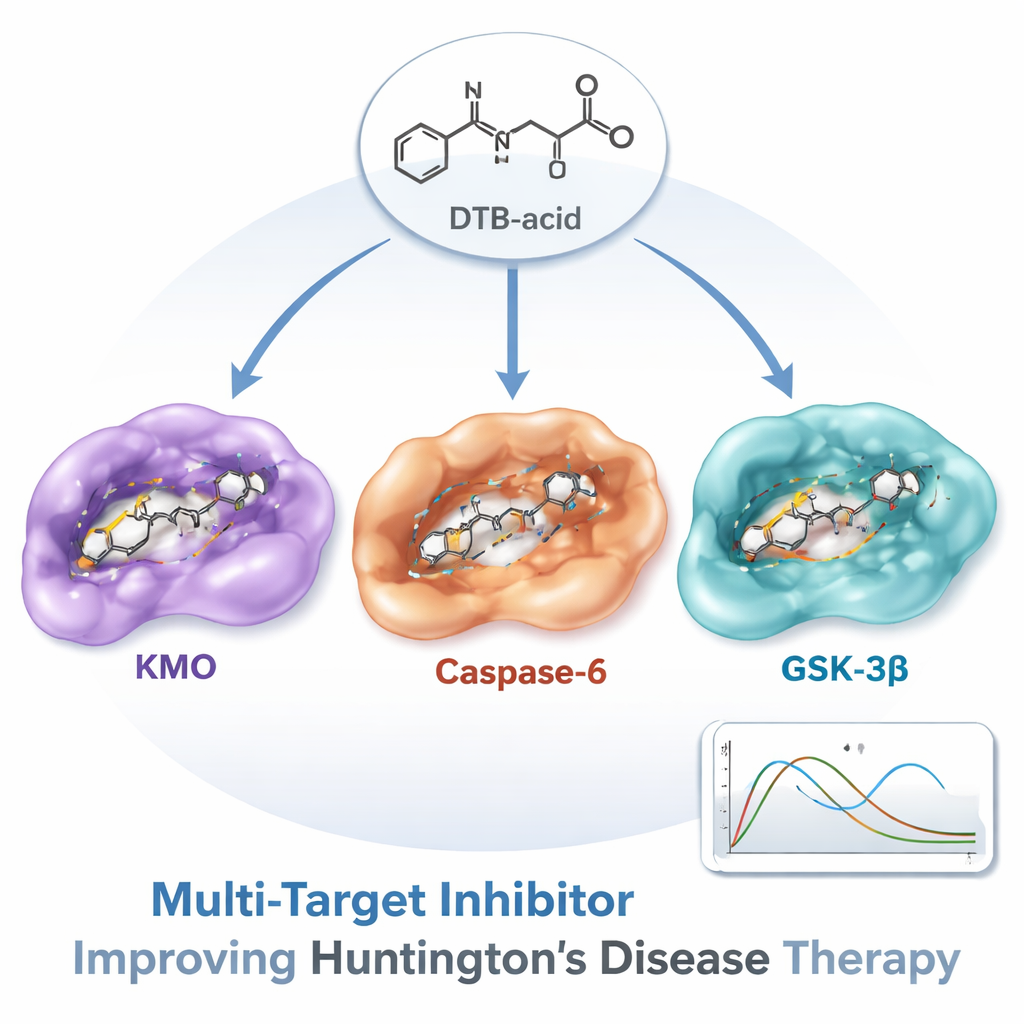
Van computergestuurde vondst naar toekomstig geneesmiddel
Natuurlijk is een molecuul dat veelbelovend oogt op een scherm slechts een eerste stap. De auteurs benadrukken dat DTB‑zuur nog in cellen en dieren moet worden getest om te bevestigen dat het de hersenen bereikt, zijn beoogde doelwitten raakt en daadwerkelijk neuronen beschermt zonder schadelijke bijwerkingen. Toch toont dit werk een krachtige, efficiënte route naar het ontdekken van multi‑target geneesmiddelen voor complexe hersenaandoeningen. Voor niet‑specialisten is de kernboodschap dat het, in plaats van Huntington te behandelen met een reeks afzonderlijke, smal gerichte geneesmiddelen, mogelijk is één zorgvuldig afgestemd verbinding zoals DTB‑zuur te ontwerpen die meerdere aanjagers van schade tegelijk aanpakt — wat nieuwe hoop biedt om het verloop van deze meedogenloze aandoening te vertragen of te veranderen.
Bronvermelding: Zheng, B., Banday, M., Gangwar, S. et al. In silico discovery of natural compound-derived multi-target inhibitor for Huntington’s disease therapy. Sci Rep 16, 7716 (2026). https://doi.org/10.1038/s41598-026-38430-w
Trefwoorden: Ziekte van Huntington, multi-target geneesmiddel, computational geneesmiddelenontdekking, natuurlijke verbindingen, neurodegeneratie