Clear Sky Science · nl
Geïntegreerde multi-dataset screening om prognose te voorspellen en immunotherapie-genen te identificeren bij patiënten met hepatocellulair carcinoom
Waarom dit belangrijk is voor mensen met leverkanker
Hepatocellulair carcinoom, de meest voorkomende vorm van primaire leverkanker, veroorzaakt jaarlijks honderden duizenden doden. Veel patiënten met hetzelfde ziektestadium reageren heel verschillend op behandelingen, met name op moderne immunotherapieën die het eigen immuunsysteem willen activeren. Deze studie stelt een eenvoudige maar cruciale vraag: kunnen we de genactiviteit van een tumor als een vingerafdruk lezen om te voorspellen wie het slecht zal doen, wie zal reageren op immuungebaseerde geneesmiddelen, en welke genen de beste nieuwe behandeldoelen zouden kunnen zijn?
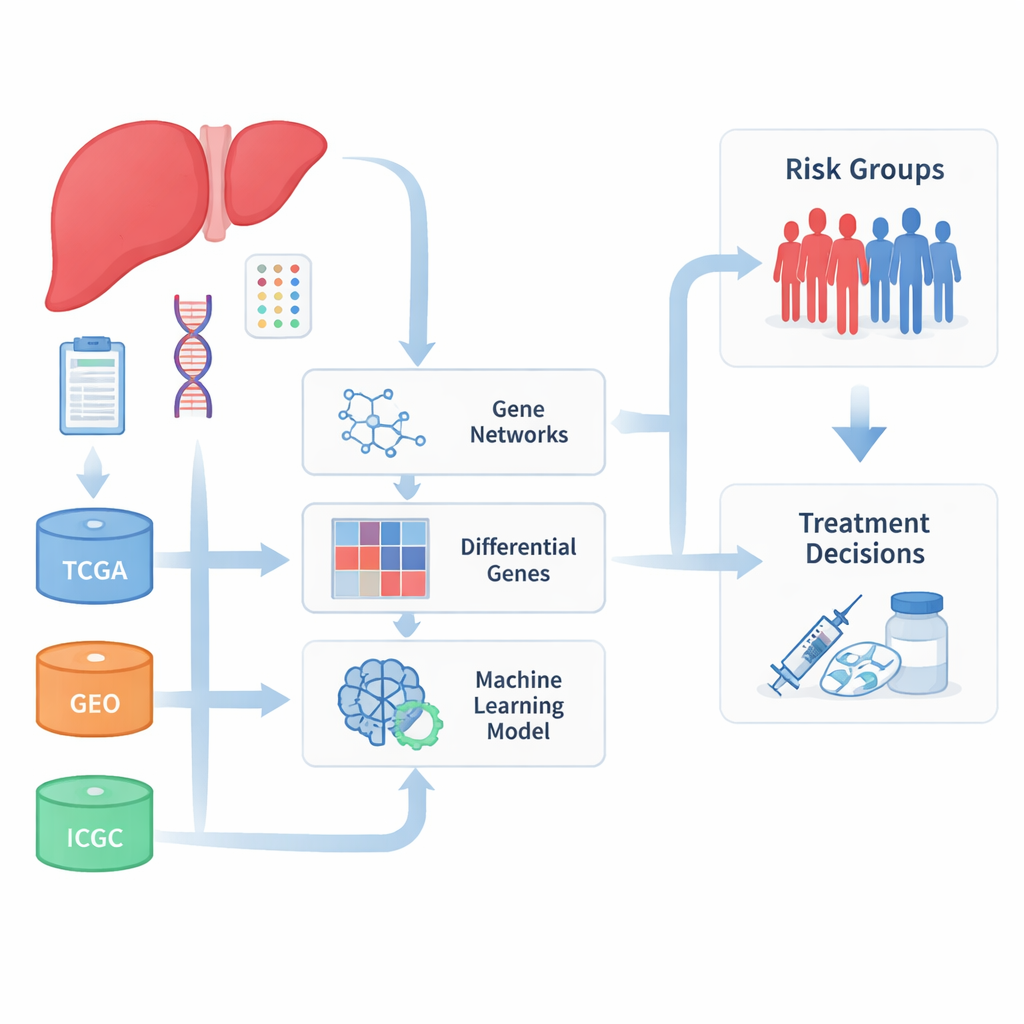
Veel datasets samenbrengen
De onderzoekers begonnen met het samenvoegen van grote verzamelingen leverkankermonsters uit verschillende internationale databases die tumor-genexpressie en klinische uitkomsten bewaren. Door data van The Cancer Genome Atlas, het International Cancer Genome Consortium en meerdere Gene Expression Omnibus-studies te combineren, stelden ze een veel grotere en diversere patiëntenpopulatie samen dan een enkel ziekenhuis of project zou kunnen bieden. Omdat deze datasets in verschillende laboratoria en met uiteenlopende methoden waren geproduceerd, investeerde het team eerst veel moeite in het corrigeren van technische verschillen, zodat echte biologische signalen — en niet laboratoriumruis — hun resultaten zouden bepalen.
Genvpatronen vinden die aan uitkomst zijn gekoppeld
Met de opgeschoonde gegevens in handen zocht het team naar groepen genen die de neiging hadden om samen aan- en uit te gaan en die tegelijk samenhingen met het ziekteverloop van patiënten. Met een netwerkachtige benadering clusterden ze duizenden genen in modules en concentreerden zich op die modules die het sterkst gekoppeld waren aan tumorgedrag en patiëntoverleving. Ze vergeleken ook tumoren met niet-tumorweefsel om genen te vinden die duidelijk meer of minder actief waren in kanker. De overlap tussen deze twee benaderingen leverde een set van 93 genen op die zowel veranderd waren bij leverkanker als nauw verbonden met belangrijke ziektekenmerken, waarvan vele betrokken bij hoe de lever geneesmiddelen verwerkt en met toxische stoffen omgaat.
Een risicoscore op basis van tien genen
Om deze genlijsten om te zetten in iets wat artsen mogelijk kunnen gebruiken, wendden de auteurs zich tot machine learning. Ze testten meer dan honderd combinaties van feature-selectie- en overlevingsvoorspellingsalgoritmen en beoordeelden ze op hoe nauwkeurig ze patiënten konden scheiden in groepen met betere en slechtere uitkomsten over meerdere onafhankelijke cohorten. Uit deze uitgebreide zoektocht destilleerden ze een compacte signatuur van tien genen die samen een risicoscore vormden. Patiënten met hoge scores hadden consequent kortere totale overleving, ziektevrije overleving en progressievrije overleving, zowel in de hoofdgegevenssets als in externe validatiegroepen. Onder deze genen viel TYMS op als een sterke indicator van slechte prognose, terwijl APOL3 en FBXO2 geassocieerd waren met gunstiger uitkomsten.
Aanwijzingen uit het immuunlandschap van de tumor
De studie ging verder dan voorspelling en onderzocht waarom deze genen van betekenis zijn. Met meerdere computationele hulpmiddelen schatte het team in welke typen immuuncellen in elke tumor aanwezig waren en hoe sterk de tien-genen-score relateerde aan dat immuunlandschap. Hoog-risico tumoren toonden vaak immuunpatronen en genveranderingen die gepaard gingen met meer mutaties en met tekenen van immuunontsnapping, inclusief verbanden met bekende checkpointmoleculen zoals PD-1 en CTLA-4. Ze onderzochten ook feitelijke mutatieprofielen en vonden dat hoog-risico tumoren vaker veranderingen in klassieke kankergenen zoals TP53 vertoonden. Tot slot bevestigden bloedtesten bij patiënten en gezonde vrijwilligers dat TYMS verhoogd en FBXO2 verlaagd was bij mensen met leverkanker, wat de indruk wekt dat deze genen biologisch actief zijn in de ziekte en niet slechts statistische artefacten.
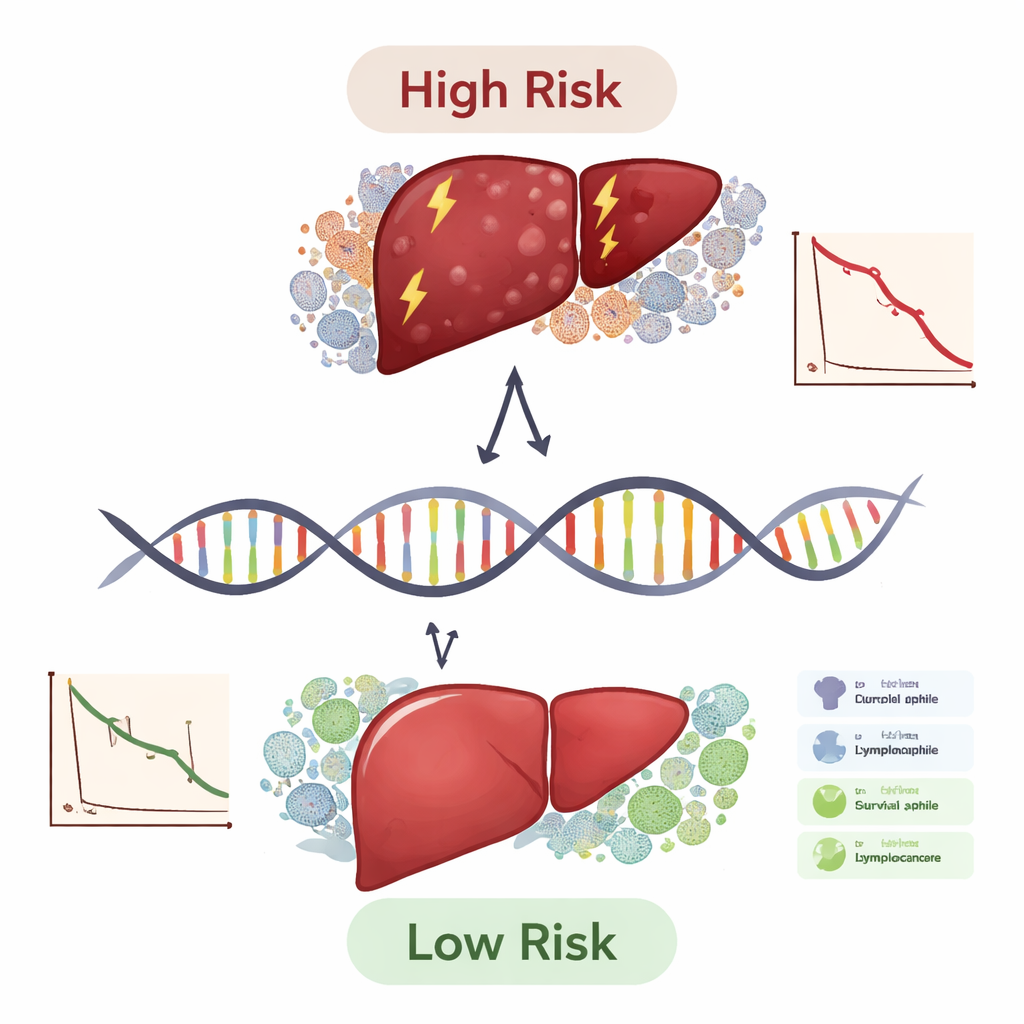
Wat dit betekent voor patiënten en artsen
Praktisch gezien biedt dit werk een blauwdruk voor het gebruik van een klein genpanel om leverkankerpatiënten in risicogroepen in te delen en om een aanwijzing te geven wie waarschijnlijk het meest profiteert van immuungebaseerde behandelingen. De tien-genen-score is nog geen klinisch kant-en-klare test, maar presteerde beter dan standaard stadiëringssystemen alleen en bleef nuttig over verschillende patiëntsubgroepen heen. Net zoals cholesterolpanelen de hartziektepreventie sturen, zou een dergelijk genpanel op een dag oncologen kunnen helpen bij het kiezen van agressievere therapie voor hoog-risicopatiënten, laag-risicopatiënten besparen van onnodige bijwerkingen, en geneesmiddelenontwikkelaars wijzen op nieuwe doelen zoals TYMS, APOL3 en FBXO2. Grotere prospectieve studies en laboratoriumexperimenten zullen nodig zijn, maar deze geïntegreerde analyse is een belangrijke stap richting meer gepersonaliseerde, biologisch gedreven zorg voor leverkanker.
Bronvermelding: Zhou, L., Zhang, W., Liu, Z. et al. Integrated multi-dataset screening to predict prognosis and identify immunotherapy gene targets in hepatocellular carcinoma patients. Sci Rep 16, 7014 (2026). https://doi.org/10.1038/s41598-026-38424-8
Trefwoorden: hepatocellulair carcinoom, gensequentie, immunotherapie, prognose, tumormicro-omgeving