Clear Sky Science · nl
CNOT2 /c-Myc/STAT3-signaalvoering speelt een cruciale rol in glycolyse-gemedieerde apoptose door benzylisothiocyanaat in hepatocellulair carcinoom
Een kankervijndig bestanddeel op uw bord
Benzylisothiocyanaat, kortweg BITC, is een natuurlijke stof die voorkomt in alledaagse groenten zoals broccoli, kool en boerenkool. Artsen weten al langer dat mensen die meer van deze groenten eten doorgaans lagere kankercijfers hebben, maar hoe specifieke plantaardige bestanddelen kankercellen vertragen of doden, wordt nog uitgezocht. Deze studie onderzoekt hoe BITC leverkankercellen in het laboratorium beïnvloedt en onthult een verrassende koppeling tussen de manier waarop kankercellen suiker verbranden en hoe ze worden aangezet tot zelfvernietiging.
Waarom leverkanker betere opties nodig heeft
Leverkanker behoort wereldwijd tot de dodelijkste vormen van kanker, en hepatocellulair carcinoom is de meest voorkomende subtype. Zelfs met chirurgie, chemotherapie en gerichte geneesmiddelen keren veel tumoren terug of verliezen ze hun gevoeligheid voor behandeling. Een reden is dat kankercellen hun energiegebruik herschikken: in plaats van voornamelijk op zuurstof in hun ‘energiecentrales’ (mitochondriën) te vertrouwen, verbranden ze grote hoeveelheden suiker zeer snel in een proces dat vaak het "Warburg-effect" wordt genoemd. Dit verstoorde suikergebruik helpt kankercellen sneller te groeien en weerstand tegen celdood te bieden. Het vinden van veilige manieren om deze energietoevoer te onderbreken, vooral met moleculen afkomstig uit voedsel, is daarom een aantrekkelijke strategie.
Een plantaardig chemisch middel testen op leverkankercellen
De onderzoekers behandelden twee menselijke leverkankercellijnen, SK-Hep1 en Huh7, met toenemende doses BITC. Naarmate de dosis toenam, overleefden minder cellen, wat aantoont dat BITC onder deze omstandigheden toxisch is voor leverkankercellen. Bij nadere bestudering van wat er in de cellen gebeurde, zagen ze klassieke kenmerken van geprogrammeerde celdood, of apoptose. Belangrijke eiwitten die normaal in een "inactieve" vorm bestaan voordat ze tijdens apoptose worden geknipt, zoals PARP en caspase-3, namen af in hun intacte, ofwel "pro-", vorm. Flowcytometrie-toetsen toonden ook meer cellen in de sub-G1-fractie van de celcyclus en meer cellen die positief waren voor Annexine V, beide aanwijzingen dat de kankercellen actief apoptose ondergingen in plaats van simpelweg beschadigd te zijn.
De suikerhonger van kanker afsluiten
Het team onderzocht vervolgens of BITC het Warburg-effect beïnvloedde. Ze maten eiwitten die kankercellen helpen suiker te verteren en om te zetten in energie en lactaat — specifiek HK2, PKM2 en LDH. BITC-behandeling verlaagde de niveaus van alle drie in beide leverkankercellijnen en verminderde zowel de hoeveelheid lactaat die de cellen afgaven als de hoeveelheid glucose die ze uit het kweekmedium verbruikten. Met andere woorden, BITC maakte leverkankercellen minder in staat hun hogesnelheid-suikerverbrandingsmachine te laten draaien. Toen de wetenschappers pyruvaat toevoegden, een downstreamproduct van suikerafbraak dat de stofwisseling nog steeds kan voeden, werden veel van de effecten van BITC teruggedraaid: de cellen herwonnen hogere niveaus van PARP, caspase-3 en de glycolyse-enzymen. Deze rescuing suggereert dat het verstoren van suikerverwerking een sleutelrol speelt in hoe BITC celdood teweegbrengt.
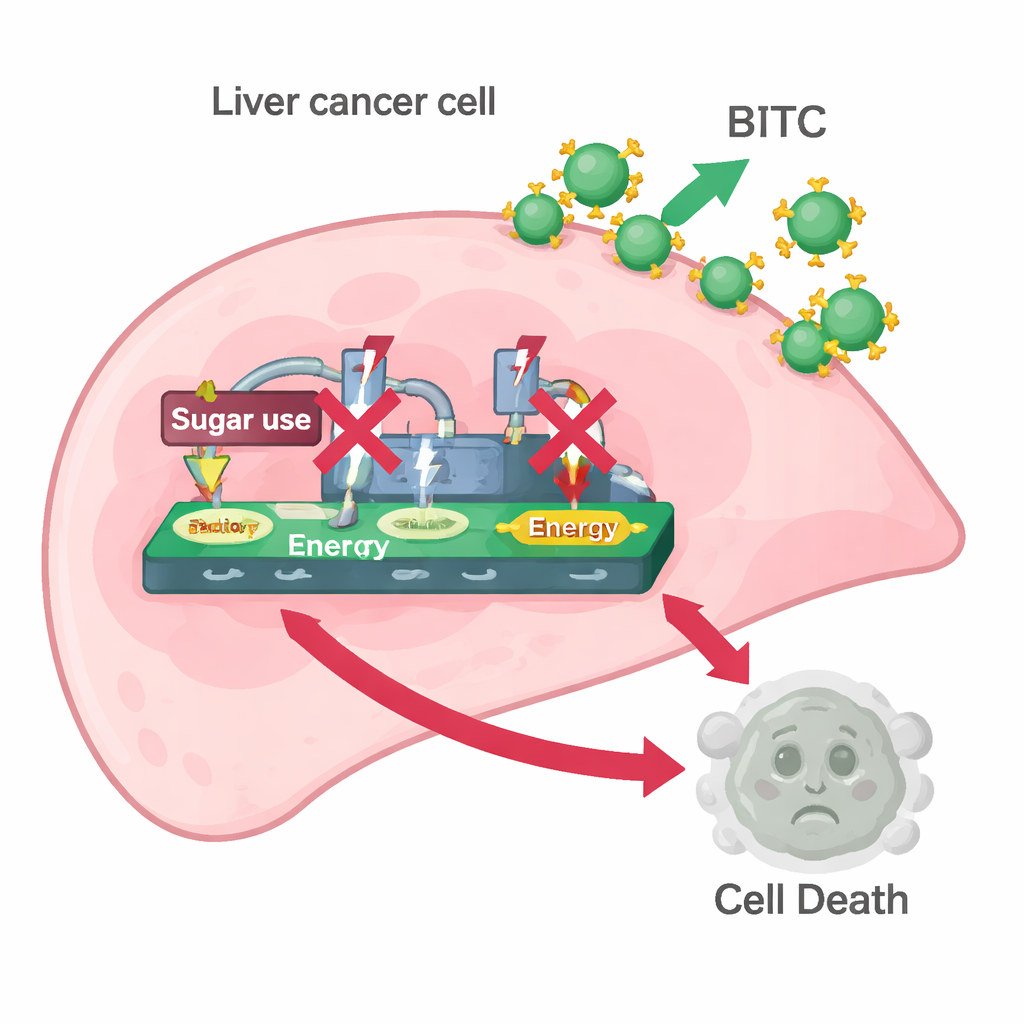
De schakelaars binnen de cel ontrafelen
Om diepere regelingslagen te begrijpen, richtten de onderzoekers zich op een signaleringstrio: CNOT2, c-Myc en STAT3. Deze eiwitten stimuleren groei, overleving en metabole herprogrammering in veel tumoren. Gegevens van leverkankerpatiënten toonden aan dat CNOT2 vaak hoger is bij mensen met slechtere uitkomsten. In het laboratorium verlaagde BITC de actieve, gefosforyleerde vorm van STAT3, zijn upstream-activator JAK1, het groeibevorderende eiwit c-Myc en CNOT2 zelf. Het gebruik van genetische middelen om CNOT2- of STAT3-niveaus te verlagen, maakte het dodeffect van BITC nog sterker, met verdere verlaging van PARP en caspase-3. Eiwit-bindingsexperimenten onthulden dat BITC ook de fysieke partnerschappen tussen CNOT2 en STAT3 en tussen CNOT2 en c-Myc verstoorde. Wanneer CNOT2 of c-Myc kunstmatig werden verhoogd, verloor BITC groot deel van zijn vermogen om glycolyse-enzymen uit te schakelen en apoptose te induceren, wat benadrukt dat deze signaleringsas fungeert als een hoofdschakel die suikermetabolisme en overleving verbindt.
Wat dit kan betekenen voor toekomstige therapieën
Samen genomen schetsen de bevindingen een samenhangend beeld: BITC valt leverkankercellen aan door hun geprefereerde suikergebaseerde brandstoftoevoer af te snijden en celdoodschakelaars om te zetten die afhankelijk zijn van de CNOT2/c-Myc/STAT3-as. Door zowel groeisignalen als suikergebruik te blokkeren, duwt BITC kankercellen voorbij een metabool kantelpunt in apoptose. Deze resultaten zijn afkomstig van kweekcelexperimenten, niet van patiënten, en slechts twee types leverkankercellen werden bestudeerd, dus veel meer werk in dieren en mensen is nodig. Toch versterkt het onderzoek het idee dat bepaalde verbindingen uit alledaagse groenten verfijnd of gecombineerd met andere behandelingen kunnen worden om levertumoren gerichter te ‘verhongeren’ terwijl ze worden aangezet tot zelfvernietiging.
Bronvermelding: Koh, W., Park, SY., Kim, B. et al. CNOT2 /c-Myc/STAT3 signaling is critically involved in glycolysis mediated apoptosis of benzyl isothiocyanate in hepatocellular carcinoma. Sci Rep 16, 7000 (2026). https://doi.org/10.1038/s41598-026-38416-8
Trefwoorden: leverkanker, benzylisothiocyanaat, kankermetabolisme, apoptose, kruisbloemige groenten