Clear Sky Science · nl
Toepassingsanalyse van een getransfecteerde celmethode voor het detecteren van AChR-antistoffen bij MG-patiënten
Waarom dit belangrijk is voor mensen met spierzwakte
Myasthenia gravis is een ziekte waarbij het afweersysteem van het lichaam de locaties aanvalt waar zenuwen met spieren communiceren, wat leidt tot afhangende oogleden, moeite met kauwen en algemene vermoeidheid. Artsen vertrouwen op bloedtesten die deze misgeleide antistoffen opsporen, maar de huidige tests missen nog een aanzienlijk deel van de patiënten. Deze studie onderzoekt een nieuwere, celgebaseerde methode om die antistoffen betrouwbaarder te vinden, wat kan leiden tot eerdere diagnoses en betere behandelrichtlijnen.
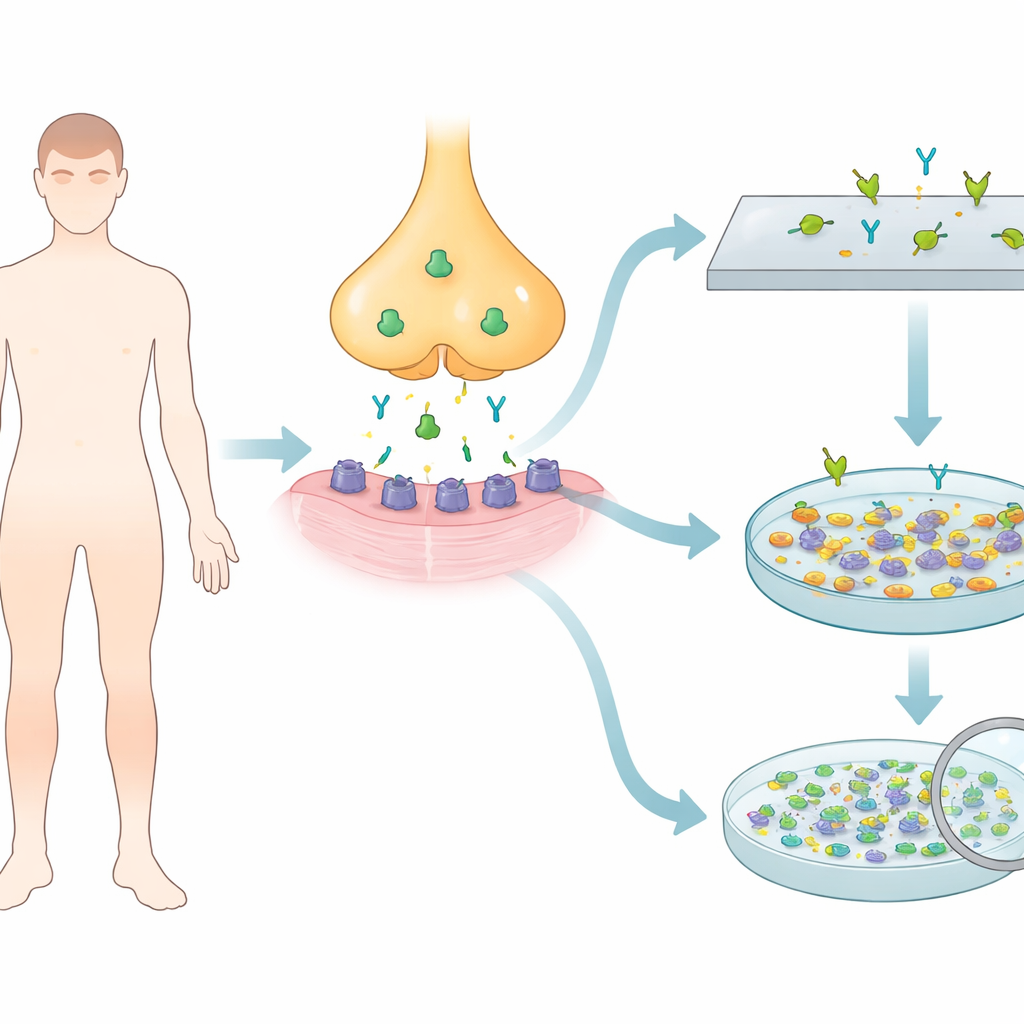
Een verborgen aanval op het zenuw–spierovergangspunt
Bij myasthenia gravis richt het immuunsysteem zich op een sleutelproteïne, de acetylcholinereceptor, die fungeert als een poort waardoor zenuwsignalen spierbewegingen activeren. De meeste patiënten met gegeneraliseerde ziekte, en veel met uitsluitend oogsymptomen, dragen antistoffen tegen deze receptor in hun bloed. Toch testen tot de helft van de mensen met enkel oogklachten en ongeveer 10–15 procent van degenen met wijdverspreide zwakte negatief met standaardbloedtesten. Een waarschijnlijke reden is dat sommige antistoffen slechts zwak aan de receptor hechten en daardoor standaardtests omzeilen die gezuiverde of vereenvoudigde vormen van het eiwit gebruiken.
Van gewone cellen naar gevoelige testplatforms
De onderzoekers wilden een interne celgebaseerde assay ontwikkelen met een menselijke cellijn die vaak in laboratoria wordt gebruikt. Ze voegden genetische instructies in voor verschillende combinaties van receptoronderdelen — volwassen type, foetaal type en een mengsel van beide — plus een hulpproteïne dat receptoren op het celoppervlak clustert. Deze gemodificeerde cellen werden op kleine glasplaatjes gekweekt en gefixeerd zodat ze als kant-en-klare testglazen konden worden bewaard. Wanneer verdunde patiëntserums werden toegevoegd, zouden eventuele antistoffen tegen de receptor aan deze gecentraliseerde eiwitten hechten en met een fluorescent secundair antilichaam zichtbaar worden gemaakt onder een microscoop.
De beste combinatie vinden om meer antistoffen te vangen
Het team ontdekte eerst dat cellen die slechts één receptoronderunit tot expressie brachten niet oplichtten, zelfs niet wanneer ze werden getest met 48 monsters die positief waren volgens een commercieel kit. Dit suggereert dat antistoffen van patiënten de volledige driedimensionale vorm van de receptor op het celoppervlak herkennen, en niet eenzame stukjes die nog in de cel gevangen zitten. Daarentegen lieten cellen die compleet volwassen of foetale receptorcombinaties tot expressie brachten duidelijke fluorescente signalen zien bij blootstelling aan positieve sera, terwijl controlemonsters van gezonde personen donker bleven. De sterkste en meest frequente signalen traden op wanneer cellen zowel volwassen als foetale receptorvormen samen tot expressie brachten, met name bij monsters met lagere antistofniveaus. In een set van 24 zorgvuldig geselecteerde pediatrische en volwassen patiënten produceerde deze ‘volledige combinatie’-slide matige tot sterke signalen in ongeveer tweederde van de gevallen, en overtrof daarmee glazenslides die alleen volwassen of alleen foetale receptoren toonden.
Face-to-face met een standaardbloedtest
Om te zien hoe hun celgebaseerde aanpak zich verhoudde tot een veelgebruikte enzymgekoppelde immunosorbentassay (ELISA), testten de onderzoekers 85 patiënten met myasthenia gravis met beide methoden. De ELISA detecteerde receptorantistoffen bij ongeveer 68 procent van de patiënten, terwijl de celgebaseerde assay ze in meer dan 75 procent detecteerde. Over het geheel genomen kwamen de twee tests goed overeen — de statistische maat voor overeenkomst, kappa genoemd, was hoog — toch waren er acht patiënten waarbij de uitkomsten verschilden. Toen een radioimmunoassay, beschouwd als referentiemethode, werd gebruikt om deze conflicten te beslechten, kwam deze in zes van de acht gevallen overeen met de celgebaseerde assay. Dit patroon suggereert dat de celgebaseerde test sommige laagaffiniteitsantistoffen kan detecteren die ELISA mist, zonder in te boeten op specificiteit.
Wat dit betekent voor patiënten en artsen
Door gewone laboratoriumcellen dicht opeengepakte, mix-leeftijdsversies van de acetylcholinereceptor te laten tonen, creëerde deze studie een gevoeliger spotlight voor ziekteveroorzakende antistoffen bij myasthenia gravis. De nieuwe assay presteert overall minstens even goed als bestaande commerciële kits en kan beter zijn in het opsporen van moeilijk detecteerbare antistoffen, met name bij patiënten met lage niveaus of complexere antistofprofielen. Hoewel grotere, multicenterstudies en verfijningen met levende cellen nog nodig zijn vóór brede toepassing, schetst dit werk een praktische route naar nauwkeuriger bloedonderzoek, waarmee artsen eerder diagnoses kunnen bevestigen, de ziekte preciezer kunnen volgen en behandelingen beter kunnen afstemmen voor mensen die met deze spierverzwakkende aandoening leven.
Bronvermelding: Liu, W., Xia, Z., Hu, J. et al. Application analysis of transfected cell method for detecting AChR antibodies in MG patients. Sci Rep 16, 8130 (2026). https://doi.org/10.1038/s41598-026-38414-w
Trefwoorden: myasthenia gravis, acetylcholinereceptor-antistoffen, celgebaseerde test, auto-imuun neuromusculaire aandoening, diagnostische gevoeligheid